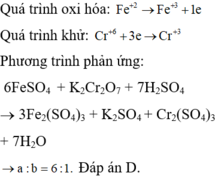Các câu hỏi tương tự
Cho các phương trình phản ứng sau: (a) Fe + 2HCl ® FeCl2 + H2 (b) Fe3O4 + 4H2SO4 ® Fe2(SO4)3 + FeSO4 + 4H2O (c) 16HCl + 2KMnO4 ® 2KCl + 2MnCl2 + 5Cl2 + 8H2O (d) FeS + H2SO4 ® FeSO4 + H2S (e) 2Al + 3H2SO4 ® Al2(SO4)3 + 3H2 Trong các phản ứng trên, số phản ứng mà ion H+ đóng vai trò chất oxi hóa là: A. 2 B. 4 C. 3 D. 1
Đọc tiếp
Cho các phương trình phản ứng sau:
(a) Fe + 2HCl ® FeCl2 + H2
(b) Fe3O4 + 4H2SO4 ® Fe2(SO4)3 + FeSO4 + 4H2O
(c) 16HCl + 2KMnO4 ® 2KCl + 2MnCl2 + 5Cl2 + 8H2O
(d) FeS + H2SO4 ® FeSO4 + H2S
(e) 2Al + 3H2SO4 ® Al2(SO4)3 + 3H2
Trong các phản ứng trên, số phản ứng mà ion H+ đóng vai trò chất oxi hóa là:
A. 2
B. 4
C. 3
D. 1
Cho phương trình: Fe(NO3)2 + KHSO4 ® Fe(NO3)3 + Fe2(SO4)3 + K2SO4 + NO + H2O Sau khi cân bằng với các hệ số của các chất là số nguyên nhỏ nhất thì tổng hệ só các chất tham gia phản ứng là A. 18 B. 21 C. 22 D. 23
Đọc tiếp
Cho phương trình: Fe(NO3)2 + KHSO4 ® Fe(NO3)3 + Fe2(SO4)3 + K2SO4 + NO + H2O
Sau khi cân bằng với các hệ số của các chất là số nguyên nhỏ nhất thì tổng hệ só các chất tham gia phản ứng là
A. 18
B. 21
C. 22
D. 23
Cho phản ứng: K2Cr2O7 + K2SO3 + KHSO4 ® K2SO4 + Cr2(SO4)3 + H2O Sau khi cân bằng tổng các hệ số (nguyên, tối giản) của phương trình thu được là: A. 19 B. 25 C. 21 D. 41
Đọc tiếp
Cho phản ứng: K2Cr2O7 + K2SO3 + KHSO4 ® K2SO4 + Cr2(SO4)3 + H2O
Sau khi cân bằng tổng các hệ số (nguyên, tối giản) của phương trình thu được là:
A. 19
B. 25
C. 21
D. 41
Cho sơ đồ phản ứng: H2SO4 (đặc nóng) + Fe ® Fe2(SO4)3 + SO2 +H2O Số phân tử H2SO4 bị khử trong phương trình hoá học của phản ứng trên là A. 2. B. 4. C. 6. D. 3.
Đọc tiếp
Cho sơ đồ phản ứng: H2SO4 (đặc nóng) + Fe ® Fe2(SO4)3 + SO2 +H2O
Số phân tử H2SO4 bị khử trong phương trình hoá học của phản ứng trên là
A. 2.
B. 4.
C. 6.
D. 3.
Cho phản ứng: FeSO4 + K2Cr2O7 + H2SO4 ® Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O Tổng hệ số cân bằng của các chất bên vế trái là: A. 12 B. 14 C. 8 D. 26
Đọc tiếp
Cho phản ứng: FeSO4 + K2Cr2O7 + H2SO4 ® Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
Tổng hệ số cân bằng của các chất bên vế trái là:
A. 12
B. 14
C. 8
D. 26
Cho phản ứng 6FeSO4 + K2Cr2O7 + 7H2SO4 ® 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là: A. FeSO4 và K2Cr2O7 B. K2Cr2O7 và FeSO4 C. H2SO4 và FeSO4 D. K2Cr2O7 và H2SO4
Đọc tiếp
Cho phản ứng
6FeSO4 + K2Cr2O7 + 7H2SO4 ® 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là:
A. FeSO4 và K2Cr2O7
B. K2Cr2O7 và FeSO4
C. H2SO4 và FeSO4
D. K2Cr2O7 và H2SO4
Cân bằng các phương trình sao1. FeCO3 + H2SO4 --- Fe2(SO4)3 + SO2 + CO2 + H2O.2. FeSO4 + H2SO4 ---- Fe2(SO4)3 + SO2 + H2O.3. Fe(OH)2 + H2SO4 ------ Fe2(SO4)3 + SO2 + H2O.4. Fe(NO3)2 + HNO3 ------- Fe(NO3)3 + NO + H2O.5. K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O6. KClO3 + HCl → KCl + Cl2 + H2O7. KNO3+ Al → KNO2 + Al2O38. KClO3+ S → KCl + SO29. KMnO4 + SO2 + H2O ---- MnSO4 + K2SO4 + H2SO4.10. K2Cr2O7 + FeSO4 + H2SO4 -------- Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 +...
Đọc tiếp
Cân bằng các phương trình sao
1. FeCO3 + H2SO4 ---> Fe2(SO4)3 + SO2 + CO2 + H2O.
2. FeSO4 + H2SO4 ----> Fe2(SO4)3 + SO2 + H2O.
3. Fe(OH)2 + H2SO4 ------> Fe2(SO4)3 + SO2 + H2O.
4. Fe(NO3)2 + HNO3 -------> Fe(NO3)3 + NO + H2O.
5. K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O
6. KClO3 + HCl → KCl + Cl2 + H2O
7. KNO3+ Al → KNO2 + Al2O3
8. KClO3+ S → KCl + SO2
9. KMnO4 + SO2 + H2O ----> MnSO4 + K2SO4 + H2SO4.
10. K2Cr2O7 + FeSO4 + H2SO4 --------> Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O.
Cho phuong trình phản ứng:
K
2
C
r
2
O
7
+
C
u
F
e
S
2
+
H
B
r
+
H
2
S
O
4
→
K
2
S
O
4
+
B...
Đọc tiếp
Cho phuong trình phản ứng:
K 2 C r 2 O 7 + C u F e S 2 + H B r + H 2 S O 4 → K 2 S O 4 + B r 2 + C u S O 4 + F e 2 ( S O 4 ) 3 + H 2 O + C r 2 ( S O 4 ) 3
Tổng các hệ số cân bằng (nguyên, tối giản) trong phương trình trên là:
A. 180
B. 327
C. 88
D. 231
Cho phương trình phản ứng: Al + HNO3 ® Al(NO3)3 + N2O + NO + H2O Nếu tỉ lệ giữa N2O và NO là
2
:
3
thì sau khi cân bằng ta có tỉ lệ số mol
n
A
l
:
n
N
O
2
:
n
N
O
là:
Đọc tiếp
Cho phương trình phản ứng: Al + HNO3 ® Al(NO3)3 + N2O + NO + H2O
Nếu tỉ lệ giữa N2O và NO là 2 : 3 thì sau khi cân bằng ta có tỉ lệ số mol n A l : n N O 2 : n N O là:
![]()
![]()
![]()
![]()