Chỉ số axit của mẫu chất béo tristearoylglixerol trên là 7. Nghĩa là cần 7mg KOH (= 0,007g KOH) trung hòa axit tự do trong 1 g chất béo
⇒ nKOH = 0,007/56 = 0,125.10-3 mol
⇒ naxit stearic = nKOH = 0,125.10-3 mol
(axit stearic: C17H35COOH) ⇒ maxit stearic = 0,125.10-3. 284 = 35,5.10-3g
⇒ Lượng tristearoylglixerol (C17H35COO)3C3H5 có trong 1g chất béo là: 1- 35,5.10-3 = 0,9645 g
n(C17H35COO)3C3H5 = 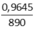 = 1,0837.10-3 mol
= 1,0837.10-3 mol
Phương trình hóa học
(C17H35COO)3C3H5 + 3KOH → 3C17H35COOK + C3H5(OH)3
⇒ nKOH = 3. n(C17H35COO)3C3H5 = 3. 1,0837.10-3 = 3,2511.10-3 mol
Số g KOH tham gia xà phòng hóa = 3,2511.10-3. 56 ≈ 182.10-3g = 182mg
Chỉ số xà phòng hóa của chất béo tristearoylixerol là 182 + 7 = 189



