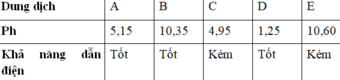
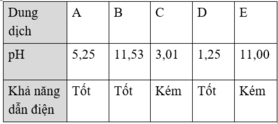
HD:
CH3COOH \(\leftrightarrow\) CH3COO- + H+
Ban đầu: 0,1 M 0,1 M 0
Cân bằng: 0,1-x 0,1+x x
Hằng số cb: ka = [CH3CO-][H+]/[CH3COOH] = (0,1+x).x/(0,1-x) = 1,76.10-5. Giải pt thu được x, mà [H+] = x nên pH = -log[H+] = -log(x).
em cũng có thể dùng công thức pH= -LogKa + Log(Cb/Ca)
với Cb,Ca là nồng độ bazo và axit
đấy là công thức gần đúng, trong một số trường hợp cần sự chính xác thì công thức đó ko dùng được