Oxy hóa hoàn toàn a(g) hỗn hợp X (gồm Zn, Pb, Ni) được b(g) hỗn hợp 3 oxit Y (ZnO, PbO, NiO). Hòa tan b(g) Y trên trong dung dịch HCl loãng thu được dung dịch Z. Cô cạn Z được hỗn hợp muối khan có khối lượng (b + 55) gam. Khối lượng a(g) của hỗn hợp X ban đầu là:
A. a = b - 16
B. a = b - 24
C. a = b - 32
D. a = b - 8
Áp dụng tăng giảm khối lượng, ta thấy 1 nguyên tử O được thay thế bởi 2 nguyên tử Cl.
ZnO, PbO, NiO → Z n C l 2 , P b C l 2 , N i C l 2
⇒ Từ 1 mol oxit ban đầu khối lượng muối sau phản ứng tăng là:
m↑= m 2 C l - m O = 2.35,5 - 16 = 55g
m h h b a n d a u = m F e 3 O 4 + m C u p ư = , 12 . 232 + 0 , 12 . 64 + 8 , 32 = 43 , 84 g
Theo bài ra, ta có:
m↑ = m m u o i - m h h o x i t = (b +55) - b = 55g
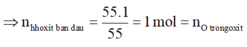
⇒mX = m h h o x i t b a n d a u - m O =b-16 = a
⇒ Chọn A.










