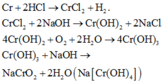Các câu hỏi tương tự
Cho dãy biến hóa sau:
R
→
(
1
)
R
C
l
2
→
(
2
)
R
(
O
H
)
2
→
(
3...
Đọc tiếp
Cho dãy biến hóa sau:
R → ( 1 ) R C l 2 → ( 2 ) R ( O H ) 2 → ( 3 ) R ( O H ) 3 → ( 4 ) N a R O 2
R có thể là kim loại nào sau đây?
A. Fe.
B. Fe hoặc Cr.
C. Cr.
D. Al.
Nung nóng từng cặp chất sau trong bình kín: (1) Fe + S (r); (2) Fe2O3 + CO (k); (3) Au + O2 (k); (4) Li + N2 ; (5) Cu + KNO3 (r); (6) Al + NaCl (r); (7) Fe + Cr2O3; (8) Mg + CaCO3 (r); Số trường hợp xảy ra phản ứng oxi hoá kim loại là
Đọc tiếp
Nung nóng từng cặp chất sau trong bình kín:
(1) Fe + S (r); (2) Fe2O3 + CO (k);
(3) Au + O2 (k); (4) Li + N2 ;
(5) Cu + KNO3 (r); (6) Al + NaCl (r);
(7) Fe + Cr2O3; (8) Mg + CaCO3 (r);
Số trường hợp xảy ra phản ứng oxi hoá kim loại là
![]()
![]()
![]()
![]()
Hỗn hợp X gồm Na, Al và Fe, hỗn hợp Y gồm Al và kim loại R. Biết rằng, khối lượng của Al có trong X và Y bằng nhau, tổng khối lượng của Na và Fe có trong X gấp 2 lần khối lượng của R có trong Y. Hòa tan hoàn toàn lần lượt X, Y băng lượng dư dung dịch
H
2
SO
4
loãng thì cả 2 trường hợp đều thu được V lít khí H2 (đktc). Kim loại R là A. Ca. B. Be. C. Zn. D. Mg.
Đọc tiếp
Hỗn hợp X gồm Na, Al và Fe, hỗn hợp Y gồm Al và kim loại R. Biết rằng, khối lượng của Al có trong X và Y bằng nhau, tổng khối lượng của Na và Fe có trong X gấp 2 lần khối lượng của R có trong Y. Hòa tan hoàn toàn lần lượt X, Y băng lượng dư dung dịch H 2 SO 4 loãng thì cả 2 trường hợp đều thu được V lít khí H2 (đktc). Kim loại R là
A. Ca.
B. Be.
C. Zn.
D. Mg.
Hòa tan hoàn toàn 2,16 gam kim loại R trong H2SO4 đặc, nóng thu được dung dịch X và 0,224 lít khí SO2 (đkc). R là kim loại nào sau đây? (Fe56; Cu64; Cr52; Ag108) A. Fe B. Zn C. Cu D. Ag
Đọc tiếp
Hòa tan hoàn toàn 2,16 gam kim loại R trong H2SO4 đặc, nóng thu được dung dịch X và 0,224 lít khí SO2 (đkc). R là kim loại nào sau đây? (Fe=56; Cu=64; Cr=52; Ag=108)
A. Fe
B. Zn
C. Cu
D. Ag
Oxit cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3. Cho các nhận định về R: (1) R có hóa trị cao nhất với oxi là 6. (2) Công thức hợp chất khí của R với H có dạng RH2. (3) R là một phi kim. (4) Axit tương ứng với oxit cao nhất của R là H2RO3 Số nhận định đúng là: A. 1. B. 2. C. 3. D. 4.
Đọc tiếp
Oxit cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3. Cho các nhận định về R:
(1) R có hóa trị cao nhất với oxi là 6.
(2) Công thức hợp chất khí của R với H có dạng RH2.
(3) R là một phi kim.
(4) Axit tương ứng với oxit cao nhất của R là H2RO3
Số nhận định đúng là:
A. 1.
B. 2.
C. 3.
D. 4.
Cho sơ đồ phản ứng sau: R + H2SO4 (loãng, nguội)
→
y RSO4 + H2 RSO4 + Cl2
→
R2(SO4)3 + RCl3 R2(SO4)3 + KOH(dư)
→
R(OH)3 + K2SO4 Kim loại R là A. Cr B. Al C. Cu D. Fe
Đọc tiếp
Cho sơ đồ phản ứng sau:
R + H2SO4 (loãng, nguội) → y RSO4 + H2
RSO4 + Cl2 → R2(SO4)3 + RCl3
R2(SO4)3 + KOH(dư) → R(OH)3 + K2SO4
Kim loại R là
A. Cr
B. Al
C. Cu
D. Fe
Cho sơ đồ phản ứng sau:
R
+
H
2
S
O
4
→
R
S
O
4
+
H
2
R
S
O
4
+
C
l
2
→
R
2
S
O...
Đọc tiếp
Cho sơ đồ phản ứng sau:
R + H 2 S O 4 → R S O 4 + H 2 R S O 4 + C l 2 → R 2 S O 4 3 + R C l 3 R 2 S O 4 3 + K O H d ư → R O H 3 + K 2 S O 4
Kim loại R là
A. Cr
B. Al
C. Cu
D. Fe
Để oxi hóa hết 6,0 gam kim loại R hóa trị 2 cần vừa đủ 0,15 mol khí Cl2. Kim loại R là
A. Ba
B. Be
C. Mg
D. Ca
Cho sơ đồ phản ứng sau:
R
+
2
HCl
loãng
→
RCl
2
+
H
2
;
2
R
+
3
Cl
2
→
t
o
2
RCl
3
4
R
OH
2...
Đọc tiếp
Cho sơ đồ phản ứng sau:
R + 2 HCl loãng → RCl 2 + H 2 ;
2 R + 3 Cl 2 → t o 2 RCl 3
4 R OH 2 + O 2 → t o 2 R 2 O 3 + 4 H 2 O
Kim loại R là
A. Fe.
B. Al.
C. Mg.
D. Cu.