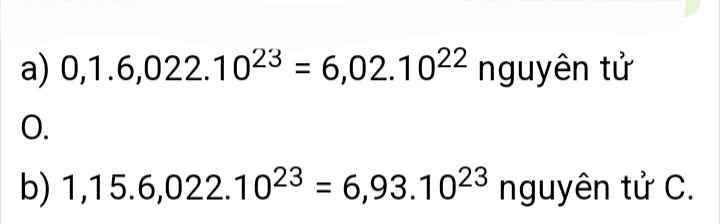Câu 1 Tính số nguyên tử hoặc phân tử có trong những lượng chất sau:
a) 0, 5 mol nguyên tử O.
b) 1, 55 mol nguyên tử C.
Câu 2. Tính số mol nguyên tử hoặc mol phân tử trong những lượng chất sau:
a) 16, 428.1022 nguyên tử K.
b) 2, 505.1024 phân tử SO2.
Câu 3 Khi cho m gam kim loại Mg phản ứng với dung dịch hydrochloric acid dư thu được muối Magnesium chloric (MgCl2) và 6,958 lít khí hydrogen ở 250C, 1 bar. Tính m?
Nhanh giúp mình và viết rõ 1 tí ạ
Câu 1:
a) Để tính số nguyên tử trong 0,5 mol nguyên tử O, ta sử dụng công thức:
Số nguyên tử = số mol x số Avogadro
Số nguyên tử O = 0,5 mol x 6,022 x 10^23 nguyên tử/mol = 3,011 x 10^23 nguyên tử
b) Tương tự, để tính số nguyên tử trong 1,55 mol nguyên tử C:
Số nguyên tử C = 1,55 mol x 6,022 x 10^23 nguyên tử/mol = 9,331 x 10^23 nguyên tử
Câu 2:
a) Để tính số mol nguyên tử trong 16,428 x 10^22 nguyên tử K, ta sử dụng công thức:
Số mol = số nguyên tử / số Avogadro
Số mol K = 16,428 x 10^22 nguyên tử / 6,022 x 10^23 nguyên tử/mol = 0,0272 mol
b) Tương tự, để tính số mol phân tử trong 2,505 x 10^24 phân tử SO2:
Số mol SO2 = 2,505 x 10^24 phân tử / 6,022 x 10^23 phân tử/mol = 4,16 mol
Câu 3:
Để tính m, ta sử dụng phương trình phản ứng giữa Mg và HCl:
Mg + 2HCl -> MgCl2 + H2
Theo phương trình, ta thấy 1 mol Mg tạo ra 1 mol H2. Vì vậy, 6,958 lít H2 (ở điều kiện tiêu chuẩn) tương ứng với 1 mol H2.
Vậy, số mol H2 = 6,958 lít / 22,4 lít/mol = 0,31 mol
Do đó, số mol Mg cần để tạo ra 0,31 mol H2 là 0,31 mol.
Molar mass của Mg là 24,31 g/mol.
Vậy, m = số mol x molar mass = 0,31 mol x 24,31 g/mol = 7,53 g.