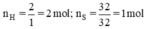Ta có: `dA/H2d` = `MA\MH2`
=> `17` = `MA\2`
=> `MA` = `17. 2 = 34` (g/mol)
Nên: `mH` = `frac{5.88.34}{100}` = `2` `(g)`
=> `mS` = `34 - 2` = `32` `(g)`
<=> `nH` = `2\1` = `2` `(mol)`
`nS` = `32\32` = `1` `(mol)`
Vậy trong phân tử `A` có 2 nguyên tử `H` và 1 nguyên tử `S`.
Công thức hóa học của `A` là `H2S`
Khối lượng mol của khí A : dA/H2 = 17 ⇒ MA = 17.2 = 34 (g)
Khối lượng mỗi nguyên tố có trong 1 mol khí A:

mS = 34 – 2 = 32 (g)
Số mol nguyên tử mỗi nguyên tố trong 1 mol khí A có: