Đáp án A
Gọi số mol N2 phản ứng là x (mol).
Phản ứng: N2 (k) + 3H2 (k) D 2NH3 (k)
Ban đầu: 0,4M 0,6M 0
Phán úng: x 3x 2x
Cần bằng: (0,4-x) (0,6-3x) 2x
H2 chiếm 25% hỗn hợp sau phản ứng nên:
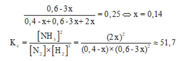
Đáp án A
Gọi số mol N2 phản ứng là x (mol).
Phản ứng: N2 (k) + 3H2 (k) D 2NH3 (k)
Ban đầu: 0,4M 0,6M 0
Phán úng: x 3x 2x
Cần bằng: (0,4-x) (0,6-3x) 2x
H2 chiếm 25% hỗn hợp sau phản ứng nên:
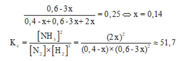
Một bình kín dung tích không đổi chứa hỗn hợp khí N2 và H2 với nồng độ tương ứng là 0,4 M và 0,6 M. Sau khi phản ứng tổng hợp NH3 đạt trạng thái cân bằng ở t°C, H2 chiếm 25% thể tích hỗn hợp thu được. Hằng số cân bằng Kc ở t0C của phản ứng có giá trị là:
A. 51,7
B. 3,125
C. 2,500
D. 6,09
Một bình kín chứa khí NH3 ở 0°C và 1 atm với nồng độ 1M. Nung bình kín đó đến 546°C, NH3 bị phân hủy theo phản ứng: 2NH3 (k) D N2 (k) + 3H2 (k). Khi phản ứng đạt tới trạng thái cân bằng, áp suất trong bình là 3,3 atm. Thể tích bình không đổi. Giá trị hằng số cân bằng của phản ứng tại 546°C là:
A.4807
B.120
C.8,33.10-3
D.2,08.10-4
Một bình kín chứa khí NH3 ở 0°C và 1 atm với nồng độ 1M. Nung bình kín đó đến 546°C, NH3 bị phân hủy theo phản ứng: 2NH3 (k) D N2 (k) + 3H2 (k). Khi phản ứng đạt tới trạng thái cân bằng, áp suất trong bình là 3,3 atm. Thể tích bình không đổi. Giá trị hằng số cân bằng của phản ứng tại 546°C là:
A.4807
B.120
C.8,33.10-3
D.2,08.10-4
Cho phản ứng sau:
H2O (k) + CO (k) D H2 (k) + CO2 (k)
Ở 700°C hằng số cân bằng là Kc = 1,873. Biết rằng hỗn hợp đầu gồm 0,300 mol H2O và 0,300 mol CO trong bình 10 lít ở 700°C. Nồng độ của H2O và CO ở trạng thái cân bằng lần lượt là:
A.0,01267M
B.0,01733M
C. 0,1267M
D.0,1733M
Cho phản ứng sau:
H2O (k) + CO (k) D H2 (k) + CO2 (k)
Ở 700°C hằng số cân bằng là Kc = 1,873. Biết rằng hỗn hợp đầu gồm 0,300 mol H2O và 0,300 mol CO trong bình 10 lít ở 700°C. Nồng độ của H2O và CO ở trạng thái cân bằng lần lượt là:
A. 0,01267M
B. 0,01733M
C. 0,1267M
D. 0,1733M
Khi phản ứng .N2 (k) + 3H2 (k) ⇄ 2NH3 (k) đạt đến trạng thái cân bằng thì hỗn hợp khí thu được có thành phần. 1,5
mol NH3, 2 mol N2 và 3 mol H2. Vậy số mol ban đầu của H2 là.
A. 3 mol
B. 4 mol
C. 5,25 mol
D. 4,5 mol
Ở một nhiệt độ nhất định, phản ứng thuận nghịch N 2 ( k ) + 3 H 2 ( k ) ⇔ 2 NH 3 ( k ) đạt trạng thái cân bằng khi nồng độ của các chất như sau.[H2] = 2,0 mol/lít.[N2]=0,01 mol/lít. [NH3] = 0,4 mol/lít. Hằng số cân bằng ở nhiệt độ đó là?
A. 2.
B. 3
C. 5
D. 7
Xét phản ứng thuận nghịch:
N2 (k) + O2 (k) D 2NO (k)
Hằng số cân bằng ở 2400°C là Kcb = 35.10-4. Biết lúc cân bằng, nồng độ của N2 và O2 lần lượt bằng 5M và 7M trong bình kín có dung tích không đổi. Nồng độ mol/1 của NO lúc cân bằng là giá trị nào trong số các giá trị sau?
A. 0,1225M
B. 0,35M
C. 1,00M
D. Đáp án khác
Xét phản ứng thuận nghịch:
N2 (k) + O2 (k) D 2NO (k)
Hằng số cân bằng ở 2400°C là Kcb = 35.10-4. Biết lúc cân bằng, nồng độ của N2 và O2 lần lượt bằng 5M và 7M trong bình kín có dung tích không đổi. Nồng độ mol/1 của NO lúc cân bằng là giá trị nào trong số các giá trị sau?
A. 0,1225M
B. 0,35M
C. 1,00M
D. Đáp án khác