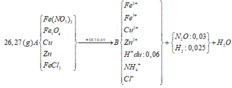
Hỗn hợp rắn A gồm Fe(NO3)2, Fe3O4, Cu, Zn và FeCl2 (trong đó Fe chiếm 19,19% về khối lượng). Cho 26,27 gam A vào dung dịch chứa 0,69 mol HCl. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch B có chứa các muối có khối lượng là 43,395 gam và 1,232 lít (đktc) hỗn hợp khí Z gồm N2O và khí H2. Tỷ khối của Z so với H2 là 137/11. Cho dung dịch AgNO3 dư vào dung dịch B, kết thúc phản ứng thấy thoát ra 0,015 mol khí NO (sản phẩm khử duy nhất); đồng thời thu được 106,375 gam kết tủa. Phần trăm số mol của Cu có trong hỗn hợp A gần nhất với giá trị nào sau đây?
A. 22,5%.
B. 31%.
C. 44,83%.
D. 30,2%.
Tính nhanh được nN2O = 0,03 mol và nH2 = 0,025 mol; nFe = 0,09 mol
Do khi cho dung dịch AgNO3 dư vào B thấy có khí NO thoát ra nên B có chứa HCl dư
nHCl dư = nH+ dư = 4nNO = 0,06 mol (do 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O)
=> nHCl pu với A = 0,69 – 0,06 = 0,63 mol
Ta có: A + HCl → muối + khí + H2O
BTKL => mH2O = mA + mHCl pư với A – m muối – m khí = 26,27 + 0,63.36,5 – 0,03.44 – 0,025.2 = 4,5 (g)
=> nH2O = 0,25 mol
BT “H”: nNH4+ = (nHCl – nH+ dư - 2nH2 – 2nH2O):4 = (0,69-0,06-2.0,025-2.0,25):4 = 0,02 mol
BT “N”: nFe(NO3)2 = (2nN2O + nNH4+):2 = (2.0,03 + 0,02):2 = 0,04 mol
BT “O”: 6nFe(NO3)2 + 4nFe3O4 = nN2O + nH2O => 6.0,04+4nFe3O4 = 0,03+0,25 => nFe3O4 = 0,01 mol
BT “Fe”: nFe = nFe(NO3)2 + 3nFe3O4 + nFeCl2 => 0,09 = 0,04 + 3.0,01 + nFeCl2 => nFeCl2 = 0,02 mol
Khi cho B + AgNO3 dư:

Đáp án B



