Cho từ từ 100ml dung dịch HCl 1,5M vào 0,4 lít dụng dịch X gồm Na2CO3 và KHCO3 thu được 1,008 lít CO2 (đktc) và dung dịch Y. Thêm dụng dịch Ba(OH)2 dư vào dưng dịch Y thu được 29,55 gam kết tủa. Nồng độ mol/lít của Na2CO3 và KHCO3 trong dung dịch X lần lượt là:
A. 0,1125 và 0,225.
B. 0,0375 và 0,05.
C.0,2625 và 0,1225.
D. 0,2625 và 0,225.
+ Tính các giá trị đã biết:
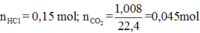
+ Với bài toán tổng hợp như này, thì ta phải viết các phương trình cụ thể cho dễ quan sát:
(1) H+ + CO3- ⟶ HCO3-
(2) H+ + HCO3- ⟶ CO2 +H2O.
Vì thu được khí CO2 nên có xảy ra phản ứng (2) ⇒ CO32- đã phản ứng hết với H+.
+ Từ
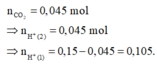
+ Vì khi thêm dung dịch Ba(OH)2 vào dung dịch Y thu được kết tủa nên trong Y phải có muối HCO3-
Như vậy suy ra ngay HCl đã phản ứng hết
Do đó từ (1) và (2) ta suy ra
![]()
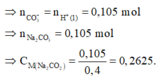
Loại ngay các đáp án A và B.
Việc cần thực hiện bây giờ là đi tính nồng độ của KHCO3 trong dung dịch X:
Vậy dung dịch Y chỉ chứa các ion K+, Na+, HCO3- và Cl-.
+ Khi thêm dịch Ba(OH)2 dư vào dung dịch Y thì:
![]()
Sau đó thì
![]()
+ Do đó 29,55 gam kết tủa là BaCO3:
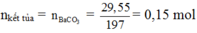
Ta sử dụng Bảo toàn nguyên tố C, toàn bộ C trong dung dịch Y chuyển hóa hết về trong kết tủa (vì thêm dung dịch Ba(OH)2 dư vào):
![]()
+ Lại áp dụng bảo toàn nguyên tốC ta được:
![]()
Hay ![]()
![]()
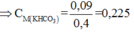
Đáp án D




