Cho m gam bột Fe vào bình kín chứa đồng thời 0,06 mol O2 và 0,03 mol Cl2, rồi đốt nóng. Sau khi các phản ứng xảy ra hoàn toàn chỉ thu được hỗn hợp chất rắn chứa các oxit sắt và muối sắt. Hòa tan hết hỗn hợp này trong một lượng dung dịch HCl ( lấy dư 25% so với lượng cần phản ứng) thu được dung dịch X. Cho dung dịch AgNO3 dư vào X, sau khi kết thúc các phản ứng thì thu được 53,28 gam kết tủa (biết sản phẩm khử của N+5 là khí NO duy nhất). Giá trị của m là
A. 6,72
B. 5,60
C. 5,96
D. 6,44
Đáp án A
Ta có nHCl cần dùng = 2∑nO trong oxit = 0,24 mol → ∑nHCl đã dùng (dư 25%) = 0,3 mol.
* Gộp cả quá trình có sơ đồ:
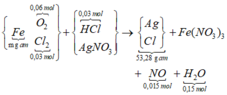
Ghép cụm NO3 bảo toàn O hoặc bảo toàn electron mở rộng ta có:
![]()
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về mặt nguyên tố ∑nAg trong tủa = 0,375 mol.
→ Bảo toàn nguyên tố N có
![]()
Theo đó, m gam Fe ban đầu tương ứng với 0,12 mol → m = 0,12 × 56 = 6,72 gam.



