Cho 56,36 gam hỗn hợp X gồm Mg, Fe(NO3)3, FeCl2, Fe 3 O 4 tác dụng với dung dịch chứa 1,82 mol HCl, thu được dung dịch Y và hỗn hợp khí Z gồm 0,08 mol NO và 0,06 mol N2O. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được 0,045 mol khí NO (sản phẩm khử duy nhất của N+5) và 298,31 gam kết tủa. Nếu cô cạn dung dịch Y thì thu được 97,86 gam muối khan. Phần trăm khối lượng của FeCl2 trong X là
A. 31,55%
B. 27,04%
C. 22,53%
D. 33,80%
Đáp án B
Thêm AgNO3 vào Y → NO chứng tỏ trong Y có chứa cặp H+ và Fe2+ → anion trong Y chỉ có Cl- mà thôi.
Lượng H+ dư được tính nhanh = 4nNO = 0,18 mol → lượng phản ứng là 1,64 mol.
Sơ đồ:
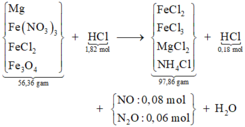
Bảo toàn khối lượng cả sơ đồ có
![]()
Theo đó, bảo toàn nguyên tố H có 0,04 mol NH4Cl và có 0,08 mol Fe(NO3)3 (theo bảo toàn N sau đó).
Tiếp tục theo bảo toàn electron mở rộng hoặc dùng bảo toàn O có ngay số mol Fe3O4 là 0,04 mol.
Gọi số mol Mg và FeCl2 trong X lần lượt là x, y mol → 24x + 127y = 27,72 gam.
Xét toàn bộ quá trình, bảo toàn electron ta có:




