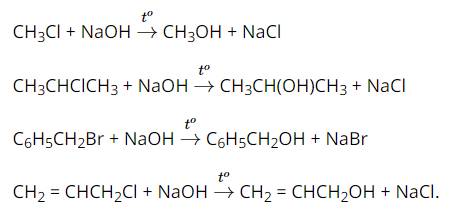C2H5Cl là một dẫn xuất halogen. Dẫn xuất halogen có những tính chất và ứng dụng gì?
Bài 15: Dẫn xuất halogen
Mở đầu (SGK Cánh diều - Trang 100)
Thảo luận (1)
Câu hỏi 1 (SGK Cánh diều - Trang 100)
Có thể tạo được những dẫn xuất halogen nào từ các hydrocarbon sau: CH4, CH3 – CH3, CH2 = CH2 và C6H6?
Thảo luận (1)Hướng dẫn giảiCH4 : CH3Cl, CH2Cl2, CHCl3, CCl4, CHBr3, CHI3, ...
(Trả lời bởi Nguyễn Việt Dũng)
CH3 – CH3 : CH3CH2Cl, CH2BrCH2Br, ...
CH2 = CH2 :CH2=CHCl, CF2=CF2, ...
C6H6 :C6H5Br, C6H5Cl, ...
Câu hỏi 2 (SGK Cánh diều - Trang 101)
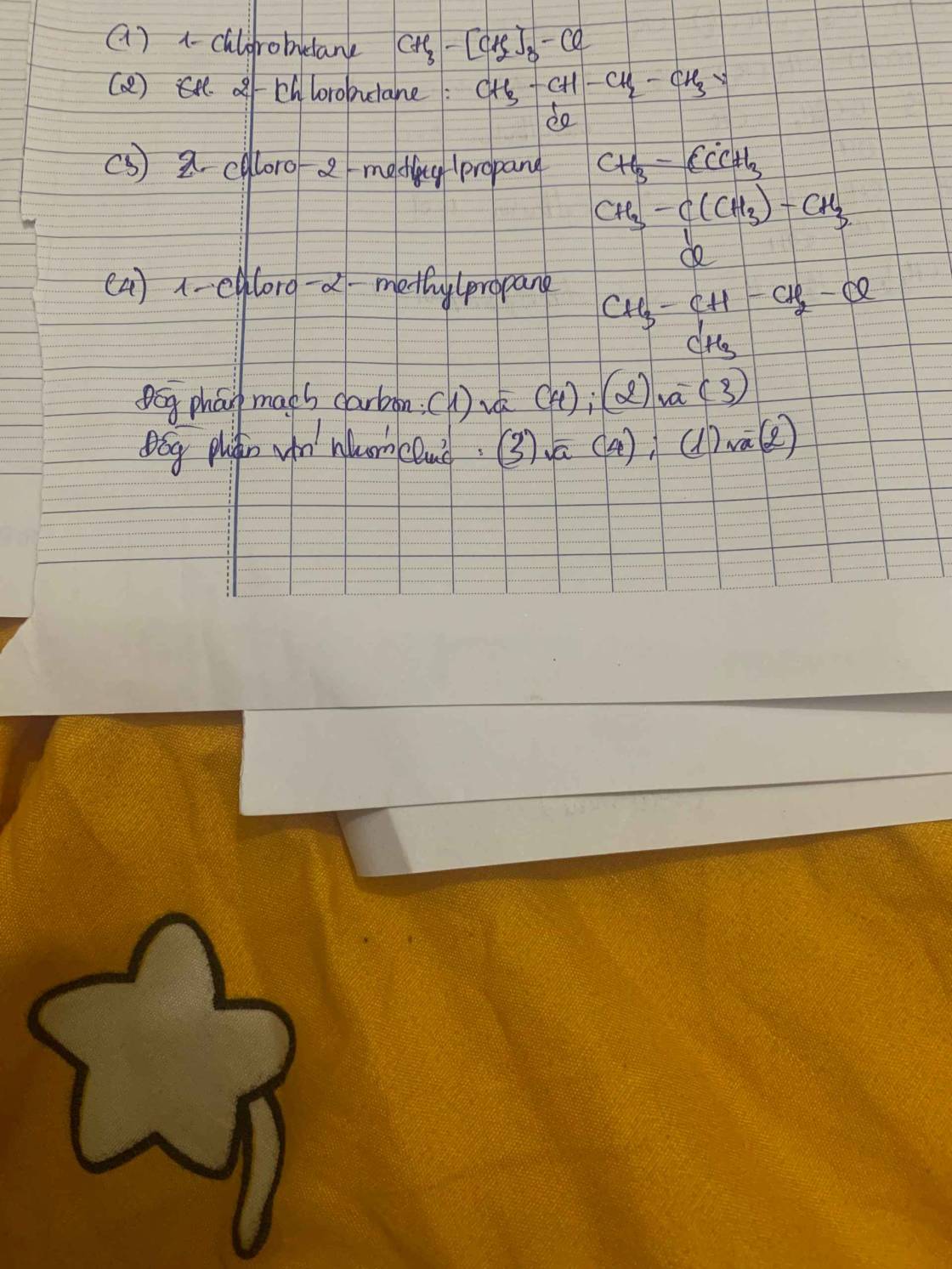
Trong các đồng phân cấu tạo có cùng công thức phân tử là C4H9Cl, hãy chỉ ra đồng phân mạch carbon, đồng phân vị trí nhóm chức.
Thảo luận (2)Hướng dẫn giải
Luyện tập 1 (SGK Cánh diều - Trang 102)
Viết công thức cấu tạo và gọi tên thay thế của các hợp chất có cùng công thức phân tử là C5H11Cl.
Thảo luận (2)Hướng dẫn giải
Luyện tập 2 (SGK Cánh diều - Trang 102)
Cho các chất có công thức: CH3F, CH3Cl, CH3Br, CH3I và nhiệt độ sôi của chúng (không theo thứ tự) là 42 oC, 4 oC, -24 oC và -78 oC. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.
Thảo luận (1)Hướng dẫn giảiTheo nguyên tử khối của Halogen, ta sẽ có: \(M_F< M_{Cl}< M_{Br}< M_I\)
Do đó: Nhiệt độ sôi tương ứng của chúng sẽ tăng dần
=> Nhiệt độ sôi của CH3F, CH3Cl, CH3Br, CH3I lần lượt là -78 độ C, -24 độ C, 4 độ C và 24 độ C
(Trả lời bởi Nguyễn Lê Phước Thịnh)
Câu hỏi 3 (SGK Cánh diều - Trang 102)
Dựa vào giá trị độ âm điện của carbon, hydrogen và chlorine, nhận xét về sự phân cực của các liên kết C – C, C – H và C – Cl.
Thảo luận (1)Hướng dẫn giải
Liên kết
C – C
C – H
C – Cl
Hiệu độ âm điện
0
0,35
0,96
Nhận xét: độ phân cực của liên kết tăng dần theo thứ tự: C – C, C – H, C – Cl.
(Trả lời bởi Quoc Tran Anh Le)
Luyện tập 3 (SGK Cánh diều - Trang 103)
Viết phương trình hoá học của phản ứng xảy ra khi đun các hợp chất sau với dung dịch sodium hydroxide: CH3Cl, CH3CHClCH3, C6H5CH2Br và CH2 = CHCH2Cl.
Thảo luận (1)Hướng dẫn giải
Câu hỏi 4 (SGK Cánh diều - Trang 103)
Trong thí nghiệm Thuỷ phân dẫn xuất halogen, cho biết:
a) Cho nước vào ống nghiệm chứa dẫn xuất halogen sau đó thử phần nước bằng dung dịch silver nitrate nhằm mục đích gì?
b) Vì sao phải acid hoá dung dịch sau khi thuỷ phân bằng dung dịch HNO3? Có thể thay dung dịch HNO3 bằng dung dịch H2SO4, hay HCl được không? Vì sao?
Thảo luận (1)Hướng dẫn giảia) Mục đích: Nhận biết ion Cl− trong dung dịch.
(Trả lời bởi Nguyễn Việt Dũng)
b) Acid hóa dung dịch sau khi thuỷ phân bằng dung dịch HNO3 để trung hòa NaOH dư.
Không thể thay dung dịch HNO3 bằng dung dịch H2SO4 hay HCI được vì khi cho dung dịch AgNO3 vào Ag+ sẽ kết hợp với SO42− và Cl− tạo kết tủa.
Luyện tập 4 (SGK Cánh diều - Trang 103)
Viết phương trình hoá học của phản ứng xảy ra khi đun các dẫn xuất halogen sau với dung dịch potassium hydroxide trong ethanol.
a) 2-chloropropane
b) 2-bromo-2-methylbutaneGọi tên các sản phẩm sinh ra.
Thảo luận (2)Hướng dẫn giảiTham khảo:
(Trả lời bởi Nguyễn Việt Dũng)
a) CH3-CH(Cl)-CH3 + KOH (C2H5OH) → CH3-CH=CH2 + KCl + H2O
b)
+ KBr + H2O
(sản phẩm chính)
CH2=C(CH3)-CH2-CH3
( sản phẩm phụ)
Câu hỏi 5 (SGK Cánh diều - Trang 104)
Trình bày một số ứng dụng trong thực tiễn của dẫn xuất halogen.
Thảo luận (1)Hướng dẫn giảiDùng làm ống dẫn, vỏ bọc dây điện, vải giả da,... để sản xuất cao su cloropren.
(Trả lời bởi Nguyễn Việt Dũng)