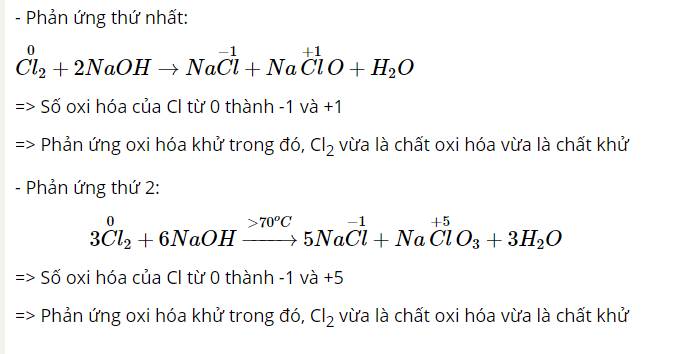Từ cấu tạo phân tử halogen và đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, nhận xét xu hướng hình thành liên kết của nguyên tử halogen trong các phản ứng hóa học.
Bài 17: Tính chất vật lý và hoá học các đơn chất nhóm VIIA
Câu hỏi 8 (SGK Chân trời sáng tạo trang 109)
Thảo luận (1)
Câu hỏi 9 (SGK Chân trời sáng tạo trang 109)
Trong phản ứng với kim loại, nhận xét sự biến đổi số oxi hóa của nguyên tử các nguyên tố halogen và viết các quá trình khử xảy ra.
Thảo luận (1)Hướng dẫn giải- Trong phản ứng với kim loại, các halogen từ số oxi hóa 0 sẽ nhận thêm 1 electron thành số oxi hóa -1
- Sơ đồ:
F + 1e → F-
Cl + 1e → Cl-
Br + 1e → Br-
I + 1e → I-
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 10 (SGK Chân trời sáng tạo trang 110)
Dựa vào điều kiện phản ứng với hydrogen và giá trị năng lượng liên kết của phân tử H – X, giải thích khả năng phản ứng của các halogen với hydrogen.
Thảo luận (1)Hướng dẫn giải- Đi từ F đến I
+ Điều kiện phản ứng với hydrogen khó dần
+ Năng lượng liên kết H-X giảm dần => Độ bền H-X giảm dần
=> Khả năng phản ứng của các halogen với hydrogen giảm dần
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 11 (SGK Chân trời sáng tạo trang 110)
Trong phản ứng với dung dịch kiềm, nhận xét sự biến đổi số oxi hóa của chlorine và cho biết phản ứng này thuộc loại phản ứng gì?
Thảo luận (1)Hướng dẫn giải
Câu hỏi 12 (SGK Chân trời sáng tạo trang 111)
Tiến hành thí nghiệm 1, quan sát và ghi nhận hiện tượng.Thí nghiệm 1: So sánh tính chất hóa học của halogenHóa chất: dung dịch NaBr, NaI, nước chlorine, nước bromine và dung dịch hồ tinh bột.Dụng cụ: ống nghiệm, ống hút nhỏ giọt, kẹp gỗ, giá để ống nghiệm.Tiến hành: Thực hiện các bước theo Bảng 17.3
Đọc tiếp
Tiến hành thí nghiệm 1, quan sát và ghi nhận hiện tượng.
Thí nghiệm 1: So sánh tính chất hóa học của halogen
Hóa chất: dung dịch NaBr, NaI, nước chlorine, nước bromine và dung dịch hồ tinh bột.
Dụng cụ: ống nghiệm, ống hút nhỏ giọt, kẹp gỗ, giá để ống nghiệm.
Tiến hành: Thực hiện các bước theo Bảng 17.3
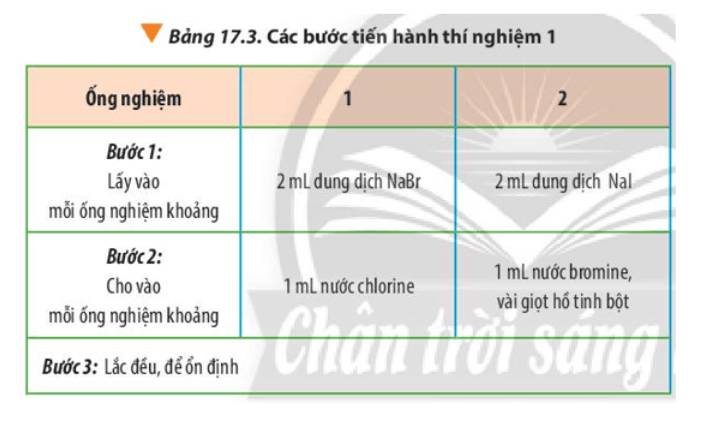
Thảo luận (1)Hướng dẫn giải- Ống nghiệm 1: dung dịch không màu chuyển thành màu vàng nhạt
- Ống nghiệm 2: dung dịch không màu chuyển thành vàng, khi cho hồ tinh bột (không màu) thì dung dịch chuyển màu xanh tím
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 13 (SGK Chân trời sáng tạo trang 111)
Dựa vào phương trình hóa học của các phản ứng, giải thích kết quả thí nghiệm 1.
Thảo luận (1)Hướng dẫn giải- Giải thích kết quả:
+ Ống nghiệm 1: dung dịch không màu chuyển thành màu vàng nhạt của Br2
Cl2 + 2NaBr → 2NaCl + Br2
+ Ống nghiệm 2: dung dịch không màu chuyển thành vàng của I2, khi cho hồ tinh bột (không màu) thì dung dịch chuyển màu xanh tím do I2 làm đổi màu hồ tinh bột
Br2 + 2NaI → 2NaBr + I2
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 14 (SGK Chân trời sáng tạo trang 111)
Tiến hành thí nghiệm 2, quan sát và ghi nhận hiện tượng.Thí nghiệm 2: Tính tẩy màu của khí chlorine ẩmHóa chất: tinh thể potassium permanganate (KMnO4), dung dịch HCl đặc, giấy màu, nước cất.Dụng cụ: ống nghiệm 2 nhánh, nút cao su, giá đỡ, thìa thủy tinh, ống hút nhỏ giọt.Tiến hành:Bước 1: Dùng thìa thủy tinh lấy một ít tinh thể KMnO4, cho vào nhánh dài của ống nghiệm. Dùng ống hút nhỏ giọt lấy khoảng 1 mL dung dịch HCl đặc cho vào nhánh ngắn của ống nghiệm. Lắp dụng cụ để điều chế khí Cl2 ẩm nh...
Đọc tiếp
Tiến hành thí nghiệm 2, quan sát và ghi nhận hiện tượng.
Thí nghiệm 2: Tính tẩy màu của khí chlorine ẩm
Hóa chất: tinh thể potassium permanganate (KMnO4), dung dịch HCl đặc, giấy màu, nước cất.
Dụng cụ: ống nghiệm 2 nhánh, nút cao su, giá đỡ, thìa thủy tinh, ống hút nhỏ giọt.
Tiến hành:
Bước 1: Dùng thìa thủy tinh lấy một ít tinh thể KMnO4, cho vào nhánh dài của ống nghiệm. Dùng ống hút nhỏ giọt lấy khoảng 1 mL dung dịch HCl đặc cho vào nhánh ngắn của ống nghiệm. Lắp dụng cụ để điều chế khí Cl2 ẩm như Hình 17.4.
Lưu ý: Kiểm tra nút cao su phải được đậy kín trước khi thực hiện bước 2.
Bước 2: Nghiêng ống nghiệm sao cho dung dịch HCl tiếp xúc với KMnO4.
Phương trình hóa học của phản ứng điều chế khí Cl2:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O

Thảo luận (1)Hướng dẫn giải
Câu hỏi 15 (SGK Chân trời sáng tạo trang 112)
Dựa vào phương trình hóa học của các phản ứng, giải thích kết quả thí nghiệm 2.
Thảo luận (1)Hướng dẫn giải\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\)
Khí clobay lên, tác dụng với nước tạo tạo thành hợp chất hỗn hợp có tính tẩy màu
\(Cl_2+H_2O\rightarrow HClO+HCl\)
=>kết quả là Giấy màu ẩm bị nhạt màu dần sau đó mất màu
(Trả lời bởi Nguyễn Lê Phước Thịnh)
Luyện tập (SGK Chân trời sáng tạo trang 112)
Viết phương trình hóa học của các phản ứng sau:Cu + Cl2 → (1)Al + Br2 → (2)Ca(OH)2 + Cl2 → (3)KOH + Br2 underrightarrow{70^oC} (4)Cl2 + KBr → (5)Br2 + NaI → (6)
Đọc tiếp
Viết phương trình hóa học của các phản ứng sau:
Cu + Cl2 → (1)
Al + Br2 → (2)
Ca(OH)2 + Cl2 → (3)
KOH + Br2 \(\underrightarrow{70^oC}\) (4)
Cl2 + KBr → (5)
Br2 + NaI → (6)
Thảo luận (1)Hướng dẫn giải(1) \(Cu+Cl_2\xrightarrow[]{t^\circ}CuCl_2\)
(2) \(2Al+3Br_2\xrightarrow[]{t^\circ}2AlBr_3\)
(3) \(Ca\left(OH\right)_2+Cl_2\rightarrow CaOCl_2+H_2O\)
(4) \(6KOH+3Br_2\xrightarrow[]{70^\circ C}KBrO_3+5KBr+3H_2O\)
(5) \(Cl_2+2KBr\xrightarrow[]{}2KCl+Br_2\)
(6) \(Br_2+2NaI\rightarrow2NaBr+I_2\)
(Trả lời bởi Phước Lộc)
Vận dụng (SGK Chân trời sáng tạo trang 112)
Tính tẩy màu của khí chlorine ẩm được ứng dụng vào lĩnh vực nào trong đời sống?
Thảo luận (3)Hướng dẫn giảiTrả lời:
Tính tẩy màu của khí chlorine ẩm được ứng dụng:
+ Tẩy trắng sợi, vải, giấy.
+ Sản xuất chất tẩy rửa.
+ Tiệt trùng nước sinh hoạt, nước trong các bể bơi.
(Trả lời bởi Toru)