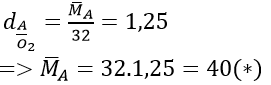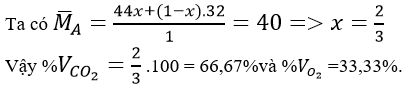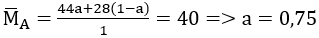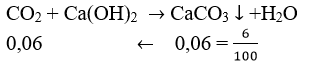Sửa đề : tỉ khối là 1.25
a)Ta có:
Phương trình phản ứng:
C + O2 -> CO2 (1)
C + CO2 -> 2CO (2)
Bài toán này có thể xảy ra hai trường hợp sau:
Trường hợp 1: Oxi dư (không có phản ứng 2): Hỗn hợp A gồm CO2 và O2 dư.
Thành phần phần trăm các chất trong hỗn hợp về mặt toán học không ảnh hưởng đến số mol hỗn hợp.
Xét 1 mol hỗn hợp A, trong đó X là số mol của CO2 và (1 - x) là số mol của O2 dư.
Vậy: %VCO2 = 2/3. 100% = 66,67% và %VO2 = 33,33%.
Trường hợp 2: O2 thiếu (có phản ứng 2), hỗn hợp A có CO2 và CO.
Tương tự trên, xét 1 mol hỗn hợp A, trong đó a là số mol của CO2 và (1 - a) là số moi của CO
Vậy %VCO2 = 0,75. 100% = 75%; %VCO = 100% - 75% = 25%.
b)
Trường hợp 1: nCO2 = 0,06 mol ⇒ nO2 dư = 1/2 nCO2 = 0,03 (mol)
Vậy: mC = 0,06.12 = 0,72 gam; VO2 = (0,06 + 0,03).22,4 = 2,016 (lít).
Trường hợp 2: nCO2 = 0,06mol; nCO = nCO2/3 = 0,02(mol)
BT nguyên tố C ⇒ nC = nCO2 +nCO = 0,06 + 0,02 = 0,08 mol ⇒ mC = 0,08.12 = 0,96(g)
BT nguyên tố O ⇒ nO2 = nCO2 + 1/2. nCO = 0,06 + 0,01 = 0,07 mol ⇒ VO2 = 0,07.22,4 = 1,568 (lít).