Phản ứng hóa học là quá trình biến đổi các chất đầu thành sản phẩm. Tuy nhiên có nhiều phản ứng, các chất sản phẩm sinh ra lại có thể phản ứng với nhau tạo thành chất đầu. Đối với những phản ứng này, làm thế nào để thu được nhiều sản phẩm hơn và làm tăng hiệu suất phản ứng?
Bài 1: Khái niệm về cân bằng hóa học
Mở đầu (SGK Kết nối tri thức và cuộc sống trang 6)
Thảo luận (1)
Hoạt động (SGK Kết nối tri thức và cuộc sống trang 6)
Hai thí nghiệm sau đều được thực hiện ở cùng một điều kiện (bình kín dung tích 10 L, nhiệt độ 445 oC):
Thực hiện yêu cầu sau:
a) Viết phương trình hoá học của các phản ứng xảy ra trong thí nghiệm 1 và thí nghiệm 2.
b) Trong cả hai thí nghiệm trên, dù thời gian phản ứng kéo dài bao lâu thì các chất đầu đều còn lại sau phản ứng. Giải thích.
Thảo luận (1)Hướng dẫn giảia) Phương trình hoá học của các phản ứng xảy ra:
- Trong thí nghiệm 1: H2(g) + I2(g) ⇌ 2HI(g).
- Trong thí nghiệm 2: 2HI(g) ⇌ H2(g) + I2(g).
b) Trong cả hai thí nghiệm trên, dù thời gian phản ứng kéo dài bao lâu thì các chất đầu đều còn lại sau phản ứng. Do hai phản ứng trên là phản ứng thuận nghịch, trong cùng một điều kiện, các chất phản ứng tác dụng với nhau tạo thành các chất sản phẩm (phản ứng thuận), đồng thời các chất sản phẩm lại tác dụng với nhau tạo thành các chất ban đầu (phản ứng nghịch).
(Trả lời bởi Quoc Tran Anh Le)
Câu hỏi 1 (SGK Kết nối tri thức và cuộc sống trang 7)
Quá trình hình thành hang động, thạch nhũ là một ví dụ điển hình về phản ứng thuận nghịch trong tự nhiên.Nước có chức CO2 chảy qua đá vôi, bào mòn đá tạo thành Ca(HCO3)2 (phản ứng thuận) góp phần hình thành các hang động. Hợp chất Ca(HCO3)2 trong nước lại bị phân hủy tạo ra CO2 và CaCO3 (phản ứng nghịch), hình thành các thạch nhũ, măng đá, cột đá.Viết phương trình hóa học của các phản ứng xảy ra trong hai quá trình trên.
Đọc tiếp
Quá trình hình thành hang động, thạch nhũ là một ví dụ điển hình về phản ứng thuận nghịch trong tự nhiên.
Nước có chức CO2 chảy qua đá vôi, bào mòn đá tạo thành Ca(HCO3)2 (phản ứng thuận) góp phần hình thành các hang động. Hợp chất Ca(HCO3)2 trong nước lại bị phân hủy tạo ra CO2 và CaCO3 (phản ứng nghịch), hình thành các thạch nhũ, măng đá, cột đá.
Viết phương trình hóa học của các phản ứng xảy ra trong hai quá trình trên.
Thảo luận (1)Hướng dẫn giải1. Phản ứng thuận: CaCO3 + H2CO3 → Ca(HCO3)2
Phản ứng nghịch: Ca(HCO3)2 → CO2 + H2O + CaCO3
(Trả lời bởi Quoc Tran Anh Le)
Câu hỏi 2+3 (SGK Kết nối tri thức và cuộc sống trang 8)
2. Phản ứng xảy ra khi cho khí Cl2 tác dụng với nước là một phản ứng thuận nghịch. Viết phương trình hóa học của phản ứng, xác định phản ứng thuận, phản ứng nghịch.3. Nhận xét nào sau đây không đúng?A. Trong phản ứng một chiều, chất sản phẩm không phản ứng được với nhau tạo thành chất đầu.B. Trong phản ứng thuận nghịch, các chất sản phẩm có thể phản ứng với nhau để tạo thành chất đầu.C. Phản ứng một chiều là phản ứng luôn xảy ra không hoàn toàn.D. Phản ứng thuận nghịch là phản ứng xảy ra theo ha...
Đọc tiếp
2. Phản ứng xảy ra khi cho khí Cl2 tác dụng với nước là một phản ứng thuận nghịch. Viết phương trình hóa học của phản ứng, xác định phản ứng thuận, phản ứng nghịch.
3. Nhận xét nào sau đây không đúng?
A. Trong phản ứng một chiều, chất sản phẩm không phản ứng được với nhau tạo thành chất đầu.
B. Trong phản ứng thuận nghịch, các chất sản phẩm có thể phản ứng với nhau để tạo thành chất đầu.
C. Phản ứng một chiều là phản ứng luôn xảy ra không hoàn toàn.
D. Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều trái ngược nhau trong cùng điều kiện.
Thảo luận (1)Hướng dẫn giải2. Phương trình hoá học của phản ứng xảy ra khi cho khí Cl2 tác dụng với nước:
Cl2(aq) + H2O(l) ⇌ HCl(aq) + HClO(aq)
Phản ứng thuận: Cl2 + H2O → HCl + HClO
Phản ứng nghịch: HCl + HClO → Cl2 + H2O
3. Đáp án C. vì phản ứng một chiều là phản ứng chỉ xảy ra một chiều, không có sự tạo lại chất ban đầu, nên phản ứng một chiều có thể xảy ra hoàn toàn hoặc không hoàn toàn. Ví dụ như phản ứng cháy là một phản ứng một chiều, có thể xảy ra hoàn toàn hoặc không hoàn toàn, tùy thuộc vào điều kiện phản ứng.
(Trả lời bởi Quoc Tran Anh Le)
Hoạt động (SGK Kết nối tri thức và cuộc sống trang 8)
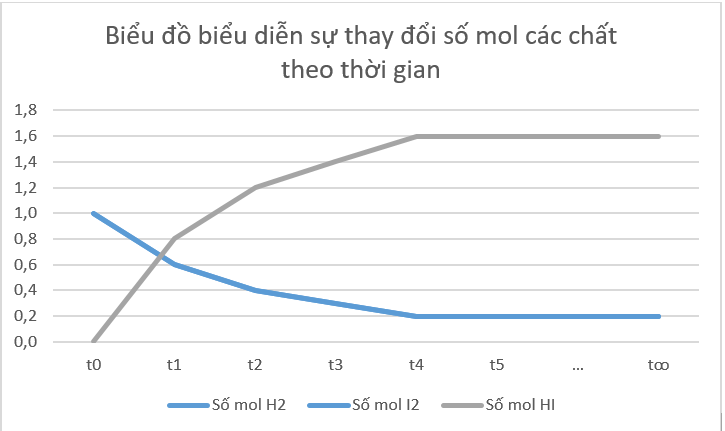
Câu hỏi: Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g).Số liệu về sự thay đổi số mol các chất trong bình phản ứng ở thí nghiệm 1 được trình bày trong Bảng 1.1 dưới đây:a) Vẽ đồ thị biểu diễn sự thay đổi số mol các chất theo thời gian.b) Từ đồ thị, nhận xét về sự thay đổi số mol của các chất theo thời gian.c) Viết biểu thức định luật tác dụng khối lượng đối với phản ứng thuận và phản ứng nghịch, từ đó dự đoán sự thay đổi tốc độ của mỗi phản ứng theo thời gian (biết các phản ứng này đều là phả...
Đọc tiếp
Câu hỏi: Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g).
Số liệu về sự thay đổi số mol các chất trong bình phản ứng ở thí nghiệm 1 được trình bày trong Bảng 1.1 dưới đây:
a) Vẽ đồ thị biểu diễn sự thay đổi số mol các chất theo thời gian.
b) Từ đồ thị, nhận xét về sự thay đổi số mol của các chất theo thời gian.
c) Viết biểu thức định luật tác dụng khối lượng đối với phản ứng thuận và phản ứng nghịch, từ đó dự đoán sự thay đổi tốc độ của mỗi phản ứng theo thời gian (biết các phản ứng này đều là phản ứng đơn giản).
d) Bắt đầu từ thời điểm nào thì số mol các chất trong hệ phản ứng không thay đổi nữa?
Thảo luận (2)Hướng dẫn giải
Câu hỏi 4+5 (SGK Kết nối tri thức và cuộc sống trang 9)
4. Cho phản ứng: 2HI (g) ⇌ H2 (g) + l2(g) a) Vẽ dạng đồ thị biểu diễn tốc độ của phản ứng thuận và phản ứng nghịch theo thời gian. b) Xác định trên đồ thị thời điềm phản ứng trên bắt đầu đạt đến trạng thái cân bằng.5. Cho các nhận xét sau: a) ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.b) ở trạng thái cân bằng, các chất không phản ửng với nhau.c) ở trạng thái cân bằng, nồng độ các chất sản phẩm luôn lớn hơn nồng độ các chất đầu.d) ở trạng thái cân bằng, nồng độ các c...
Đọc tiếp
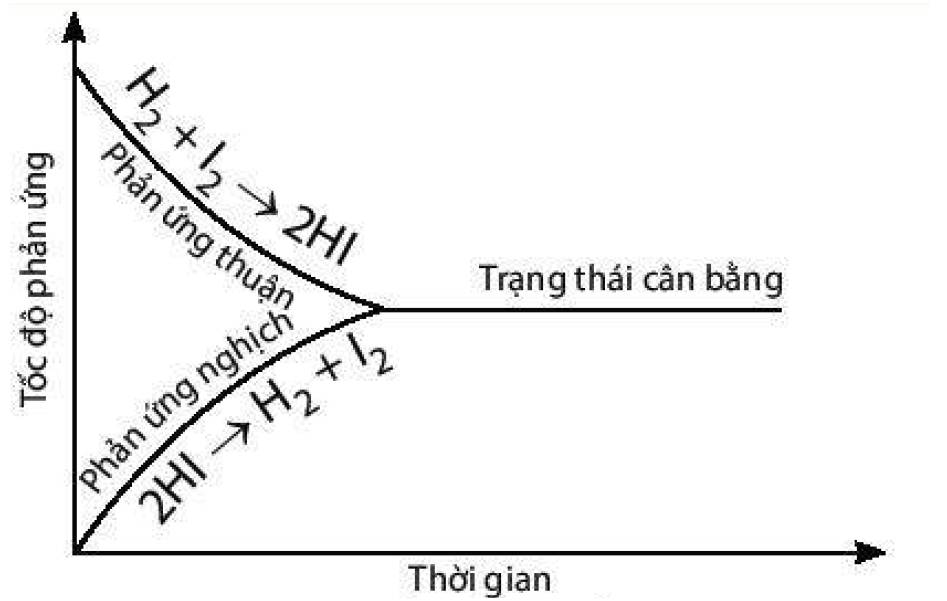
4. Cho phản ứng: 2HI (g) ⇌ H2 (g) + l2(g)
a) Vẽ dạng đồ thị biểu diễn tốc độ của phản ứng thuận và phản ứng nghịch theo thời gian.
b) Xác định trên đồ thị thời điềm phản ứng trên bắt đầu đạt đến trạng thái cân bằng.
5. Cho các nhận xét sau:
a) ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
b) ở trạng thái cân bằng, các chất không phản ửng với nhau.
c) ở trạng thái cân bằng, nồng độ các chất sản phẩm luôn lớn hơn nồng độ các chất đầu.
d) ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Các nhận xét đúng là:
A. (a) và (b).
B. (b) và (c).
C. (a) và (c).
D. (a) và (d).
Thảo luận (2)Hướng dẫn giải4.
a) Đồ thị biểu diễn tốc độ của phản ứng thuận và phản ứng nghịch theo thời gian:
b) Thời điểm phản ứng trên bắt đầu đạt trạng thái cân bằng là thời điểm tốc độ phản ứng thuận bắt đầu bằng tốc độ phản ứng nghịch.
(Trả lời bởi Quoc Tran Anh Le)
Hoạt động (SGK Kết nối tri thức và cuộc sống trang 9)
Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g)
Thực hiện phản ứng trên ở trong bình kín, ở nhiệt độ 445 oC với các nồng độ ban đầu khác nhau. Số liệu về nồng độ các chất ở thời điểm ban đầu và trạng thái cân bằng trong các thí nghiệm được trình bày trong Bảng 1.2.
Thảo luận (1)Hướng dẫn giảiGiá trị hằng số cân bằng ở mỗi thí nghiệm:
- Thí nghiệm 1: \({{\rm{K}}_{\rm{C}}} = \frac{{{{\left( {{\rm{HI}}} \right)}^2}}}{{\left( {{{\rm{H}}_{\rm{2}}}} \right)\left( {{{\rm{I}}_{\rm{2}}}} \right)}} = \frac{{{{0,16}^2}}}{{0,02.0,02}} = 64\)
- Thí nghiệm 2: \({{\rm{K}}_{\rm{C}}} = \frac{{{{\left( {{\rm{HI}}} \right)}^2}}}{{\left( {{{\rm{H}}_{\rm{2}}}} \right)\left( {{{\rm{I}}_{\rm{2}}}} \right)}} = \frac{{{{0,18936}^2}}}{{0,00532.0,10532}} \approx 64\)
- Thí nghiệm 3: \({{\rm{K}}_{\rm{C}}} = \frac{{{{\left( {{\rm{HI}}} \right)}^2}}}{{\left( {{{\rm{H}}_{\rm{2}}}} \right)\left( {{{\rm{I}}_{\rm{2}}}} \right)}} = \frac{{{{0,19420}^2}}}{{0,20290.0,00290}} \approx 64\)
Nhận xét: Hằng số cân bằng KC của một phản ứng thuận nghịch chỉ phụ thuộc vào nhiệt độ và bản chất của phản ứng.
(Trả lời bởi Quoc Tran Anh Le)
Câu hỏi 6+7 (SGK Kết nối tri thức và cuộc sống trang 10)
6. Viết biểu thức hằng số cân bằng cho các phản ứng sau:a) Phản ứng tồng hợp ammonia: N2(g) + 3H2(g) ⇌ 2NH3(g)b) Phản ứng nung vôi: CaCO3(s) ⇌ CaO(s) + CO2(g)7. Ammonia (NH3) được điều chế bằng phản ứng: N2(g) + 3H2(g) ⇌ 2NH3(g) ở t °C, nồng độ các chất ở trạng thái cân bằng là: (N2) 0,45 M; (H2) 0,14 M; (NH3) 0,62 M.Tính hằng số cân bằng KC của phản ứng trên tại t °C.
Đọc tiếp
6. Viết biểu thức hằng số cân bằng cho các phản ứng sau:
a) Phản ứng tồng hợp ammonia: N2(g) + 3H2(g) ⇌ 2NH3(g)
b) Phản ứng nung vôi: CaCO3(s) ⇌ CaO(s) + CO2(g)
7. Ammonia (NH3) được điều chế bằng phản ứng: N2(g) + 3H2(g) ⇌ 2NH3(g) ở t °C, nồng độ các chất ở trạng thái cân bằng là: (N2) = 0,45 M; (H2) = 0,14 M; (NH3) = 0,62 M.
Tính hằng số cân bằng KC của phản ứng trên tại t °C.
Thảo luận (1)Hướng dẫn giải\(6.\\a.K_C=\dfrac{\left[NH_3\right]^2}{\left[N_2\right]\left[H_2\right]^3}\\ b.K_C=\left[CO_2\right]\\ 7.\\ K_C =\dfrac{\left[NH_3\right]^2}{\left[N_2\right]\left[H_2\right]^3}=\dfrac{0,62^2}{0,45\cdot0,14^3}=311,30\)
(Trả lời bởi Khai Hoan Nguyen)
Thí nghiệm 1 (SGK Kết nối tri thức và cuộc sống trang 10)
Ảnh hưởng của nhiệt độ đến sự chuyển dịch cân bằng:
2NO2(g) ⇌ N2O4(g) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{o}}{\rm{ < 0}}\)
(màu nâu đỏ) (không màu)
Thảo luận (1)Hướng dẫn giải(Trả lời bởi Quoc Tran Anh Le)
Tác động
Hiện tượng
Chiều chuyển dịch cân bằng
(thuận/ nghịch)
Chiều chuyển dịch cân bằng
(toả nhiệt/ thu nhiệt)
Tăng nhiệt độ
Màu khí trong ống nghiệm đậm dần lên
Nghịch
Thu nhiệt
Giảm nhiệt độ
Màu khí trong ống nghiệm nhạt dần đi
Thuận
Toả nhiệt
Thí nghiệm 2 (SGK Kết nối tri thức và cuộc sống trang 11)
CH3COONa + H2O ⇌CH3COOH + NaOH \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{o}}{\rm{ > 0}}\)
Thảo luận (1)Hướng dẫn giải
Tác động
Hiện tượng
Chiều chuyển dịch cân bằng
(thuận/ nghịch)
Chiều chuyển dịch cân bằng
(toả nhiệt/ thu nhiệt)
Tăng nhiệt độ
Màu dung dịch trong ống nghiệm đậm dần lên
Thuận
Thu nhiệt
Giảm nhiệt độ
Màu dung dịch trong ống nghiệm nhạt dần đi
Nghịch
Toả nhiệt
Ảnh hưởng của nhiệt độ đến sự chuyển dịch cân bằng:
CH3COONa + H2O ⇌CH3COOH + NaOH \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{o}}{\rm{ > 0}}\)
(Trả lời bởi Quoc Tran Anh Le)