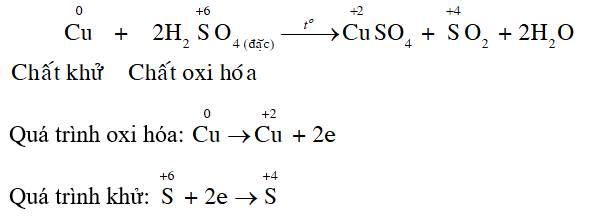Bài 7. Sulfuric acid và muối sulfate
Các câu hỏi tương tự
Viết phương trình hoá học khi cho dung dịch H2SO4 đặc tác dụng với KBr, C. Cho biết sản phẩm khử duy nhất là SO2.
Thí nghiệm 1. Phản ứng của dung dịch H2SO4 đặc, nóng với CuDụng cụ: ống nghiệm, kẹp ống nghiệm, đèn cồn.Hoá chất: dung dịch H2SO4 đặc, dung dịch NaOH, mảnh đồng, bông.Tiến hành: Cho khoảng 2 mL dung dịch H2SO4 đặc vào ống nghiệm. Cho một mảnh đồng vào ống nghiệm, đun nóng nhẹ trên ngọn lửa đèn cồn. Dùng bông tẩm dung dịch NaOH đậy trên miệng ống nghiệm.Quan sát và mô tả hiện tượng xảy ra.
Đọc tiếp
Thí nghiệm 1. Phản ứng của dung dịch H2SO4 đặc, nóng với Cu
Dụng cụ: ống nghiệm, kẹp ống nghiệm, đèn cồn.
Hoá chất: dung dịch H2SO4 đặc, dung dịch NaOH, mảnh đồng, bông.
Tiến hành: Cho khoảng 2 mL dung dịch H2SO4 đặc vào ống nghiệm. Cho một mảnh đồng vào ống nghiệm, đun nóng nhẹ trên ngọn lửa đèn cồn. Dùng bông tẩm dung dịch NaOH đậy trên miệng ống nghiệm.
Quan sát và mô tả hiện tượng xảy ra.
Thí nghiệm 2. Phản ứng của dung dịch H2SO4 đặc với đường
Dụng cụ: cốc thuỷ tinh.
Hoá chất: dung dịch H2SO4đặc, đường tinh luyện.
Tiến hành: Cho một thìa nhỏ đường vào cốc thuỷ tinh. Nhỏ vài giọt dung dịch H2SO4 đặc vào cốc.
Quan sát và mô tả hiện tượng xảy ra.
Tính chất nào sau đây không phải tính chất của dung dịch sulfuric acid đặc?
A. Tính háo nước. B. Tính oxi hoá. C. Tính acid. D. Tính khử.
Hãy giải thích vì sao ở giai đoạn tạo ra SO3 người ta chọn điều kiện phản ứng ở nhiệt độ cao (450 °C - 500 °C).
Cho các dung dịch không màu của mỗi chất sau: K2CO3, Na2SO4, Ba(NO3)2. Hãy trình bày cách phân biệt các dung dịch đã cho bằng phương pháp hoá học. Viết phương trình hoá học của các phản ứng xảy ra.
Có 4 mẫu sau: dung dịch NaOH, dung dịch HCl, dung dịch H2SO4 và H2O được kí hiệu bằng các chữ cái: A, B, C và D (không theo trình tự trên). Kết quả của những thí nghiệm nhận biết những mẫu này được ghi trong bảng sau:MẫuThuốc thửQuỳ tímDung dịch BaCl2AĐỏKết tủa trắngBXanhKhông kết tủaCTímKhông kết tủaDĐỏKhông kết tủaHãy cho biết A, B, C và D là kí hiệu của những chất nào. Giải thích và viết phương trình hóa học của các phản ứng xảy ra.
Đọc tiếp
Có 4 mẫu sau: dung dịch NaOH, dung dịch HCl, dung dịch H2SO4 và H2O được kí hiệu bằng các chữ cái: A, B, C và D (không theo trình tự trên). Kết quả của những thí nghiệm nhận biết những mẫu này được ghi trong bảng sau:
Mẫu | Thuốc thử | |
Quỳ tím | Dung dịch BaCl2 | |
A | Đỏ | Kết tủa trắng |
B | Xanh | Không kết tủa |
C | Tím | Không kết tủa |
D | Đỏ | Không kết tủa |
Hãy cho biết A, B, C và D là kí hiệu của những chất nào. Giải thích và viết phương trình hóa học của các phản ứng xảy ra.
Nếu ứng dụng trong đời sống, sản xuất của một số muối sulfate mà em biết.
Giải thích hiện tượng xảy ra trong Thí nghiệm 2.