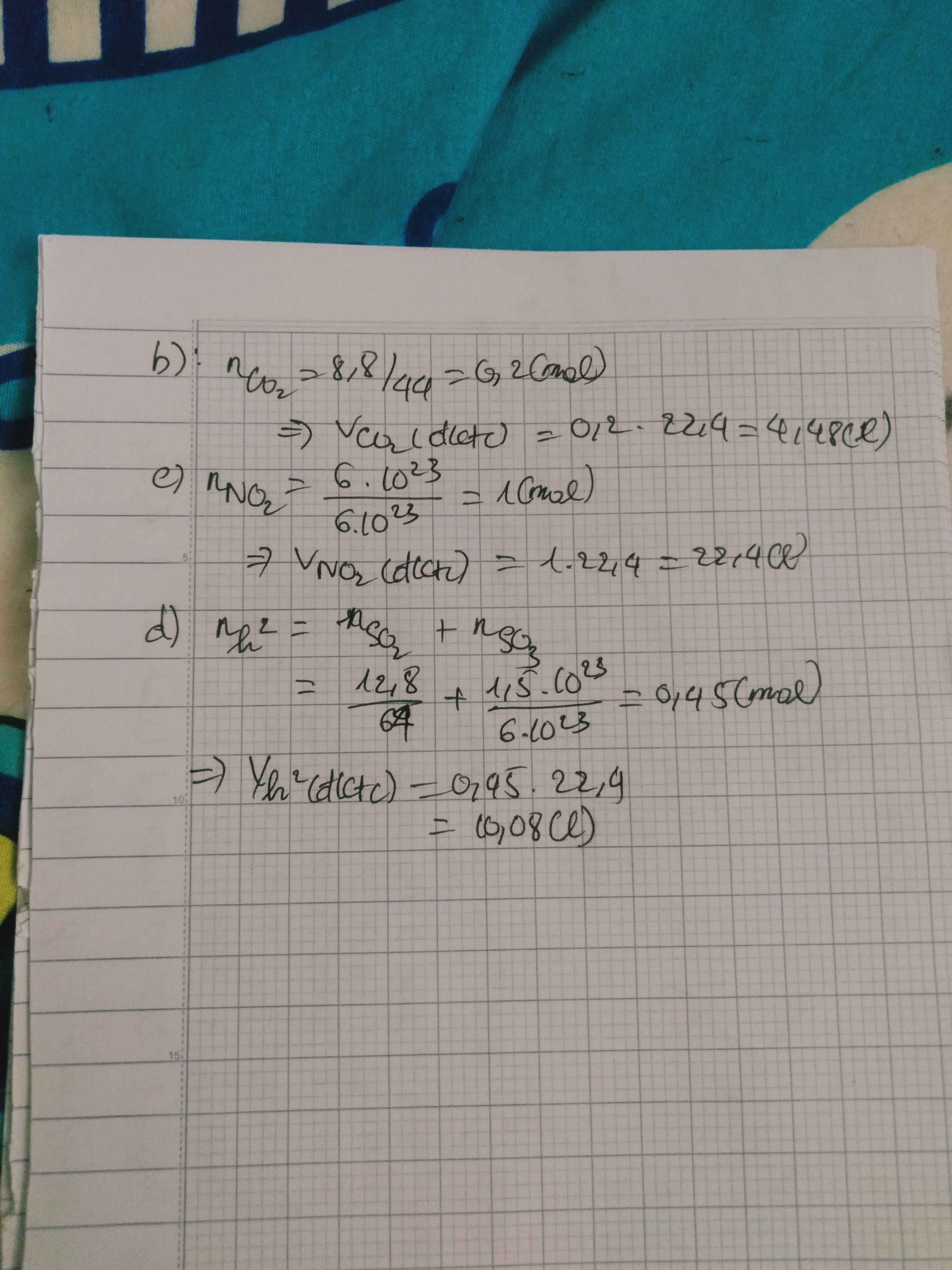$n_{CO_2} = \dfrac{8,8}{44} = 0,2(mol)$
$V_{CO_2} = 0,2.22,4 = 4,48(lít)$
$n_{NO_2} = \dfrac{6.10^{23}}{6.10^{23}} = 1(mol)$
$V_{NO_2} = 1.22,4 = 22,4(lít)$
$n_{SO_2} = \dfrac{12,8}{64} = 0,2(mol)$
$V_{SO_2} = 0,2.22,4 = 4,48(lít)$
$n_{SO_3} = \dfrac{1,5.10^{23}}{6.10^{23}} = 0,25(mol)$
$V_{SO_3} = 0,25.22,4 = 5,6(lít)$
Hãy tính thể tích (đktc) của
b)8,8g CO2
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
C)6.1023 phân tử NO2
\(n_{NO_2}=\dfrac{6.10^{23}}{6.10^{23}}=1\Rightarrow V_{NO_2}=1.22,4=22,4\left(lít\right)\)
d)Hỗn hợp gồm {12,8 g SO2, 1,5.10 pt SO3
\(n_{SO_2}=\dfrac{12,8}{54}=0,2\left(mol\right);n_{SO3}=\dfrac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
=> \(V_{hh}=\left(0,2+0,25\right).22,4=10,08\left(l\right)\)
b) Số mol của khí cacbonic
nCO2 = \(\dfrac{V_{CO2}}{22,4}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
Thể tích của khí cacbonic ở dktc
VCO2 = nCO2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
c) Số mol của nito đioxit
nNO2 = \(\dfrac{6.10^{-23}}{6.10^{-23}}\) = 1 (mol)
Thể tích của khí nito đioxit ở dktc
VNO2 = nNO2 . 22,4
= 1. 22,4
= 22,4 (l)
d) Số mol của lưu huỳnh đioxit
nSO2 = \(\dfrac{m_{SO2}}{M_{SO2}}=\dfrac{12,8}{64}=0,2\left(mol\right)\)
Thể tích của khí lưu huỳnh đioxit ở dktc
VSO2 = nSO2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
Số mol của lưu huỳnh trioxit
nSO3 = \(\dfrac{1,5.10^{-23}}{6.10^{-23}}=0,25\left(mol\right)\)
Thể tích của khí lưu huỳnh trioxit ở dktc
VSO3 = nSO3 . 22,4
= 0,25 . 22,4
= 5,6 (l)
Chúc bạn học tốt