\(V_{45}=0.068\)
=>\(2^3\cdot0.017=0.068\)
=>Cần giảm nhiệt độ xuống 15 độ C để tốc độ phản ứng là 0,017mol/(L.min)
\(V_{45}=0.068\)
=>\(2^3\cdot0.017=0.068\)
=>Cần giảm nhiệt độ xuống 15 độ C để tốc độ phản ứng là 0,017mol/(L.min)
Câu 4. Hãy thiết kế một thí nghiệm để chứng minh ảnh hưởng của nhiệt độ đến tốc độ phản ứng của zinc và sulfuric acid loãng.
Câu 2. Cho khoảng 2 g zinc (kẽm) dạng hạt vào một cốc đựng dung dịch H2SO4 2M (dư) ở nhiệt độ phòng. Nếu chỉ biến đổi một trong các điều kiện sau đây (các điều kiện khác giữ nguyên) thì tốc độ phản ứng sẽ thay đổi thế nào (tăng lên, giảm xuống hay không đổi)?
(a) Thay kẽm hạt bằng kẽm bột cùng khối lượng và khuấy đều.
(b) Thay dung dịch H2SO4 2 M bằng dung dịch H2SO4 1M có cùng thể tích.
(c) Thực hiện phản ứng ở nhiệt độ cao hơn (khoảng 50oC).
Câu 1. Hãy cho biết trong các phản ứng sau, phản ứng nào có tốc độ nhanh, phản ứng nào có tốc độ chậm?
(a) Đốt cháy nhiên liệu.
(b) Sắt bị gỉ.
(c) Trung hòa acid - base
Câu 3. Hydrogen peroxide phân hủy theo phản ứng: 2H2O2 → 2H2O + O2.
Đo thể tích oxygen thu được theo thời gian, kết quả được ghi trong bảng sau:
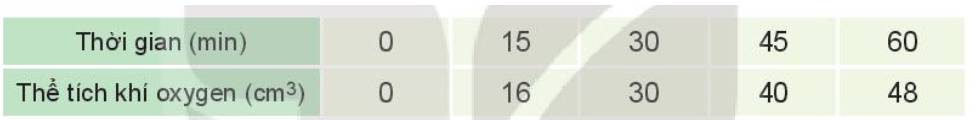
a) Vẽ đồ thị mô tả sự phụ thuộc của thể tích khí oxygen theo thời gian.
b) Tính tốc độ trung bình của phản ứng (theo cm3/min) trong khoảng thời gian:
- Từ 0 – 15 phút
- Từ 15 – 30 phút
- Từ 30 – 45 phút
- Từ 45 – 60 phút
Nhận xét sự thay đổi tốc độ trung bình theo thời gian.