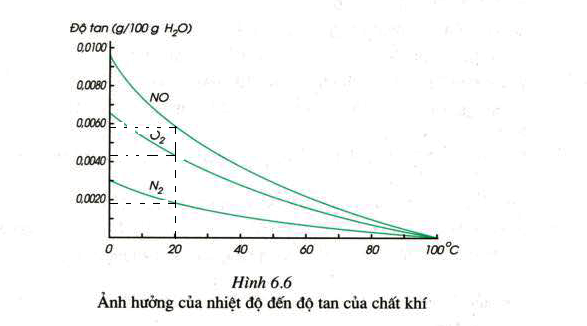
Căn cứ vào đồ thị về độ tan của chất khí trong nước( Hình 6.6 sgk), hãy ước lượng độ tan của các khí NO, O2, N2 ở nhà 20°C. Hãy chuyển đổi có bao nhiêu ml những khí trên tan trong 1 lít nước? Biết rằng ở 20°C và 1 atm, 1 mol chất khí có thể tích là 24l và khối lượng riêng của nước là 1g/ml. Giúp rm giải bài này với ạ. Giải thích rõ từng bước giúp e vì e k hiểu lắm 😐.
-Xét khí NO:
Tại 20oC, độ tan của NO là 0,0057 (g/ 100g H2O)
hay 100g H2O hòa tan tối đa 0,0057g NO
<=> 1000g H2O hòa tan tối đa 0,057g NO (1)
Mặt khác: \(V_{H_2O}=\dfrac{1000}{1}=1000\left(ml\right)=1\left(l\right)\)
\(n_{NO}=\dfrac{0,057}{30}=0,0019\left(mol\right)\Rightarrow V_{NO}=0,0019.24=0,0456\left(l\right)=45,6\left(ml\right)\)
(1) <=> 1 lít H2O hòa tan tối đa 45,6 ml khí NO
- Xét khí O2:
Tại 20oC, độ tan của O2 là 0,0042 (g/ 100g H2O)
hay 100g H2O hòa tan tối đa 0,0042g O2
<=> 1000g H2O hòa tan tối đa 0,042g O2 (2)
Mặt khác: \(V_{H_2O}=\dfrac{1000}{1}=1000\left(ml\right)=1\left(l\right)\)
\(n_{O_2}=\dfrac{0,042}{32}=1,3125.10^{-3}\left(mol\right)\Rightarrow V_{O_2}=1,3125.10^{-3}.24=0,0315\left(l\right)=31,5\left(ml\right)\)
(2) <=> 1 lít H2O hòa tan tối đa 31,5 ml khí O2
- Xét khí N2:
Tại 20oC, độ tan của N2 là 0,0018 (g/ 100g H2O)
hay 100g H2O hòa tan tối đa 0,0018g N2
<=> 1000g H2O hòa tan tối đa 0,018g N2 (3)
Mặt khác: \(V_{H_2O}=\dfrac{1000}{1}=1000\left(ml\right)=1\left(l\right)\)
\(n_{N_2}=\dfrac{0,018}{28}=\dfrac{9}{14000}\left(mol\right)\Rightarrow V_{N_2}=\dfrac{9}{14000}.24\approx0,01543\left(l\right)=15,43\left(ml\right)\)
(3) <=> 1 lít H2O hòa tan tối đa 15,43 ml khí N2













