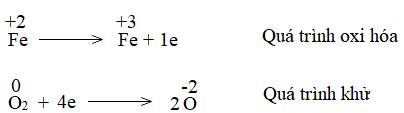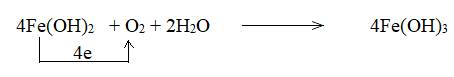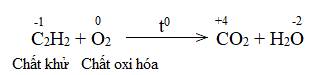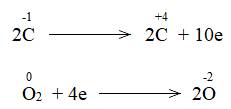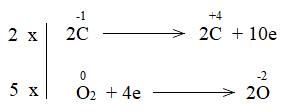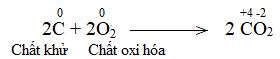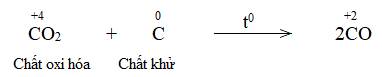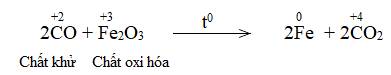Trong lò luyện gang, xảy ra phản ứng oxi hóa – khử theo sơ đồ:
Fe2O3 + CO \(\underrightarrow{t^o}\) Fe + CO2
Về bản chất, phản ứng oxi hóa - khử là gì, dựa vào dấu hiệu nào để nhận ra loại phản ứng đó?
Làm thế nào để lập phương trình hóa học của phản ứng trên?