P.ứ với acid : Tính base
P.ứ với oxy: Tính khử
P.ứ với acid : Tính base
P.ứ với oxy: Tính khử
Ammonia là một hợp chất của hydrogen và nitrogen, có rất nhiều ứng dụng trong đời sống và sản xuất. Ammonia có những tính chất và ứng dụng gì?
Khi thải rác thải sinh hoạt chứa một lượng lớn ion ammonium vào ao, hồ sẽ xảy ra quá trình oxi hoá ammonium thành ion nitrate dưới tác dụng của vi khuẩn. Quá trình này làm giảm oxygen hoà tan trong nước, gây ngạt cho sinh vật sống dưới nước. Người ta phải xử lí nguồn nước gây ô nhiễm đó bằng cách chuyển ion ammonium thành ammonia, rồi chuyển tiếp thành nitrogen không độc. Hãy đề xuất một số hóa chất để thực hiện quá trình trên và viết phương trình hoá học của các phản ứng xảy ra.
Cho cân bằng hoá học: 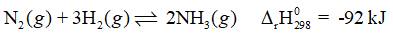
Cân bằng chuyển dịch theo chiều nào (có giải thích) khi:
a) tăng nhiệt độ.
b) tách ammonia ra khỏi hỗn hợp phản ứng.
c) giảm thể tích của hệ phản ứng.
Tìm hiểu thông tin và nêu một số ứng dụng của ammonia trong đời sống và sản xuất.
Quan sát Hình 4.2, giải thích hiện tượng thí nghiệm. Từ đó cho biết tại sao không thu khí ammonia bằng phương pháp đẩy nước.

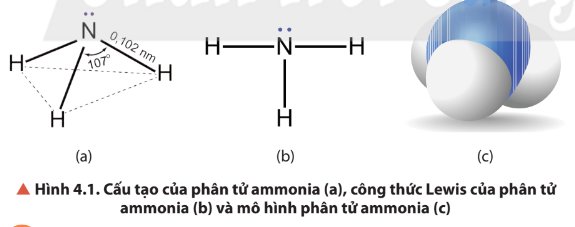
Quan sát Hình 4.1, mô tả cấu tạo phân tử ammonia. Dự đoán tính tan (trong nước) và tính oxi hóa – khử của ammonia. Giải thích.
Từ sự kết hợp giữa NH3 với nước, nhận xét tính acid — base của NH3 trong dung dịch. Nêu cách nhận biết khí NH3 bằng quỳ tím. Giải thích.
Chuẩn bị hai đầu đũa thuỷ tinh quấn bông. Đũa 1 nhúng vào dung dịch HCl đặc, đũa 2 nhúng vào dung dịch NH3 đặc, sau đó đưa lại gần nhau (Hình 4.3). Quan sát và nêu hiện tượng xảy ra. Từ đó để xuất phương pháp nhận biết ammonia bằng dung dịch HCl đặc.

Dựa vào nguyên lí chuyển dịch cân bằng Le Chatelier, hãy cho biết để tăng hiệu suất phản ứng tổng hợp NH3 cần điều chỉnh nhiệt độ và áp suất như thế nào. Điều đó có gây trở ngại gì cho phản ứng tổng hợp NH3 trên thực tế hay không? Vì sao?