Vì sao nước chlorine được sử dụng phổ biến để khử trùng, sát khuẩn?
Bài 17: Nguyên tố và đơn chất halogen
Mở đầu (SGK Cánh Diều trang 99)
Thảo luận (2)
Luyện tập 1 (SGK Cánh Diều trang 101)
Dựa vào xu hướng biến đổi tính chất của các đơn chất halogen trong bảng 17.3, hãy dự đoán về thể (trạng thái) của đơn chất astatine ở điều kiện thường. Giải thích.
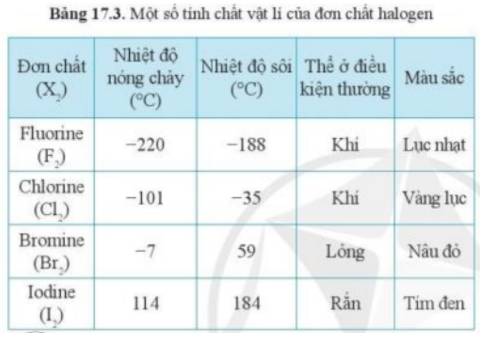
Thảo luận (1)Hướng dẫn giải- Theo bảng 17.3, xu hướng biến đổi trạng thái của các halogen ở điều kiện thường từ: khí → lỏng → rắn
- Mà astatine đứng dưới cùng trong nhóm halogen
=> Astatine tồn tại ở thể rắn trong điều kiện thường
- Giải thích: Do sự tăng khối lượng phân tử và sự tăng tương tác van dể Waals
(Trả lời bởi Hà Quang Minh)
Luyện tập 2 (SGK Cánh Diều trang 101)
Trong điều kiện thường, halogen nào ở thể rắn? Vì sao?
Thảo luận (1)Hướng dẫn giải- Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn
- Giải thích:
+ Khối lượng phân tử cao
+ Lực tương tác van der Waals giữa phân tử iodine mạnh
(Trả lời bởi Hà Quang Minh)
Luyện tập 3 (SGK Cánh Diều trang 102)
Calcium và fluorine kết hợp thành phân tử calcium fluorine, CaF2. Trong đó, nguyên tử nào đã nhường và nhường bao nhiêu electron? Nguyên tử nào đã nhận và nhận bao nhiêu electron?
Thảo luận (1)Hướng dẫn giải- Nguyên tử Fluorine có 7 electron ở lớp ngoài cùng => Nhận 1 electron từ nguyên tử Calcium để đạt cấu hình electron của khí hiếm
- Nguyên tử Calcium có 2 electron ở lớp ngoài cùng => Nhường 2 electron cho 2 nguyên tử Fluorine để đạt cấu hình electron của khí hiếm
(Trả lời bởi Hà Quang Minh)
Luyện tập 4 (SGK Cánh Diều trang 102)
Để hình thành phân tử phosphorus trichloride (PCl3) thì mỗi nguyên tử chlorine và phosphorus đã góp chung bao nhiêu electron hóa trị? Viết công thức Lewis của phân tử.
Thảo luận (1)Hướng dẫn giải- Trong phân tử phosphorus trichloride gồm 2 nguyên tố: P và Cl
+ Nguyên tử P có 5 electron ở lớp ngoài cùng => Góp chung 3 electron độc thân để hình thành 3 liên kết cộng hóa trị
+ Nguyên tử Cl có 7 electron ở lớp ngoài cùng => 3 nguyên tử Cl, mỗi nguyên tử góp chung 1 electron độc thân để hình thành 3 liên kết cộng hóa trị với P.
=> Khi đó, quanh P và Cl đều có 8 electron như khí hiếm Argon.
- Công thức Lewis của phân tử:
(Trả lời bởi Hà Quang Minh)
Luyện tập 5 (SGK Cánh Diều trang 103)
Theo độ âm điện, boron trifluoride là hợp chất ion, thực tế nó là hợp chất cộng hóa trị, với công thức Lewis như sau:
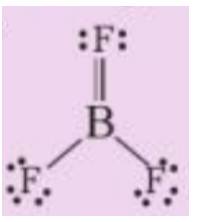
a) Viết phương trình hóa học tạo chất trên từ các đơn chất
b) Phân tử BF3 có bao nhiêu liên kết σ và bao nhiêu liên kết п?
Thảo luận (1)Hướng dẫn giảia) Phương trình hóa học: 2B + 3F2 → 2BF3
b) Trong phân tử BF3 có 2 liên kết đơn, 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết п)
=> Trong phân tử BF3 có 3 liên kết σ và 1 liên kết п
(Trả lời bởi Hà Quang Minh)
Thực hành (SGK Cánh Diều trang 104)
Thí nghiệm chlorine phản ứng với hydrogen được mô tả như sau:Bước 1: Chuẩn bị thí nghiệm như hình 17.1a với các ống nghiệm cùng đặt vào một giá thí nghiệmBước 2: Bơm vài giọt dung dịch hydrochloric acid (HCl) đặc từ xi – lanh chứa acid vào ống nghiệm chứa tinh thể potassium permanganate (thuốc tím, KMnO4) - ống nghiệm (1) để tạo khí chlorine. Khi pit – tông nâng lên khoảng ½ chiều cao của xi – lanh thu khí thì ngừng bơm acid (hình 17.1b)Bước 3: Rút xi – lanh thu khí ra khỏi ống nghiệm (1), chuy...
Đọc tiếp
Thí nghiệm chlorine phản ứng với hydrogen được mô tả như sau:
Bước 1: Chuẩn bị thí nghiệm như hình 17.1a với các ống nghiệm cùng đặt vào một giá thí nghiệm
Bước 2: Bơm vài giọt dung dịch hydrochloric acid (HCl) đặc từ xi – lanh chứa acid vào ống nghiệm chứa tinh thể potassium permanganate (thuốc tím, KMnO4) - ống nghiệm (1) để tạo khí chlorine. Khi pit – tông nâng lên khoảng ½ chiều cao của xi – lanh thu khí thì ngừng bơm acid (hình 17.1b)
Bước 3: Rút xi – lanh thu khí ra khỏi ống nghiệm (1), chuyển sang ghim vào ống nghiệm chứa kẽm - ống nghiệm (2) (hình 17.1c). Chuyển xi – lanh chứa dung dịch hydrochloric acid sang ống nghiệm (2)
Bước 4: Bơm vào giọt dung dịch hydrochloric acid từ xi – lanh chứa acid vào ống nghiệm (2) để tạo khí hydrogen. Đến khí pit – tông được nâng lên khoảng 2/3 xi – lanh thu khí thì ngừng bơm acid
Bước 5: Rút xi – lanh thu khí ra khỏi ống nghiệm (2). Ghim xi – lanh chứa hỗn hợp khí vào một nút cao su như hình 17.1d rồi kẹp vào giá thí nghiệm
Bước 6: Dùng đèn tử ngoại chiếu vào xi – lanh chứa hỗn hợp khí (hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi – lanh)
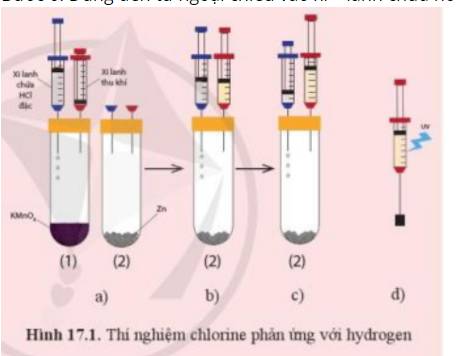
+ Quan sát và giải thích hiện tượng xảy ra khi dùng đèn tử ngoại chiếu vào xi – lanh chứa hỗn hợp khí (hoặc khi dùng ngọn lửa hơ nhẹ bên ngoài xi – lanh)
+ Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen có thể xảy ra hiện tượng như đã thấy trong thí nghiệm trên không? Giải thích
Thảo luận (1)Hướng dẫn giảia)
- Ở Bước 2: Ta thu được khí chlorine
- Ở Bước 4: Ta thu được khí hydrogen
=> Trong xi – lanh là hỗn hợp kí chlorine và hydrogen
- Khi chiếu đèn tử ngoại vào xi – lanh hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi - lanh chứa hỗn hợp khí chlorine và hydrogen sẽ gây ra hiện tượng nổ
- Phương trình hóa học: H2 + Cl2 → 2HCl
b) Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen không xảy ra hiện tượng như trên.
- Giải thích: Phản ứng giữa H2 và I2 cần đun nóng để phản ứng diễn ra, là phản ứng thuận nghịch, tạo hỗn hợp gồm HI sinh ra và lượng H2, I2 còn lại. Khả năng phản ứng kém nên không có hiện tượng nổ
H2 + I2 \( \rightleftharpoons \) 2HI
(Trả lời bởi Hà Quang Minh)
Thực hành (SGK Cánh Diều trang 105)
- Thí nghiệm 1: + Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium bromide hoặc potassium bromide loãng. + Nhỏ tiếp vào ống nghiệm vài giọt nước chlorine và lắc nhẹ + Có thể tiếp tục nhỏ vào ống nghiệm khoảng 2 mL cyclohexane- Thí nghiệm 2: + Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium iodide hoặc potassium iodide loãng + Nhỏ tiếp vào ống nghiệm vài giọt nước bromine loãng và lắc nhẹ. Có thể thêm tiếp vào ống nghiệm khoảng 2 mL cyclohexane + Thêm tiếp vào ống nghiệm vài giọt hồ ti...
Đọc tiếp
- Thí nghiệm 1:
+ Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium bromide hoặc potassium bromide loãng.
+ Nhỏ tiếp vào ống nghiệm vài giọt nước chlorine và lắc nhẹ
+ Có thể tiếp tục nhỏ vào ống nghiệm khoảng 2 mL cyclohexane
- Thí nghiệm 2:
+ Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium iodide hoặc potassium iodide loãng
+ Nhỏ tiếp vào ống nghiệm vài giọt nước bromine loãng và lắc nhẹ. Có thể thêm tiếp vào ống nghiệm khoảng 2 mL cyclohexane
+ Thêm tiếp vào ống nghiệm vài giọt hồ tinh bột
Giải thích các hiện tượng xảy ra và minh họa bằng phương trình hóa học
Thảo luận (1)Hướng dẫn giải- Thí nghiệm 1:
+ Khi cho nước chlorine màu vàng rất nhạt vào dung dịch sodium bromide không màu thì tạo ra dung dịch màu vàng nâu của bromine:
Cl2(aq) + 2NaBr(aq) → 2NaCl(aq) + Br2(aq)
+ Khi nhỏ 2 mL cyclohexane vào ống nghiệm, quan sát thấy màu vàng nâu của bromine nhạt dần do bromine tham gia phản ứng với cyclohexane:
Br2 + C6H12 → HBr + C6H11Br
- Thí nghiệm 2:
+ Khi cho nước bromine màu vàng vào dung dịch sodium iodine không màu thì tạo ra dung dịch màu vàng:
Br2(aq) + 2NaI(aq) → 2NaBr(aq) + I2(aq)
+ Khi cho thêm 2 mL cyclohexane thấy màu dung dịch nhạt dần do bromine tham gia phản ứng với cyclohexane:
Br2 + C6H12 → HBr + C6H11Br
+ Khi thêm tiếp vài giọt hồ tinh bột thì thấy dung dịch từ màu vàng chuyển sang màu xanh tím do iodine tác dụng với hồ tinh bột
(Trả lời bởi Hà Quang Minh)
Câu hỏi (SGK Cánh Diều trang 105)
Giả sử có thí nghiệm sau: Nhỏ nhanh vài giọt bromine màu nâu đỏ vào ống nghiệm chứa nước, đậy kín, lắc đều. Trong dung dịch bromine có những chất nào? Vì sao?
Thảo luận (1)Hướng dẫn giảiSau khi nhỏ nhanh vài giọt bromine vào ống nghiệm chứa nước, dung dịch bromine có những chất: Br2, H2O, HBr, HBrO.
Br2(aq) + H2O(l) \( \rightleftharpoons \) HBr(aq) + HBrO(aq)
- Vì phản ứng xảy ra thuận nghịch nên trong dung dịch có cả chất tham gia và chất sản phẩm
(Trả lời bởi Hà Quang Minh)
Thực hành (SGK Cánh Diều trang 106)
Thí nghiệm tính tẩy màu của khí chlorine.
Chuẩn bị thí nghiệm như hình 17.2
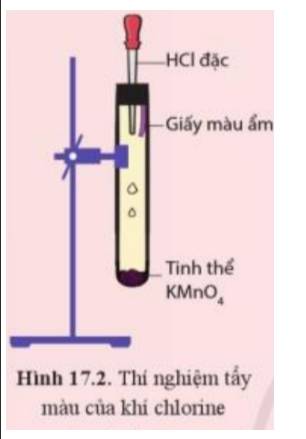
Bóp nhẹ phần cao su của ống nhỏ giọt để dung dịch hydrochloric acid chảy xuống ống nghiệm. Quan sát các hiện tượng xảy ra và giải thích.
Thảo luận (1)Hướng dẫn giải- Hiện tượng: Xuất hiện khí màu vàng và giấy màu ẩm bị nhạt màu dần rồi mất màu
- Giải thích:
+ Khi nhỏ HCl đặc vào tinh thể KMnO4, sản phẩm tạo thành có khí chlorine:
2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O
+ Khí chlorine tác dụng với nước ở giấy màu ẩm tạo thành hỗn hợp có tính tẩy màu: HCl và HClO
Cl2(aq) + H2O(l) \( \rightleftharpoons \) HCl(aq) + HClO(aq)
=> Dung dịch này còn được gọi là dung dịch nước chlorine, có tính tẩy màu, sát khuẩn
(Trả lời bởi Hà Quang Minh)
