Bài 4. Sơ lược về bảng tuần hoàn các nguyên tố hoá học
Nội dung lý thuyết
I. Nguyên tắc sắp xếp các nguyên tố hoá học trong bảng tuần hoàn
- Năm 1869, nhà bác học người Nga D. I. Mendeleev đã xây dựng bảng tuần hoàn theo chiều tăng dần khối lượng nguyên tử.
- Các nhà khoa học hiện đại đã chứng minh rằng điện tích hạt nhân nguyên tử mới là cơ sở để xây dựng bảng tuần hoàn.
- Hiện nay, bảng tuần hoàn các nguyên tố hoá học gồm 118 nguyên tố được xây dựng theo nguyên tắc sau:
- Các nguyên tố hóa học được sắp xếp theo chiều tăng dần của điện tích hạt nhân.
- Các nguyên tố hóa học trong cùng một hàng có cùng số lớp electron trong nguyên tử.
- Các nguyên tố hóa học trong cùng một cột có tính chất hóa học gần giống nhau.

Một mẫu bảng tuần hoàn các nguyên tố hoá học
II. Cấu tạo bảng tuần hoàn các nguyên tố hoá học
1. Ô nguyên tố
- Mỗi nguyên tố hoá học được sắp xếp vào một ô của bảng tuần hoàn, được gọi là ô nguyên tố.
Ví dụ 1: Ô nguyên tố carbon cung cấp các thông tin về nguyên tử carbon.
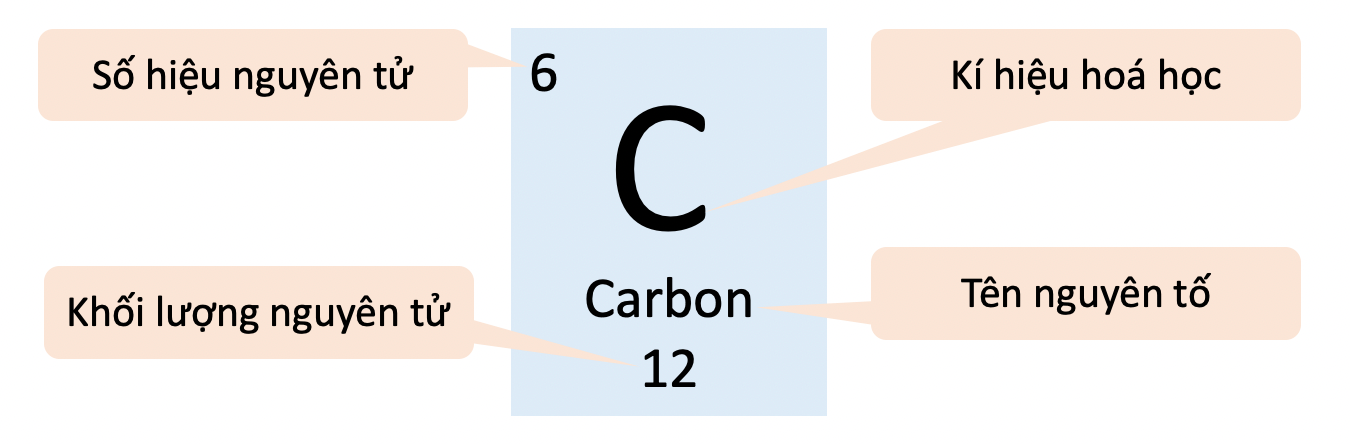
- Ô nguyên tố cho biết:
- Số hiệu nguyên tử (Z).
- Kí hiệu hoá học.
- Tên nguyên tố.
- Khối lượng nguyên tử.
- Số hiệu nguyên tử (Z) = số đơn vị điện tích hạt nhân = số electron trong nguyên tử = số thứ tự của nguyên tố trong bảng tuần hoàn.
@2314995@
2. Chu kì
- Chu kì gồm các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được sắp xếp thành hàng theo điện tích hạt nhân tăng dần từ trái qua phải.
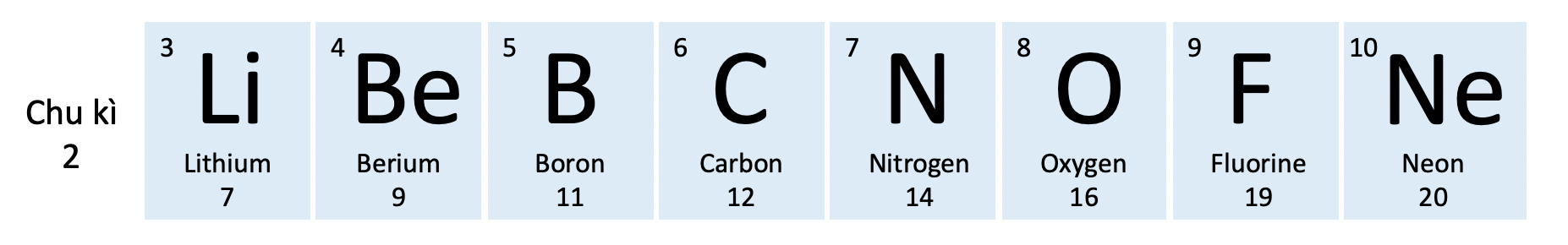
Chu kì 2 trong bảng tuần hoàn các nguyên tố hoá học
- Bảng tuần hoàn hiện nay gồm 7 chu kì, được đánh số từ 1 đến 7.
- Chu kì 1, 2, 3 được gọi là là các chu kì nhỏ, chu kì 4, 5, 6, 7 được gọi là là các chu kì lớn.
Ví dụ 2: Chu kì 1 gồm hai nguyên tố H và He, chu kì 2 gồm 8 nguyên tố từ Li đến Ne, chu kì 3 gồm 8 nguyên tố từ Na đến Ar.
3. Nhóm
- Bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
- Các nguyên tố trong cùng một nhóm A có số electron lớp ngoài cùng giống nhau, do đó chúng có tính chất hoá học tương tự nhau.
- Trong cùng một nhóm, khi đi từ trên xuống dưới, điện tích hạt nhân tăng dần.
- Số thứ tự của nhóm A bằng số electron lớp ngoài cùng trong nguyên tử của nguyên tố thuộc nhóm đó.
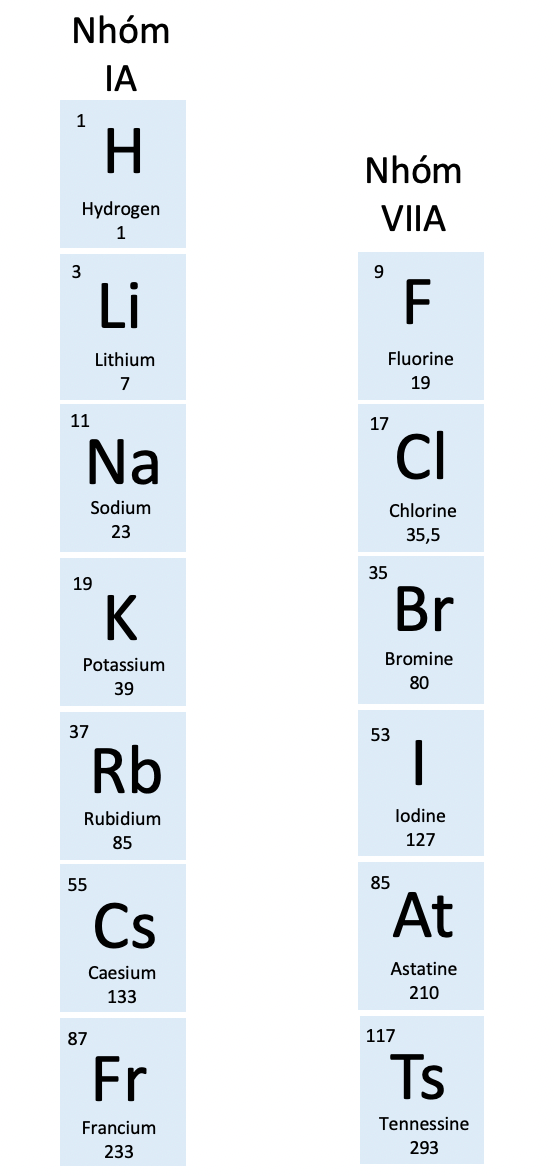
Nhóm IA và VIIA trong bảng tuần hoàn
@2315053@
III. Vị trí các nhóm nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn
1. Các nguyên tố kim loại
- Trong số 118 nguyên tố hoá học đã biết có hơn 90 nguyên tố kim loại.
- Vị trí nguyên tố kim loại trong bảng tuần hoàn:
- Hầu hết các nguyên tố thuộc nhóm IA, IIA, IIIA và một số nguyên tố ở các nhóm IVA, VA, VIA.
- Các nguyên tố thuộc nhóm IB đến VIIIB, các nguyên tố lanthanide và actinide ở cuối bảng tuần hoàn.

Ứng dụng của một số nguyên tố kim loại thông dụng trong đời sống
2. Các nguyên tố phi kim
- Trong số 118 nguyên tố hoá học đã biết có chưa đến 20 nguyên tố là phi kim.
- Ở điều kiện thường, chúng có thể ở thể rắn, thể lỏng hay thể khí.
- Vị trí nguyên tố phi kim trong bảng tuần hoàn:
- Hầu hết các nguyên tố thuộc nhóm VA, VIA, VIIA.
- Một số nguyên tố thuộc nhóm IIIA, IVA.
- Nguyên tố H ở nhóm IA.
3. Các nguyên tố khí hiếm
- Trong số 118 nguyên tố hoá học đã biết có 7 nguyên tố là nguyên tố khí hiếm.
- Nguyên tử của chúng có lớp electron ngoài cùng bền vững nên khó bị biến đổi hoá học.
- Nguyên tố khí hiếm nằm ở nhóm VIIIA trong bảng tuần hoàn.
@2315152@
1. Các nguyên tố hoá học trong bảng tuần hoàn được sắp xếp theo chiều tăng dần điện tích hạt nhân của nguyên tử. Các nguyên tố cùng chu kì có cùng số lớp electron, các nguyên tố cùng nhóm có tính chất gần giống nhau.
2. Cấu trúc bảng tuần hoàn gồm các ô nguyên tố, chu kì và nhóm.
3. Trong bảng tuần hoàn, các nguyên tố kim loại tập trung ở các nhóm IA, IIA, IIIA và các nhóm B. Các nguyên tố phi kim tập trung ở các nhóm VA, VIA, VIIA, còn các nguyên tố khí hiếm ở nhóm VIIIA.