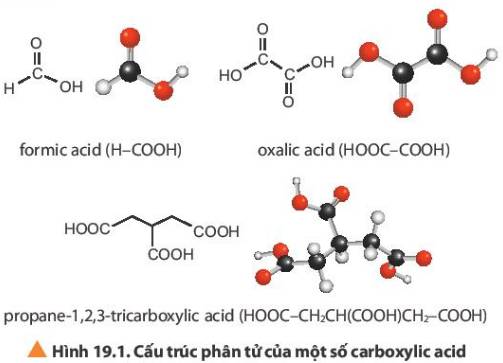
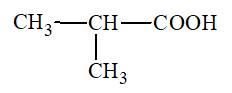
Một số loại acid hữu cơ được dùng trong thực phẩm như acetic acid, lactic acid. Thường gặp nhất là carboxylic acid, có nhiều trong tự nhiên như trong thành phần của các loại trái cây, chúng gây ra vị chua và một số mùi quen thuộc. Carboxylic acid là gì? Những tính chất nào đặc trưng cho carboxylic acid?