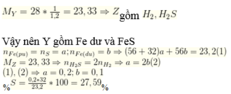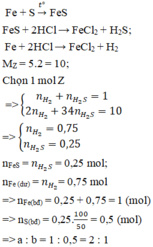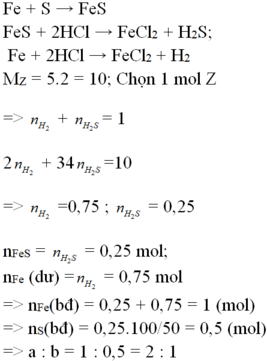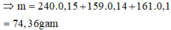Nung hỗn hợp bột gồm Cu và KClO3 (tỉ lệ mol 1:1) trong bình kín, sau phản ứng kết thúc thu được khí X và chất rắn Y. Dùng khí X để đốt cháy hết hỗn hợp C và S thu được hỗn hợp khí Z gồm 3 khí. Xác định X, Y, Z và viết các phương trình hóa học.

Những câu hỏi liên quan
Một hỗn hợp gồm KMnO4 và KClO3 có khối lượng m gam đem nung nóng thu được chất rắn x và khí O2 trọng lượng khí oxi sinh ra với không khí theo tỉ lệ thể tích là 2/3 trong bình kín thu được hỗn hợp Y. Cho vào bình 1,128 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp khí Z( có mặt một khí duy trì sự cháy) trong đó khí CO2 chiếm 27,5% về khối lượng. Tính khối lượng m ban đầu, biết trong chất rắn X có 43,5g MnO2 chiếm 46,4% về khối lượng
Đọc tiếp
Một hỗn hợp gồm KMnO4 và KClO3 có khối lượng m gam đem nung nóng thu được chất rắn x và khí O2 trọng lượng khí oxi sinh ra với không khí theo tỉ lệ thể tích là 2/3 trong bình kín thu được hỗn hợp Y. Cho vào bình 1,128 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp khí Z( có mặt một khí duy trì sự cháy) trong đó khí CO2 chiếm 27,5% về khối lượng. Tính khối lượng m ban đầu, biết trong chất rắn X có 43,5g MnO2 chiếm 46,4% về khối lượng
Z gồm CO2 và O2 dư
$C + O_2 \xrightarrow{t^o} CO_2$
$n_{CO_2} =n_{O_2\ pư} = n_C = \dfrac{1,128}{12} = 0,094(mol)$
Gọi $n_{O_2} = 2a \to n_{không\ khí} = 3a(mol)$
Trong Y :
$n_{O_2} = 2a + 3a.20\% = 2,6a(mol)$
$n_{N_2} = 3a.80\% = 2,4a(mol)$
Trong Z :
$n_{CO_2} = 0,094(mol)$
$n_{N_2} = 2,4a(mol)$
$n_{O_2\ dư} = n_{O_2} - n_{O_2\ pư} = 2,6a - 0,094(mol)$
m CO2 =0,094.44 = 4,136(gam)
=> m Z = 4,136 : 27,5% = 15,04(gam)
SUy ra :
4,136 + 2,4a.28 + (2,6a - 0,094).32 = 15,04
=> a = 0,0925
=> n O2 = 0,0925.2 = 0,185(mol)
m X = 43,5 : 46,4% = 93,75(gam)
Bảo toàn khối lượng : m = 93,75 + 0,185.32 = 99,67(gam)
Đúng 2
Bình luận (1)
Nung m gam hỗn hợp KClO3 và KMnO4 thu được chất rắn Y và O2, biết KClO3 phản ứng hết, còn KMnO4 còn dư một phần, trong Y có 0,894 gam KCl chiếm 8,132% theo khối lượng, trộn lượng O2 trên với không khí theo tỉ lệ 1:3 trong bình kín ta thu được hỗn hợp khí Z, cho vào bình 0,528 gam Cacbon rồi đốt cháy hết thì thu được hỗn hợp khí T gồm N2, O2, CO2 trong đó CO2 chiếm 22,92% về thể tích. Giá trị của m gần nhất với giá trị nào sau đây? A. 11,96 B. 12,40 C. 12,53 D. 12,12
Đọc tiếp
Nung m gam hỗn hợp KClO3 và KMnO4 thu được chất rắn Y và O2, biết KClO3 phản ứng hết, còn KMnO4 còn dư một phần, trong Y có 0,894 gam KCl chiếm 8,132% theo khối lượng, trộn lượng O2 trên với không khí theo tỉ lệ 1:3 trong bình kín ta thu được hỗn hợp khí Z, cho vào bình 0,528 gam Cacbon rồi đốt cháy hết thì thu được hỗn hợp khí T gồm N2, O2, CO2 trong đó CO2 chiếm 22,92% về thể tích. Giá trị của m gần nhất với giá trị nào sau đây?
A. 11,96
B. 12,40
C. 12,53
D. 12,12
Có sự thay đổi số mol hỗn hợp khí xảy ra trong các phản ứng đốt cháy, hoặc đôi khi không thay đổi.
C/S + O2 → CO2/ SO2 (1)
2Al +3/2O2 → Al2O3 (2)
C, S hay A1, chúng là các chất rắn được đem đốt cháy với oxi hoặc một hỗn hợp khí chứa oxi,… và sau phản ứng người ta thu được một khí/hỗn hợp khí mới,…
Trong nhiều trường hợp, ta cần so sánh số mol hỗn hợp khí mới và cũ, như trong tình huống (1), hai giá trị này bằng nhau, tình huống (2) thì khác, khi có oxit tạo thành, tổng số mol khí sẽ giảm.
Với bài tập này, phản ứng của cacbon với oxi xảy ra và số mol hỗn hợp khí không thay đổi, đó chỉ là một sự thay thế như tăng giảm khối lượng vậy, O2 trở thành CO2 theo tỉ lệ 1:1 → nZ = nT
Bảo toàn nguyên tố C: nC/T = nCO2/T = 0,528/12 =0,044
→nT = 0,044/22,92% = 0,192 = nZ → nO2 trộn = 0,192/4 =0,048
→m = mY + mO2 = 0,894/8,132% + 32.0,048 = 12,5296
Chọn đáp án C
Đúng 0
Bình luận (0)
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y và O2. Biết KClO3 phân hủy hoàn toàn, còn KMnO4 chỉ bị phân hủy một phần. Trong Y có 0,894 gam KCl chiếm 8,132% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích VO2 : Vkk 1 : 3 trong một bình kín ta thu được hỗn hợp khí Z. Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbon, phản ứng hoàn toàn, thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22,92% thể tích. Biết không khí chứa 20% thể tích oxi...
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y và O2. Biết KClO3 phân hủy hoàn toàn, còn KMnO4 chỉ bị phân hủy một phần. Trong Y có 0,894 gam KCl chiếm 8,132% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích VO2 : Vkk = 1 : 3 trong một bình kín ta thu được hỗn hợp khí Z. Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbon, phản ứng hoàn toàn, thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22,92% thể tích. Biết không khí chứa 20% thể tích oxi, còn lại là. Giá trị m (gam) là
A. 12,59
B. 12,53
C. 12,70
D. 12,91
Đáp án B
Từ mKCl = 0,894g => mY = 10,994g
Đặt nO2 tạo ra = x => nkk = 3x có nO2 = 0,75x và nN2 = 2,25x (mol)
, nCO2 = nC = 0,044 mol => nO2 dư = (x + 0,75x) – 0,044 (mol)
=> nT = nCO2.100/22,92 = nO2 dư + nN2 + nCO2
=> 1,75x – 0,044 + 2,25x + 0,044 = 0,192
=> x = 0,048 mol
=> m = mY + mO2 tạo ra = 12,53g
=>B
Đúng 0
Bình luận (1)
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được 11 gam chất rắn Y và O2. Trộn lượng O2 trên với không khí theo tỉ lệ thể tích trong một bình 0,576 gam cacbon rồi đốt cháy hết cacbon, sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp khí T gồm ba khí O2, N2, CO2 trong CO2 chiếm 25% thể tích. Giá trị m là: A. 12,92 B. 12,672 C. 12,536 D. 12,73
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được 11 gam chất rắn Y và O2. Trộn lượng O2 trên với không khí theo tỉ lệ thể tích trong một bình 0,576 gam cacbon rồi đốt cháy hết cacbon, sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp khí T gồm ba khí O2, N2, CO2 trong CO2 chiếm 25% thể tích. Giá trị m là:
A. 12,92
B. 12,672
C. 12,536
D. 12,73
Cho 23,2 gam hỗn hợp X gồm S và Fe vào một bình kín không chứa không khí. Nung bình đến khi phản ứng kết thúc thu được chất rắn Y. Cho Y tác dụng với axit H2SO4 loãng, dư thu được khí Z có tỉ khối đối với N2 là 1/1,2. Phần trăm khối lượng của S trong hỗn hợp X là A. 20,69% B. 27,59% C. 16,55% D. 48,28%
Đọc tiếp
Cho 23,2 gam hỗn hợp X gồm S và Fe vào một bình kín không chứa không khí. Nung bình đến khi phản ứng kết thúc thu được chất rắn Y. Cho Y tác dụng với axit H2SO4 loãng, dư thu được khí Z có tỉ khối đối với N2 là 1/1,2. Phần trăm khối lượng của S trong hỗn hợp X là
A. 20,69%
B. 27,59%
C. 16,55%
D. 48,28%
Nung nóng hỗn hợp bột X gồm a mol Fe và b mol S trong khí trơ, hiệu suất phản ứng bằng 50%, thu được hỗn hợp rắn Y. Cho Y vào dung dịch HCl dư, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z có tỉ khối so với H 2 bằng 5. Tỉ lệ a:b bằng
A. 2:1
B. 1:1
C. 3:1
D. 3:2
Nung nóng hỗn hợp bột X gồm a mol Fe và b mol S trong khí trơ, hiệu suất phản ứng bằng 50%, thu được hỗn hợp rắn Y. Cho Y vào dung dịch HCl dư, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z có tỉ khối so với H2 bằng 5. Tỉ lệ a:b bằng:
A. 2:1
B. 1:1
C. 3:1
D. 3:2
Một bình kín chỉ chứa hỗn hợp X gồm các chất sau: axetilen (0,2 mol), vinylaxetilen (0,3 mol), Hiđro (0,25 mol), và một ít bột niken. Nung nóng bình một thời gian thu được hỗn hợp khí Y có tỉ khối so với
H
2
bằng 17,75. Khí Y phản ứng vừa đủ với 0,54 mol
AgNO
3
trong
NH
3
thu được m gam kết tủa và 4,704 lít hỗn hợp khí Z (điều kiện tiêu chuẩn). Khí Z phản ứng tối...
Đọc tiếp
Một bình kín chỉ chứa hỗn hợp X gồm các chất sau: axetilen (0,2 mol), vinylaxetilen (0,3 mol), Hiđro (0,25 mol), và một ít bột niken. Nung nóng bình một thời gian thu được hỗn hợp khí Y có tỉ khối so với H 2 bằng 17,75. Khí Y phản ứng vừa đủ với 0,54 mol AgNO 3 trong NH 3 thu được m gam kết tủa và 4,704 lít hỗn hợp khí Z (điều kiện tiêu chuẩn). Khí Z phản ứng tối đa với 0,23 mol brom trong dung dịch. Giá trị của m là:
A. 74,36
B. 75,92
C. 76,18
D. 82,34
Nung m gam hỗn hợp X gồm KClO3 và KMnO4, thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là: A. 8,77. B. 8,53. C. 8,70. D. 8,91.
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4, thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là:
A. 8,77.
B. 8,53.
C. 8,70.
D. 8,91.