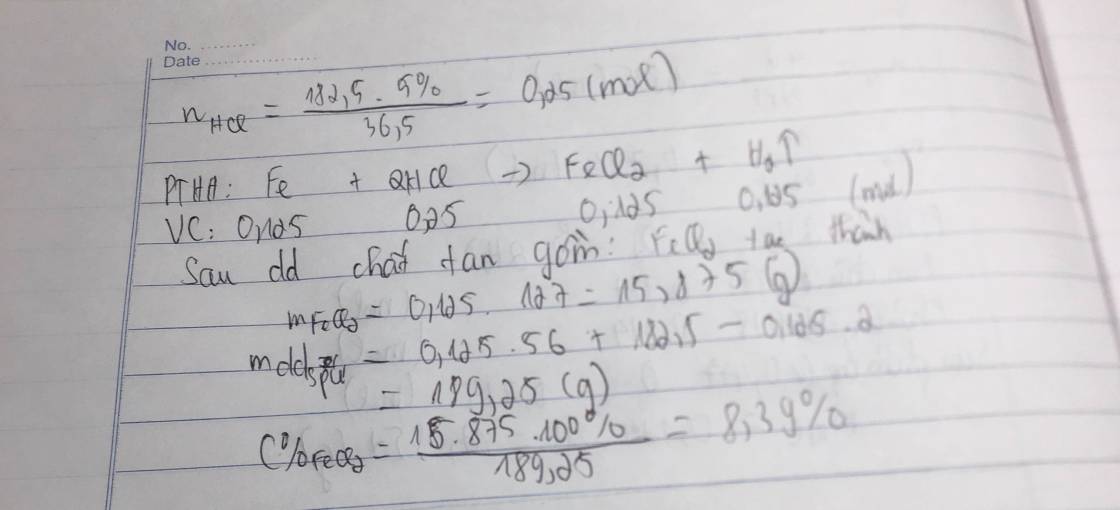Cho dung dịch CuSO4 có chứa 64g CuSO4 phản ứng vừa đủ với 400ml dung dịch NaOH a.Viết phương trình hoá học xảy ra b.Tính khối lượng kết tủa thu được c.tính nồng độ mol của dung dịch NaOH

Những câu hỏi liên quan
Cho 400 ml dung dịch CuSO4 1M tác dụng với dung dịch có chứa 40 g NaOH, thu được kết tủa A và dung dịch B. Nung kết tủa A đến khối lượng không đổi, được chất rắn C. a.Viết các phương trình phản ứng xảy ra. b.Tính khối lượng chất rắn C. c.Tính khối lượng các chất có trong dung dịch B.
Cho 400 ml dung dịch CuSO4 1M tác dụng với dung dịch có chứa 40 g NaOH, thu được kết tủa A và dung dịch B. Nung kết tủa A đến khối lượng không đổi, được chất rắn C. a.Viết các phương trình phản ứng xảy ra. b.Tính khối lượng chất rắn C. c.Tính khối lượng các chất có trong dung dịch B.
a) \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
b) \(n_{CuSO_4}=0,4.1=0,4\left(mol\right)\)
\(n_{NaOH}=\dfrac{40}{40}=1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,4}{1}< \dfrac{1}{2}\) => CuSO4 hết, NaOH dư
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
_______0,4----->0,8---------->0,4-------->0,4
Cu(OH)2 --to--> CuO + H2O
0,4------------->0,4
=> mCuO = 0,4.80 = 32 (g)
c) \(\left\{{}\begin{matrix}m_{NaOH\left(dư\right)}=\left(1-0,8\right).40=8\left(g\right)\\m_{Na_2SO_4}=0,4.142=56,8\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho dung dịch chứa 16 gam CuSO4 tác dụng vừa đủ với 200 gam dung dịch NaOH. a. Viết PTHH b.Tính khối lượng chất kết tủa tạo thành c.Tính nồng độ % của dung dịch NaOH
Ta có: \(n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\)
a. \(PTHH:CuSO_4+2NaOH--->Cu\left(OH\right)_2\downarrow+Na_2SO_4\)
b. Theo PT: \(n_{Cu\left(OH\right)_2}=n_{CuSO_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu\left(OH\right)_2}=0,1.98=9,8\left(g\right)\)
c. Theo PT: \(n_{NaOH}=2.n_{CuSO_4}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{NaOH}=0,2.40=8\left(g\right)\)
\(\Rightarrow C_{\%_{NaOH}}=\dfrac{8}{200}.100\%=4\%\)
Đúng 1
Bình luận (0)
Cho 40 ml dung dịch có chứa 15,2 gam CuSO4 tác dụng vừa đủ với dung dịch NaOH 2M
a) Tính khối lượng chất rắn thu được sau phản ứng và thể tích dung dịch NaOH cần dùng.
b) tính nồng độ mol các chất tan có trong dung dịch sau phản ứng?
c) Lọc lấy kết tủa nung trong không khí đến khối lượng không đổi thu được bao nhiêu gam chất rắn
\(n_{CuSO_4}=\dfrac{15,2}{160}=0,095mol\\ CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
0,095 0,19 0,095 0,095
\(m_{rắn}=m_{Cu\left(OH\right)_2}=0,095.98=9,31g\\ V_{ddNaOH}=\dfrac{0,19}{2}=0,095l\\ b)C_{M_{Na_2SO_4}}=\dfrac{0,095}{0,04+0,095}\approx0,7M\\ c)Cu\left(OH\right)_2\xrightarrow[t^0]{}CuO+H_2O\)
0,095 0,095
\(m_{rắn}=m_{CuO}=0,095.80=7,6g\)
Đúng 2
Bình luận (0)
Cho 50 gam dung dịch NaOH 20% vào dung dịch CuSO4 phản ứng xảy ra vừa đủ Hãy tính
a khối lượng dung dịch CuSO4 5% cần vừa đủ
b. khối lượng kết tủa tạo thành
C . khối lượng Na2SO4 tạo thành với nồng độ phần trăm của N2 SO4 trong dung dịch thu được sau phản ứng
Trộn 40 ml dung dịch có chứa 16 g CuSO4 với 60 ml dung dịch có chứa 12 g NaOH a Viết phương trình phản ứng xảy ra b Tính khối lượng chất rắn thu được sau phản ứng c tính nồng độ mol các chất tan có trong dung dịch sau phản ứng? cho rằng thể tích của dung dịch không thay đổi đáng kể
Cho 200ml dung dịch CuSO4 1M phản ứng vừa đủ với 200ml dung dịch KOH. a/ Viết phương trình phản ứng b/ Tính nồng độ M (mol/l) của dung dịch KOH c/ Tính khối lượng kết tủa Cu(OH)2 thu được? d/ Tính nồng độ M (mol/l) dung dịch K2SO4 thu được sau phản ứng? (Xem như thể tích dung dịch thay đổi không đáng kể)(Cho: Cu 64; K 39; O 16; H 1; S 32)
Đọc tiếp
Cho 200ml dung dịch CuSO4 1M phản ứng vừa đủ với 200ml dung dịch KOH.
a/ Viết phương trình phản ứng
b/ Tính nồng độ M (mol/l) của dung dịch KOH
c/ Tính khối lượng kết tủa Cu(OH)2 thu được?
d/ Tính nồng độ M (mol/l) dung dịch K2SO4 thu được sau phản ứng?
(Xem như thể tích dung dịch thay đổi không đáng kể)
(Cho: Cu = 64; K = 39; O = 16; H = 1; S = 32)
200ml = 0,2l
\(n_{CuSO4}=1.0,2=0,2\left(mol\right)\)
a) Pt : \(CuSO_4+2KOH\rightarrow Cu\left(OH\right)_2+K_2SO_4|\)
1 2 1 1
0,2 0,4 0,2 0,2
b) \(n_{KOH}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddKOH}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
c) \(n_{Cu\left(OH\right)2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
⇒ \(m_{Cu\left(OH\right)2}=0,2.98=19,6\left(g\right)\)
d) \(n_{K2SO4}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{ddspu}=0,2+0,2=0,4\left(l\right)\)
\(C_{M_{K2SO4}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Cho săt tác dụng vừa đủ với 182,5 gam dung dịch HCl 5% đến khi phản ứng kết thúc thu được V lít khí ở đktc?
a.Viết phương trình hóa học xảy ra?
b. Tính khối lượng sắt đã phản ứng và tính V?
c.Tính nồng độ phần trăm của dung dịch muối thu được?
Fe+2HCl->FeCl2+H2
0,125--0,25---0,125-0,125
m HCl=9,125 g=>n HCl=\(\dfrac{9,125}{26,5}\)=0,25 mol
=>m Fe=0,125.56=7g
=>VH2=0,125.22,4=2,8l
=>C%FeCl2=\(\dfrac{0,125.127}{7+182,5-0,25}\).100=8,388%
Đúng 4
Bình luận (0)
Cho 500 (ml) dung dịch CuSO4 0,4M, thêm 300 (ml) dung dịch NaOH vừa đủ thì thu được kết tủa. Lọc lấy kết tủa đem nung thu được chất rắn. a) Tính khối lượng kết tủa. b) Tính nồng độ mol của dung dịch NaOH. c) Tính khối lượng chất rắn
a)\(n_{CuSO_4}=0,4.0,5=0,2\left(mol\right)\)
\(PTHH:CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
Mol: 0,2 0,4 0,2
⇒ \(m_{Cu\left(OH\right)_2}=0,2.98=19,6\left(g\right)\)
b)\(C_{M\left(ddNaOH\right)}=\dfrac{0,4}{0,3}=1,3\left(M\right)\)
c)\(PTHH:Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Mol: 0,2 0,2
=> mCuO = 0,2.80 = 16 (g)
Đúng 2
Bình luận (0)