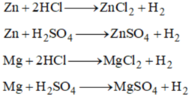Từ kẽm, sắt, axit clohydric (HCl), axit Sunfuric (H2SO4 ). Em hãy viết phương trình điều chế khí hidro.

Những câu hỏi liên quan
hãy viết phương trình điều chế khí hidro từ kẽm và axit sunfuric
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm có các kim loại kẽm và sắt, dung dịch axit clohiđric HCl và axit sunfuric H2SO4 loãng:
a. Viết phương trình hóa học có thể điều chế hi đro;
b. Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để diều chế được 2,24 lít khí hiđro (ở đktc)?
Xem chi tiết
\(Zn + 2HCl \to ZnCl_2 + H_2\\ Zn + H_2SO_4 \to ZnSO_4 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{Fe} = n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ m_{Fe} = 0,1.56 = 5,6(gam) ; m_{Zn} = 0,1.65 = 6,5(gam)\)
Đúng 3
Bình luận (2)
Trong phòng thí nghiệm có các kim loại kẽm và magie, các dung dịch axit sunfuric loãng H 2 S O 4 và axit clohidric HCl. Hãy viết các phương trình phản ứng để điều chế khí H 2 .
Trong phòng thí nghiệm có các kim loại kẽm và sắt, dung dịch axit clohiđric HCl và axit sunfuric H2SO4 loãng:
a. Viết phương trình hóa học có thể điều chế hi đro;
b. Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để diều chế được 2,24 lít khí hiđro (ở đktc)?
a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2
Fe + H2SO4 (loãng) → FeSO4 + H2
Zn + H2SO4 → ZnSO4 + H2
Fe + 2HCl → FeCl2 + H2
b. Số mol khí hiđro là: n = 0,1 (mol)
Khối lượng kẽm cần dùng là: m = 0,1x65 = 6,5 (g)
Khối lượng sắt cần dùng là: m = 0,1x56 = 5,6 (g).
Đúng 1
Bình luận (1)
a) Các PTHH biểu diễn phản ứng điều chế khí H2 trong phòng thí nghiệm dựa vào các hóa chất : HCl, H2SO4 loãng, Zn và Fe là:
(1) Zn + 2HCl -> ZnCl2 + H2\(\uparrow\)
(2) Fe + 2HCl -> FeCl2 + H2\(\uparrow\)
(3) Zn + H2SO4 (loãng) -> ZnSO4 + H2\(\uparrow\)
(4) Fe + H2SO4 (loãng) -> FeSO4 + H2\(\uparrow\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo các PTHH và đề bài, ta có:
\(n_{Zn\left(1\right)}=n_{Fe\left(2\right)}=n_{Zn\left(3\right)}=n_{Fe\left(4\right)}=n_{H_2}=0,1\left(mol\right)\)
- Khối lượng kẽm cần dùng : \(m_{Zn}=0,1.65=6,5\left(g\right)\)
- Khối lượng sắt cần dùng: \(m_{Fe}=0,1.56=5,6\left(g\right)\)
Đúng 0
Bình luận (0)
a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2 ↑
Fe + H2SO4 (loãng) → FeSO4 + H2 ↑
Zn + H2SO4 → ZnSO4 + H2 ↑
Fe + 2HCl → FeCl2 + H2 ↑
b. Số mol khí hiđro là: n = = 0,1 (mol)
Khối lượng kẽm cần dùng là: m = 0,1x65 = 6,5 (g)
Khối lượng sắt cần dùng là: m = 0,1x56 = 5,6 (g).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hãy viết các phương trình hóa học sau đây:
a/ Nhiệt phân thuốc tím KMnO4
b/ Điều chế khí hydrogen (hidro) từ kim loại sắt và hydrochloride acid (axit clohidric) HCl
c/ Điện phân nước
d/ Phản ứng giữa P2O5. và nước
e/ Đốt cháy kim loại kẽm trong khí oxigen (oxi)
Hãy viết các phương trình hóa học sau đây:
a/ Nhiệt phân thuốc tím KMnO4
2KMNO4-to>K2MnO4+MnO2+O2
b/ Điều chế khí hydrogen (hidro) từ kim loại sắt và hydrochloride acid (axit clohidric) HCl
Fe+2HCl->FeCl2+H2
c/ Điện phân nước
2H2O-đp->2H2+O2
d/ Phản ứng giữa P2O5. và nước
P2O5+3H2O->2H3PO4
e/ Đốt cháy kim loại kẽm trong khí oxigen (oxi)
2Zn+O2-to>2ZnO
Đúng 2
Bình luận (0)
`a)` `2KMnO_4` $\xrightarrow[]{t^o}$ `K_2MnO_4 + MnO_2 + O_2`
`b) Fe + 2HCl -> FeCl_2 + H_2`
`c)` `2H_2O` $\xrightarrow[]{đpnc}$ `2H_2 + O_2`
`d) P_2O_5 + 3H_2O -> 2H_3PO_4`
`e) 2Zn + O_2` $\xrightarrow[]{t^o}$ `2ZnO`
Đúng 0
Bình luận (1)
hãy trình bày 2 phương pháp điều chế hidro sunfua từ sắt , lưu huỳnh và axit sunfuric loãng .
hãy trình bày 2 phương pháp điều chế hidro sunfua từ sắt , lưu huỳnh và axit sunfuric loãng .
hãy trình bày 2 phương pháp điều chế hidro sunfua từ sắt , lưu huỳnh và axit sunfuric loãng .
Hai phương pháp điều chế H2S từ những chất trên.
Fe + S -> FeS (1)
FeS + H2SO4 -> FeSO4 + H2S (2)
Fe + H2SO4 -> FeSO4 + H2 (3)
H2 + S -> H2S (4)
Đúng 0
Bình luận (0)
hãy trình bày 2 phương pháp điều chế hidro sunfua từ sắt , lưu huỳnh và axit sunfuric loãng .