0,24 mol clo và 0,26 mol oxi phản ứng hết với 16,98g hỗn hợp gồm Mg và Al. khối lượng Mg và Al trong hỗn hợp là

Những câu hỏi liên quan
để oxi hóa hỗn hợp kim loại gồm 0,2 mol Al và 0,1 mol Mg cần phải dùng V lít (dktc) hỗn hợp clo và oxi. sau khi phản ứng kết tủa thu được 25,2 gam hh gồm oxit và muối. Vậy thể tích có trong hỗn hợp ban đầu là ( biết Cl= 35,5. O=16, Mg= 24, Al= 27)
A. 6,72 l B. 3,36 lít C. 2,24 lít D. 4,48 lít
help me !!!
\(\left\{{}\begin{matrix}Cl_2:x\left(mol\right)\\O_2:y\left(mol\right)\end{matrix}\right.\)
\(BTe:3n_{Al}+2n_{Mg}=2n_{Cl_2}+4n_{O_2}\)
\(\Rightarrow2x+4y=3\cdot0,2+0,1\cdot2=0,8\left(1\right)\)
\(BTKL:m_{muối}=m_{Al^{3+}}+m_{Mg^{2+}}+m_{Cl^-}+m_{O^{2-}}\)
\(\Rightarrow25,2=0,2\cdot27+0,1\cdot24+35,5\cdot2x+16\cdot2y\)
\(\Rightarrow71x+32y=17,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1mol\\y=0,1mol\end{matrix}\right.\)
\(V=V_{Cl_2}+V_{O_2}=0,1\cdot22,4+0,1\cdot22,4=4,48l\)
Chọn D
Đúng 1
Bình luận (0)
... "thể tích có trong hỗn hợp ban đầu" là thể tích của gì thế bn :)
Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 4,8 gam Mg và 8,1 gam Al, sau phản ứng thu được 37,05 gam hỗn hợp rắn Z gồm muối clorua và oxit của 2 kim loại. Phần trăm theo khối lượng của Clo trong hỗn hợp X là A. 26,5% B. 73,5% C. 62,5% D. 37,5%
Đọc tiếp
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 4,8 gam Mg và 8,1 gam Al, sau phản ứng thu được 37,05 gam hỗn hợp rắn Z gồm muối clorua và oxit của 2 kim loại. Phần trăm theo khối lượng của Clo trong hỗn hợp X là
A. 26,5%
B. 73,5%
C. 62,5%
D. 37,5%
Hỗn hợp khí X gồm oxi và clo có tỉ khối đối với hidro là 23,8 . Để phản ứng hết với 7,8 gam hỗn hợp Y gồm Mg và Al cần vừa hết 5,6 lít khí X ( đktc ) . Khối lượng Al có trong Y là ??
A. 4,5g
B. 2,7g
C. 3,6g
D. 5,4g
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 3,6
gam Mg và 5,4 gam Al, sau phản ứng thu được 29,95 gam hỗn hợp rắn Z gồm muối clorua và
oxit của 2 kim loại. Phần trăm theo khối lượng của Oxi trong hỗn hợp X là:
n Mg = 3,6/24 = 0,15(mol)
n Al = 5,4/27 = 0,2(mol)
Gọi n Cl2 = a(mol) ; n O2 = b(mol)
Bảo toàn e :
2n Cl2 + 4n O2 = 2n Mg + 3n Al
<=> 2a + 4b = 0,15.2 + 0,2.3 = 0,9(1)
Bảo toàn khối lượng :
m X + m Al + m Mg = m Z
=> 71a + 32b = 29,95 - 3,6 -5,4 = 20,95(2)
Từ (1)(2) suy ra a = 0,25 ; b = 0,1
%m O2 = 0,1.32/(0,25.71 + 0,1.32) .100% = 15,27%
Đúng 3
Bình luận (0)
Cho 1,35 gam hỗn hợp gồm Mg, Al, Cu tác dụng hết với HNO3 thu được hỗn hợp khí gồm 0,01 mol NO và 0,04 mol NO2. Cô cạn dung dịch sau phản ứng thu được hỗn hợp muối với khối lượng là: A. 5,69 gam B. 5,5 gam C. 4,98 gam D. 4,72 gam
Đọc tiếp
Cho 1,35 gam hỗn hợp gồm Mg, Al, Cu tác dụng hết với HNO3 thu được hỗn hợp khí gồm 0,01 mol NO và 0,04 mol NO2. Cô cạn dung dịch sau phản ứng thu được hỗn hợp muối với khối lượng là:
A. 5,69 gam
B. 5,5 gam
C. 4,98 gam
D. 4,72 gam
Cho 15,72 gam hỗn hợp gồm Mg, Al và Zn tác dụng với oxi không khí, sau phản ứng thu được 23,88 gam hỗn hợp A gồm các oxit (MgO, Al2O3, ZnO). Hòa tan hoàn toàn A trong dung dịch HCl dư.
a) Tính số mol HCl đã tham gia phản ứng
b) Tính khối lượng muối clorua thu được.
a) Bảo toàn khối lượng : $n_{O(oxit)} = \dfrac{23,88 - 15,72}{16} = 0,51(mol)$
$2H^+ + O^{2-} \to H_2O$
$n_{HCl} = 2n_O = 0,51.2 = 1,02(mol)$
b)
$n_{Cl^-} = n_{HCl} = 1,02(mol)$
Suy ra :
$m_{muối} = m_{kim\ loại} + m_{Cl} = 15,72 + 1,02.35,5 =51,93(gam)$
Đúng 1
Bình luận (0)
Cho V lít hỗn hợp khí A gồm clo và oxi tác dụng vừa hết với hỗn hợp B gồm 0,2 mol Al và 0,1 mol Mg thì thu được 25,2 gam hỗn hợp muối clorua và oxit của 2 kim loại. Số mol của Cl2 có trong V lít hỗn hợp khí A là A. 0,15 B. 0,25 C. 0,2 D. 0,3
Đọc tiếp
Cho V lít hỗn hợp khí A gồm clo và oxi tác dụng vừa hết với hỗn hợp B gồm 0,2 mol Al và 0,1 mol Mg thì thu được 25,2 gam hỗn hợp muối clorua và oxit của 2 kim loại. Số mol của Cl2 có trong V lít hỗn hợp khí A là
A. 0,15
B. 0,25
C. 0,2
D. 0,3
Chọn C. Đặt nCl2=x mol và nO2=y mol. Phản ứng vừa đủ tạo muối gồm các ion sau: Al3+, Mg2+ , Cl- , O2-.
Theo định luât bảo toàn điện tích: 3nAl3+ +2nMg2+ = nCl- + 2nO2- = 2nCl2 + 4nO2
mmuối= 27nAl3+ +24nMg2+ + 35,5nCl- + 16nO2-
→ Hệ
3 . 0 , 2 + 2 . 0 , 1 = 2 x + 4 y 27 . 0 , 2 + 24 . 0 , 1 + 71 x + 32 y = 25 , 2 → x = 0 , 2 y = 0 , 1
Đúng 0
Bình luận (0)
Để oxi hóa vừa hết 3,9 gam hỗn hợp gồm Mg và Al thành muối và oxit tương ứng cần phải dùng 3,36 lít hỗn hợp khí X gồm O2 và Cl2. Biết các khí đo ở đktc và trong X thì số mol của Cl2 gấp đôi số mol của O2. Vậy % khối lượng của Al trong hỗn hợp ban đầu bằng A. 30,77%. B. 96,23%. C. 69,23%. D. 34,62%.
Đọc tiếp
Để oxi hóa vừa hết 3,9 gam hỗn hợp gồm Mg và Al thành muối và oxit tương ứng cần phải dùng 3,36 lít hỗn hợp khí X gồm O2 và Cl2. Biết các khí đo ở đktc và trong X thì số mol của Cl2 gấp đôi số mol của O2. Vậy % khối lượng của Al trong hỗn hợp ban đầu bằng
A. 30,77%.
B. 96,23%.
C. 69,23%.
D. 34,62%.
Hỗn hợp X gồm Mg, Al, Al2O3 và MgCO3( trong đó oxi chiếm 25,157% về khối lương ) Hỗn hợp X gồm Mg, Al, Al2O3 và MgCO3 (trong đó oxi chiếm 25,157% về khối lượng). Hòa tan hết 19,08 gam X trong dung dịch chứa 1,32 mol NaHSO4 và x mol HNO3, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa có khối lượng 171,36 gam và hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 7,5. Cho dung dịch NaOH dư vào Y, thu được 19,72 gam kết tủa. Trong các nhận định dưới đây có bao nhiêu nh...
Đọc tiếp
Hỗn hợp X gồm Mg, Al, Al2O3 và MgCO3( trong đó oxi chiếm 25,157% về khối lương ) Hỗn hợp X gồm Mg, Al, Al2O3 và MgCO3 (trong đó oxi chiếm 25,157% về khối lượng). Hòa tan hết 19,08 gam X trong dung dịch chứa 1,32 mol NaHSO4 và x mol HNO3, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa có khối lượng 171,36 gam và hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 7,5. Cho dung dịch NaOH dư vào Y, thu được 19,72 gam kết tủa. Trong các nhận định dưới đây có bao nhiêu nhận định đúng :
(1) Trong X có 0,06 mol MgCO3
(2) Giá trị của x là 0,16
(3) Trong Z có 0,06 mol H2
(4) Khối lượng Al trong X là 4,86 g
A. 1
B. 2
C. 3
D. 4
Giải thích:
- Theo đề bài ta có :
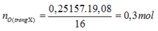
- Khi cho dung dịch tác dụng với NaOH dư ta được :
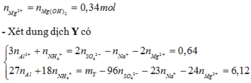
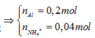
- Quy đổi hỗn hợp rắn X thành Mg, Al, O và C. → bảo toàn C
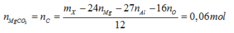
- Quay lại hỗn hợp rắn X với Al, Al2O3, Mg và MgCO3 có :
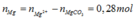
Bảo toàn O
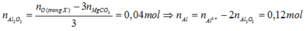
- Xét hỗn hợp khí Z ta có : nN2O = a và nH2 = b và nCO2 = 0,06 mol
→ MZ = 30 = (44a + 2b + 0,06.44) : (a + b +0,06)
Bảo toàn e cho phản ứng với HNO3 có 8nN2O + 2nH2 + 8nNH4+ = 3nAl + 2nMg
→ a = 0,06 và b =0,06 mol
- Xét toàn bộ quá trình phản ứng của X với dung dịch chứa 1,32 mol NaHSO4 và x mol HNO3 có:
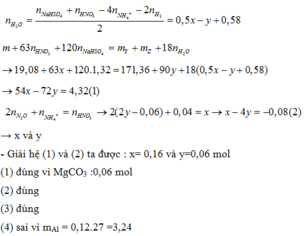
Đáp án C
Đúng 0
Bình luận (0)




















