Khí A có tỉ số đối với không khí là 0,552 và có thành phần khối lượng 75%C , 25%H. Nếu đốt 11,2 lít A(đktc) thì thể tích Oxi cần dùng là bao nhiêu ?

Những câu hỏi liên quan
Hãy tìm thể tích khí oxi đủ để đốt cháy hết 11,2 lít khí A.
Biết rằng:
- Khí A có tỉ lệ khối đối với không khí là 0,552.
- Thành phần theo khối lượng của khí A là: 75% C và 25% H.
Các thể tích khí đo ở đktc.
dA/kk = 0,552 ⇒ Khối lượng mol của khí A: 29.0,552 = 16 (g)
Đặt CTHH của khí A là CxHy
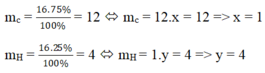
Công thức hóa học của khí A là: CH4
PTPỨ:

Tỉ lệ số mol cũng chính là tỉ lệ thể tích.
Theo phương trình nO2 = 2.nCH4 ⇒ VO2 = 2.VCH4 = 2.11,2 = 22,4(l)
Đúng 0
Bình luận (0)
Hãy tìm thể tích khí oxi đủ để đốt cháy hết 11,2 lít khí A. Biết rằng: – Khí A có tỉ lệ khối đối với không khí là 0,552. Thành phần theo khối lượng của khí A là: 75% C và 25% H (Các thể tích khí đo ở đktc)
Ta có: \(M_A=0,552.29=16\)
Gọi CTTQ của A là \(C_xH_y\) (với x;y thuộc N*)
Ta có: \(x:y=\dfrac{\%m_C}{M_C}:\dfrac{\%m_H}{M_H}=\dfrac{75\%}{12}:\dfrac{25\%}{1}=0,0625:0,25=1:4\)
Suy ra CTDGN của A là \(\left(CH_4\right)_n\)
Mặt khác \(16.n=16\Rightarrow n=1\)
Vậy A là CH4
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=2.\dfrac{11,2}{22,4}=1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=22,4\left(l\right)\)
Đúng 1
Bình luận (0)
Bài 5: Hãy tìm thể tích khí oxi đủ để đốt cháy hết 11,2 lít khí A.
Biết rằng:
- Khí A có tỉ lệ khối đối với không khí là 0,552.
- Thành phần theo khối lượng của khí A là: 75% C và 25% H.
Các thể tích khí đo ở đktc.
\(n_A=\dfrac{V\left(đktc\right)}{22,4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(d_{\dfrac{A}{kk}}=\dfrac{M_A}{M_{kk}}=\dfrac{M_A}{29}=0,552\)
⇒ \(M_A=16\) g/mol
Khối lượng của từng nguyên tố trong 1 mol khí A:
\(\left\{{}\begin{matrix}m_C=\dfrac{16.75}{100}=12g\\m_H=\dfrac{16.25}{100}=4g\end{matrix}\right.\)
Số mol của từng nguyên tố trong 1 mol khí A:
\(\left\{{}\begin{matrix}n_C=\dfrac{12}{12}=1mol\\n_H=\dfrac{4}{1}=4mol\end{matrix}\right.\)
⇒ \(CTHH:CH_4\)
Đúng 0
Bình luận (0)
Hãy tìm thể tích khí oxi đủ để đốt cháyheets 11,2 lít khí A
Biết rằng:
- Khí A có tỉ khối với không khí là 0,552.
- Thành phần theo khối lượng của khí A là: 75% C và 25% H.
Các thể tích khí đo ở đktc.
Khis A có tỉ khối so với khí hiđrô là 8. Thành phần theo khối lượng khí A là 75% Cacbon còn lại là Hidro. Hãy tìm thể tích không khi đủ để đốt cháy hoàn toàn 11,2 lít khí A. Biết trong không khi có chứa 20% là khí oxi (các thể tích đo ở dktc)
Gọi CTPT của A là CxHy.
Ta có: \(\dfrac{m_C}{m_H}=\dfrac{75\%}{25\%}\Rightarrow\dfrac{12n_C}{n_H}=\dfrac{75\%}{25\%}\Rightarrow\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
⇒ x:y = 1:4
→ A có CTPT dạng (CH4)n
Mà: \(M_A=8.2=16\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{16}{12+4}=1\)
→ CTPT của A là CH4.
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}=1\left(mol\right)\)
\(\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
\(\Rightarrow V_{kk}=5V_{O_2}=112\left(l\right)\)
Đúng 2
Bình luận (0)
Hãy tìm thể tích khí oxi đủ để đốt cháy hết 11,2 lít khi a biet rang:
-khí A có tỉ khối với không khí là0,552
-thành phần theo khối lượng của khí A là:75%Cva 25% H.
các thể tích khí do o dktc
ai giúp mình giải được bài này mình nguyện làm bạn gái của người đó (^_^)
Vì A có tỉ khối với không khí là 0,552
=> MA = 0,552 x 29 = 16 (g/mol)
Gọi công thức của A là CxHy
=> mC = \(\frac{16.75}{100}=12\left(gam\right)\)
=> nC = 12 / 12 = 1 (mol)
=> mH = 16 - 12 = 4 (gam)
=> nH = 4 / 1 = 4 (mol)
=> x : y = 1 : 4
=> Công thức hóa học của A: CH4
Đúng 0
Bình luận (0)
đốt 1,44g Mg trong bình đựng oxi
a) tính thể tích khí oxi cần dùng ( ở đktc)
b) nếu đốt cháy ngoài không khí thì thể tích không khí tối thiểu cần dùng ở đktc là bao nhiêu? Biết thể tích oxi bằng 1/5 thể tích không khí
c) tính khối lượng sản phẩm tạo thành sau phản ứng?
d) để có lượng oxi cần cho phản ứng trên thì nhiệt phân bao nhiêu KClO3?
nMg = 1.44/12 = 0.12 (mol)
2Mg + O2 -t0-> 2MgO
0.12....0.06..........0.12
VO2 = 0.06 * 22.4 = 1.344 (l)
Vkk= 5 VO2 = 1.344 * 5 = 6.72 (l)
mMgO = 0.12 * 40 = 4.8 (g)
2KClO3 -t0-> 2KCl + 3O2
0.08............................0.12
mKClO3 = 0.08 * 122.5 = 9.8 (g)
Đúng 2
Bình luận (0)
Đốt cháy hết 2,8 l khí A ta thu được khí CO2 và nước . Tính khối lượng nước và thể tích không khí cần dùng biết A nặng gấp 8 lần khí H2 và phần trăm theo khối lượng của C và H trong A là 75% và 25%; thể tích oxi chiếm 1/5 thể tích không khí( các khí ở đktc).
Đốt cháy 11,2 lít khí metan. Thể tích không khí cần dùng đế đốt cháy hết lượng metan trên là bao nhiêu (đktc)? Biết oxi chiếm 1/5 thể tích không khí. *
nCH4 =11,2/22,4 = 0,5 (mol)
PTHH CH4 + 2O2 -to-> CO2 + 2H2O
...........0,5.........1.............0,5............1
Vkk= 5. VO2 = 5. 22,4 .1 = 112 l
Đúng 3
Bình luận (0)
\(n_{CH_4}\)\(=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
\(0,5\) \(1\) \(\left(mol\right)\)
\(V_{O_2}=1.22,4=22,4\left(l\right)\)
\(V_{kk}=22,4:\dfrac{1}{5}=112\left(l\right)\)
Đúng 2
Bình luận (0)
























