Cho hỗn hợp gồm 18,56 gam Fe3O4 và 7,68 gam Cu vào 600 ml dung dịch HCl 1M, kết thúc phản ứng thu được dung dịch X và còn lại x gam rắn không tan. Giá trị của x là
A. 4,04
B. 3,84
C. 2,88
D. 2,56
Cho hỗn hợp gồm 18,56 gam Fe3O4 và 7,68 gam Cu vào 600 ml dung dịch HCl 1M, kết thúc phản ứng thu được dung dịch X và còn lại x gam rắn không tan. Giá trị của x là
A. 4,04
B. 3,84
C. 2,88
D. 2,56
PT : Fe3O4 + 8HCl + Cu => 3FeCl2 + CuCl2 + 4H2O
BĐ 0,08 0,6 0,12
Dư 0,005 0 0,45
mrắn không tan = mFe3O4 dư + mCu =4,04g
Cho hỗn hợp gồm 18,56 gam F e 3 O 4 và 7,68 gam Cu vào 600 ml dung dịch HCl 1M, kết thúc phản ứng thu được dung dịch X và còn lại x gam rắn không tan. Giá trị của x là
![]()
![]()
![]()
![]()
Cho hỗn hợp gồm Cu và Fe3O4 vào 500 ml dung dịch HC1 aM thu được dung dịch X và còn lại 2 gam chất rắn không tan. Cho dung dịch AgNO3 dư vào dung dịch X, kết thúc phản ứng thu được 0,03 mol khí NO (sản phẩm khử duy nhất) và 95,82 gam kết tủa. Giá trị của a là
A. 1,4
B. 1,6
C. 1,2
D. 1,8
Một hỗn hợp X gồm 0,2 mol Cu và 0,1 mol Fe3O4. Cho X vào 400 ml dung dịch H2SO4 1M. Sau khi phản ứng kết thúc thu được dung dịch A và còn lại x gam chất rắn B không tan. Cho dung dịch A tác dụng với dung dịch NaOH dư rồi đun nóng trong không khí cho các phản ứng xảy ra hoàn toàn. Lọc lấy kết tủa, nung đến khối lượng không đổi thu được y gam chất rắn C. Xác định giá trị của x và y.
Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
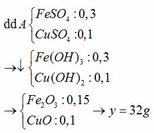
Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với dung dịch AgNO3 dư thu được 102,3 gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với
A. 22,7
B. 34,1
C. 29,1
D. 27,5
Cho 7,68 gam hỗn hợp gồm FeO, Fe2O3 và Fe3O4 tác dụng vừa hết với 260 ml dung dịch HCl 1M thu được dung dịch X. Cho X phản ứng với dung dịch NaOH dư thu được kết tủa Y. Nung Y ngoài không khí đến khối lượng không đổi thì thu được m (gam) chất rắn. Giá trị của m là
A. 7,6 gam
B. 8,0 gam
C. 9,6 gam
D. 11,2 gam
Đáp án B
Sơ đồ bài toán: F e O F e 2 O 3 F e 3 O 4 → H C l F e C l 2 F e C l 3 → N a O H F e ( O H ) 2 F e ( O H ) 3 → n u n g t r o n g k h ô n g k h í F e 2 O 3
Ta có : nH+ = nHCl = 0,26 mol.
0,26 0,13 mol
=> nO2−=0,13mol.Mà mFe + mO = 7,68 => mFe = 5,6 gam => nFe = 0,1 mol.
Bảo toàn nguyên tố Fe ta có 2 n F e = n F e 2 O 3 ⇒ n F e 2 O 3 = 0 , 05 mol
=> mFe2O3 = 0,05 . 160 = 8 gam.
Hoà tan m gam hỗn hợp gồm Cu và Fe3O4 trong dung dịch HCl dư, sau phản ứng còn lại 8,32 gam chất rắn không tan và dung dịch X. Cô cạn dung dịch X thu được 61,92 gam chất rắn khan. Giá trị của m là
A. 103,67
B. 43,84
C. 70,24
D. 55,44
Có các phản ứng sau:
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
Cu + 2FeCl3 → CuCl2 + 2FeCl2
Đặt n Fe3O4 = x mol
=> hỗn hợp muối gồm : x mol CuCl2 ; 3x mol FeCl2
Chất rắn còn dư chính là Cu.
=> m muối = 135x+127.3x =61,92 => x = 0,12 mol
=> m= m Fe3O4+ mCu = 232.0,12 + 64.0,12 + 8,32=43,84 g
=> B
Hoà tan m gam hỗn hợp gồm Cu và Fe3O4 trong dung dịch HCl dư, sau phản ứng còn lại 8,32 gam chất rắn không tan và dung dịch X. Cô cạn dung dịch X thu được 61,92 gam chất rắn khan. Giá trị của m là
A. 103,67
B. 43,84
C. 70,24
D. 55,44
Có các phản ứng sau:
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
Cu + 2FeCl3 → CuCl2 + 2FeCl2
Đặt n Fe3O4 = x mol
=> hỗn hợp muối gồm : x mol CuCl2 ; 3x mol FeCl2
Chất rắn còn dư chính là Cu. => m muối = 135x+127.3x =61,92
=> x = 0,12 mol
=> m= m Fe3O4+ mCu = 232.0,12 + 64.0,12 + 8,32=43,84 g => B
Hoà tan m gam hỗn hợp gồm Cu và Fe3O4 trong dung dịch HCl dư, sau phản ứng còn lại 8,32 gam chất rắn không tan và dung dịch X. Cô cạn dung dịch X thu được 61,92 gam chất rắn khan. Giá trị của m là:
A. 70,24
B. 55,44
C. 103,67.
D. 43,84
Đáp án : D
Do sau phản ứng có chất rắn => Cu dư và sau phản ứng dung dịch có FeCl2 ; CuCl2
Fe3O4 + 8HCl à FeCl2 + 2FeCl3 + 4H2O
x à x à 2x
Cu + 2FeCl3 à CuCl2 + 2FeCl2
x ß 2x à x à 2x
=> m muối = m FeCl2 + m CuCl2 => 61,92g = 3x.127 + x.135 => x = 0,12mol
=> m = mFe3O4 + mCu pứ + mCu dư = 43,86g