Cho 22 gam dd NaOH 10% vào 5 gam dd axit H3PO4 39,2%. Muối thu được sau phản ứng là:
A. Na2HPO4 và NaH2PO4
B. Na2HPO4.
C. NaH2PO4.
D. Na3PO4 và Na2HPO4.
Cho 0,2 mol H3PO4 tác dụng với dung dịch chứa 0,5 mol NaOH, sau phản ứng thu được muối gì khối lượng bao nhiêu?
A.11,8g NaH2P04
B.14,2g Na2HPO4 và 16,4g Na3PO4
C.11,8g NaH2PO4 và 16,4g Na3PO4
D.11,8g NaH2PO4 và 14,2g Na2HPO4
T =\(\frac{0,5}{0,2}\) = 2,5 \(\rightarrow\)Na2HPO4 và Na3PO4
2NaOH + H3PO4\(\rightarrow\) Na2HPO4 + 2H2O
2x ________x________x
3NaOH + H3PO4\(\rightarrow\) Na3PO4 + 3H2O
3y______y _________ y
\(\left\{{}\begin{matrix}\text{2x + 3y = 0,5}\\\text{ x + y =0,2 }\end{matrix}\right.\rightarrow x=y=0,1\)
m Na2HPO4 = 142 . 0,1 = 14,2 (g)
m Na3PO4 = 164 . 0,1 = 16,4 (g)
Cho a mol axit H3PO3 vào dung dịch chứa 2,4a mol NaOH thu được dung dịch X. Vậy dung dịch X chứa những chất tan gì?
A. Na3PO4 và NaOH B. Na3PO4 và Na2HPO4 C. Na2HPO4 và NaH2PO4 D. NaH2PO4 và H3PO4
nOH- = 2,4a(mol)
nH3PO4= a(mol)
=> 2< nOH-/nH3PO4= 2,4a/a=2,4<3
=> Sp thu được hỗn hợp 2 muối : Na3PO4 và Na2HPO4
=> Chọn B
Chúc em học tốt!
Rót 300ml dung dịch NaOH 1M vào 200 ml dung dịch H3PO4 1M .Sau phản ứng trong dung dịch tồn tại muối nào, khối lượng đứng bao nhiêu?
A.11g NaH2PO4 và 14,2 g Na2HPO4
B.12g NaH2PO4 và 14,2 g Na2HPO4
C.14,2 g Na2HPO4 và 16,4g Na3PO4
D.14,2g NaH2PO4 và 12 g Na2HPO4
Cho các chất sau : NaOH, H 3 PO 4 , NaH 2 PO 4 , Na 2 HPO 4 , Na 3 PO 4 . Trộn các chất trên với nhau theo từng đôi, số cặp xảy ra phản ứng là
A. 4.
B. 5.
C. 7.
D. 6.
Đáp án D
Trộn các chất trên với nhau theo từng đôi, số cặp xảy ra phản ứng là 6
Cho các chất sau : N a O H , H 3 P O 4 , N a H 2 P O 4 , N a 2 H P O 4 , N a 3 P O 4 . Trộn các chất trên với nhau theo từng đôi, số cặp xảy ra phản ứng là
A. 4
B. 5
C. 7
D. 6
Cho m gam P2O5 vào 300ml dung dịch NaOH 2M thì dung dịch sau phản ứng chỉ chứa 2 muối NaH2PO4 và Na2HPO4 có nồng độ mol bằng nhau. Giá trị của m là?
Cho 100g dung dịch H3PO4 39,2% tác dụng với 100g dung dịch NaOH 25% thu được dung dịch A. Tính nồng độ phần trăm các chất trong A.
Bài giải:
Ta có: nH3PO4 = 3,92:98=0,4(mol); nNAOH=25:40=0,625(mol)
Như vậy nH3PO4<nNaOH<2nH3PO4
Nên xảy ra các phản ứng sau:
H3PO4+NaOH->NaH2PO4+H2O (1)
NaH2PO4+NaOH->Na2HPO4+H2O (2)
Thu được dd chứa x mol NaH2PO4 và y mol Na2HPO4
Số mol nguyên tử Na trong hh muối bằng số mol Na trong NaOH, nên x+2y=0,625 (a)
Số mol PO4 trong hh muối bằng số mol PO4 trong lượng axit ban đầu :x+y=0,04(b)
Giải hpt (a) và (b) ta được:
y=0,225 và x=0,175
Mà mdd sau p/ứ thu đc =100+100=200g
Vậy C% của NaH2PO4=(120x0,175)/200x100%=10,5%
C% của Na2HPO4=142x0,225/200x100%=15,975%
Trong sách của mình giải như thế này nhưng mình không hiểu chỗ mình in đậm, bạn nào có cách giải dễ hiểu hơn cho mình tham khảo với. Với lại các bạn giải thích dùm mình chỗ in đậm luôn nha! Cảm ơn bạn nhìu :D
Axit H3PO4 là axit 3 nấc nên phản ứng với NaOH có thể xảy ra 3 phương trình như sau
H3PO4 +3NaOH =>Na3PO4 +3H2O
H3PO4 +2NaOH =>Na2HPO4 +2H2O
H3PO4+NaOH =>NaH2PO4 +H2O
Xét tỉ lệ mol NaOH/mol H3PO4=T
Nếu T=1=>chỉ tạo muối NaH2PO4 Tương tự với T=2;T=3
ở đây đbài của bạn là 0,625/0,4=1,5625 T nằm giữa khoảng 1 và 2 nên sẽ ra 2 muối NaH2PO4 và Na2HPO4
Pt đó không sai nhưng nếu bạn chưa học về dung dịch điện li thì hãy viết 2NaOH+H3PO4 đặt ẩn giải hpt cho đỡ rối
Vậy là ở pt (2) không phải là NaH2PO4+NaOH-> Na2HPO4+H2O như trong sách đã ghi mà phải là H3PO4 + 2NaOH->Na2HPO4+2H2O đúng không ạ ![]()
Đốt cháy hoàn toàn m gam hợp chất X của photpho cần m 17 mol oxi, sau phản ứng chỉ thu được P2O5 và 13 , 5 m 17 gam H2O. Cho toàn bộ sản phẩm cháy vào 125 gam dung dịch NaOH 16% thu được dung dịch B chỉ chứa hai muối NaH2PO4 và Na2HPO4 có nồng độ phần trăm bằng nhau. Giá trị của m là
A. 24,35
B. 11,66
C. 13,6
D. 11,9
Đáp án B.
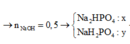
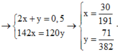
→ n P 2 O 5 = 131 764
→ B T K L m + m 17 . 32 → m = 11 , 66
Đốt cháy hoàn toàn m gam hợp chất X của photpho cần m 17 mol oxi, sau phản ứng chỉ thu được P2O5 và 13 , 5 m 17 gam H2O. Cho toàn bộ sản phẩm cháy vào 125 gam dung dịch NaOH 16% thu được dung dịch B chỉ chứa hai muối NaH2PO4 và Na2HPO4 có nồng độ phần trăm bằng nhau. Giá trị của m là
A. 24,35.
B. 11,66.
C. 13,6.
D. 11,9.