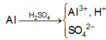
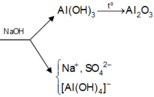
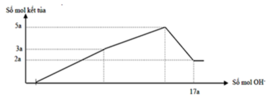
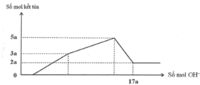
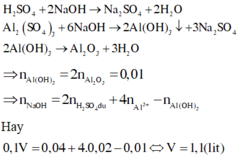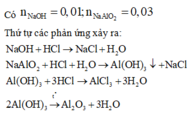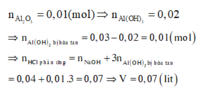Hoà tan 0,54 gam Al trong 0,5 lít dung dịch H2SO4 0,1M, thu được dung dịch X. Thêm V lít dung dịch NaOH 0,1M cho đến khi kết tủa tan một phần. Nung kết tủa thu được đến khối lượng không đổi ta được chất rắn nặng 0,51 gam. V có giá trị là
A. 1,1.
B. 0,8.
C. 1,2.
D. 1,5.