H2O2 thể hiện là chất oxi hóa trong phản ứng với chất nào dưới đây ?
A. dung dịch KMnO4
B. dung dịch H2SO3
C. MnO2
D. O3
Chất nào trong 4 chất dưới đây có thể tham gia cả 4 phản ứng: phản ứng cháy trong oxi; phản ứng cộng với brom; phản ứng cộng với H 2 (chất xúc tác Ni, nhiệt độ); phản ứng-với dung dịch A g N O 3 trong amoniac ?
A. etan;
B. eten;
C. axetilen;
D. xiclopropan.
5: Phản ứng nào dưới đây là phản ứng hóa hợp?
A. CuO + H2_10> Cu +H2O
B. CO2 + Ca(OH)21° > CaCO3 + H2O
C. 2KMnO4 10 KMnO4 + MnO2 + O2
D. CaO + H200 Ca(OH)2
Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 .
B. KMnO4 và H2O.
C. KClO3 và CaCO3 .
D. KMnO4 và không khí.
Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit?
A. CuO, CaCO3, SO3
B. N2O5 ; Al2O3 ; SiO2
C. FeO; KC1, P2O5
D. CO2 ; H2SO4; MgO
Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá là
A. 4NH3 + 502 + 4NO + 6H2O
B. Na2O + H2O → 2NaOH
C. CaCO3 +CaO + CO2
D. Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Câu 9: Đốt cháy hoàn toàn 2,4 gam Mg trong khí oxi dư thu được khối lượng MgO làm
A. 4 gam.
B. 4,3 gam.
C. 4,6 gam.
D. 4.9 gam.
Câu 10: Khối lượng KMnO4 cần dùng để điều chế 1,12 lít khí oxi là
A. 7,9 gam.
B. 15,8 gam.
C. 3,95 gam.
D. 14,2 gam.
Câu 11: Người ta không nên dùng nước để dập tắt đám cháy bằng xăng dầu vì
A. xăng dầu không tan trong nước, nhẹ hơn nước.
B. xăng dầu cháy mạnh trong nước.
C. xăng dầu nặng hơn nước.
D. xăng dầu cháy mạnh hơn khi có nước.
Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 5,6 lít khí oxi thu được khối lượng P2O5 là
A.9,1 gam. B. 8,1 gam. C. 7,1 gam. D. 6,1 gam.
5: Phản ứng nào dưới đây là phản ứng hóa hợp?
A. CuO + H2_10> Cu +H2O
B. CO2 + Ca(OH)21° > CaCO3 + H2O
C. 2KMnO4 10 KMnO4 + MnO2 + O2
D. CaO + H200 Ca(OH)2
Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 .
B. KMnO4 và H2O.
C. KClO3 và CaCO3 .
D. KMnO4 và không khí.
Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit?
A. CuO, CaCO3, SO3
B. N2O5 ; Al2O3 ; SiO2
C. FeO; KC1, P2O5
D. CO2 ; H2SO4; MgO
Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá là
A. 4NH3 + 502 + 4NO + 6H2O
B. Na2O + H2O → 2NaOH
C. CaCO3 +CaO + CO2
D. Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Câu 9: Đốt cháy hoàn toàn 2,4 gam Mg trong khí oxi dư thu được khối lượng MgO làm
A. 4 gam.
B. 4,3 gam.
C. 4,6 gam.
D. 4.9 gam.
Câu 10: Khối lượng KMnO4 cần dùng để điều chế 1,12 lít khí oxi là
A. 7,9 gam.
B. 15,8 gam.
C. 3,95 gam.
D. 14,2 gam.
Câu 11: Người ta không nên dùng nước để dập tắt đám cháy bằng xăng dầu vì
A. xăng dầu không tan trong nước, nhẹ hơn nước.
B. xăng dầu cháy mạnh trong nước.
C. xăng dầu nặng hơn nước.
D. xăng dầu cháy mạnh hơn khi có nước.
Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 5,6 lít khí oxi thu được khối lượng P2O5 là
A.9,1 gam. B. 8,1 gam. C. 7,1 gam. D. 6,1 gam.
Có những chất sau: KMnO4, MnO2, K2Cr2O7 và dung dịch HCl.
a) Nếu các chất oxi hóa có khối lượng bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn?
b) Nếu chất oxi hóa có số mol bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn?
Hãy trả lời bằng cách tính toán trên cơ sở của các phương trình phản ứng.
a) Giả sử lấy lượng mỗi chất là a gam
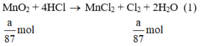
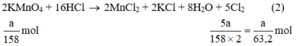
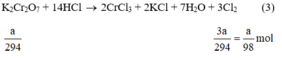
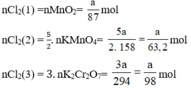
Ta có: 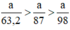
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 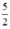 . nKMnO4 = 2,5a mol
. nKMnO4 = 2,5a mol
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.
Cho các phương trình phản ứng:
1) dung dịch FeCl2 + dung dịch AgNO3 dư →
2 ) Hg + S →
3 ) F2 + H2O →
4) NH4Cl + NaNO2 đun nóng →
5) K + H2O →
6) H2S + O2 dư đốt →
7) SO2 + dung dịch Br2 →
8) Mg + dung dịch HCl →
9) Ag + O3 →
10) KMnO4 nhiệt phân →
11) MnO2 + HCl đặc →
12) dung dịch FeCl3 + Cu →
Trong các phản ứng trên, số phản ứng tạo đơn chất là
A. 9
B. 6
C. 7
D. 8
Đáp án D
1) dung dịch FeCl2 + dung dịch AgNO3 dư →Tạo đơn chất Ag
2 ) Hg + S → Không
3 ) F2 + H2O → Tạo đơn chất O2
4) NH4Cl + NaNO2 đun nóng → Tạo đơn chất N2
5) K + H2O → Tạo đơn chất H2
6) H2S + O2 dư đốt → Không
7) SO2 + dung dịch Br2 →Không
8) Mg + dung dịch HCl → Tạo đơn chất H2
9) Ag + O3 → Tạo đơn chất O2
10) KMnO4 nhiệt phân →Tạo đơn chất O2
11) MnO2 + HCl đặc → Tạo đơn chất Cl2
12) dung dịch FeCl3 + Cu →Không
Hình vẽ sau đây mô tả quá trình điều chế dung dịch X trong phòng thí nghiệm
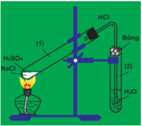
Trong điều kiện thích hợp, dung dịch X có thể phản ứng được với bao nhiêu chất trong số các chất sau: CuS, NaHCO3, KMnO4, KNO3, Cu, Ag, MnO2, KClO3, Fe3O4, Al có sinh ra khí:
A. 4
B. 7
C. 6
D. 5
Đáp án C
Định hướng tư duy giải
Từ mô hình điều chế X là HCl
Các chất thỏa mãn: NaHCO3; KMnO4; MnO2; KClO3; FeS2; Al
Hình vẽ sau đây mô tả quá trình điều chế dung dịch X trong phòng thí nghiệm
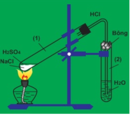
Trong điều kiện thích hợp, dung dịch X có thể phản ứng được với bao nhiêu chất trong số các chất sau: CuS, NaHCO3, KMnO4, KNO3, Cu, Ag, MnO2, KClO3, Fe3O4, Al có sinh ra khí:
A. 4
B. 7
C. 6
D. 5
Đáp án C
Định hướng tư duy giải
Từ mô hình điều chế ↦ X là HCl
Các chất thỏa mãn: NaHCO3; KMnO4; MnO2; KClO3; FeS2; Al
Hình vẽ sau đây mô tả quá trình điều chế dung dịch X trong phòng thí nghiệm
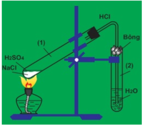
Trong điều kiện thích hợp, dung dịch X có thể phản ứng được với bao nhiêu chất trong số các chất sau: CuS, NaHCO3, KMnO4, KNO3, Cu, Ag, MnO2, KClO3, Fe3O4, Al có sinh ra khí:
A. 4
B. 7
C. 6
D. 5
Đáp án C
Định hướng tư duy giải
Từ mô hình điều chế X là HCl
Các chất thỏa mãn: NaHCO3; KMnO4; MnO2; KClO3; FeS2; Al
Cho các phản ứng sau:
(a) SiO2 + dung dịch HF ®
(b) Si + dung dịch NaOH ®
(c) FeO + Co → t o
(d) O3 + KI + H2O ®
(e) C u N O 3 3 → t o
(g) K M n O 4 → t o
Số phản ứng sinh ra đơn chất là
A. 4.
B. 6.
C. 5.
D. 3.
Cho những chất sau: CuO, dung dịch HCl, H2, MnO2. Cho biết chất oxi hóa, chất khử, sự oxi hóa và sự khử trong những phản ứng hóa học nói trên.
Trong phản ứng (1):
- Nguyên tử hiđro nhường electron là chất khử, sự nhường electron của H2 được gọi là sự oxi hóa nguyên tử hiđro.
- Ion Cu nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Trong phản ứng (2):
- Ion Clo nhường electron là chất khử. Sự nhường electron của Cl- được gọi là sự oxi hóa ion Clo.
- Ion Mn nhận electron là chất oxi hóa. Sự nhận electron của ion Mn được gọi là sự khử ion Mn.