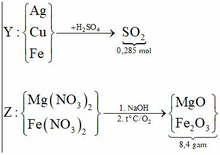
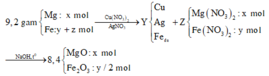
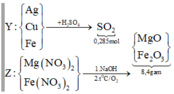
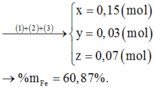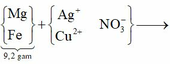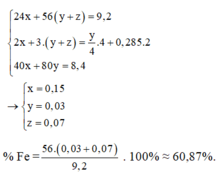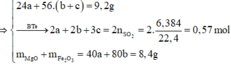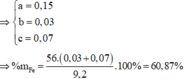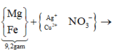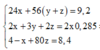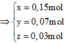Cho 9,2 gam hỗn hợp X gồm Mg và Fe cho vào dung dịch A g N O 3 và C u N O 3 2 được chất rắn Y gồm 3 kim loại và dung dịch . Hòa tan hết Y bằng dung dịch H 2 S O 4 đặc nóng thu được 6,384 lít S O 2 (đktc) – sản phầm khử duy nhất. Cho NaOH dư vào Z thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi thu được 8,4 gam hỗn hợp rắn khan. Các phản ứng xảy ra hoàn toàn . % khối lượng Fe ban đầu là
A. 57,23%
B. 60,87%
C. 62,35%
D. 65,24%