Hòa tan 0,9 gam một kim loại M (hóa trị không đổi) vào dung dịch H N O 3 dư, thu được 0,28 lít (đktc) khí N 2 O duy nhất. Kim loại M là
A. Mg
B. Zn
C. Al
D. Ag
Gọi hóa trị của M là n.
Ta có: \(n_{H_2}=\dfrac{5,376}{22,4}=0,24\left(mol\right)\)
PT: \(2M+nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nH_2\)
Theo PT: \(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,48}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{15,6}{\dfrac{0,48}{n}}=\dfrac{65}{2}n\left(g/mol\right)\)
Với n = 2 thì MM = 65 (g/mol)
Vậy: M là Zn.
Hòa tan hoàn toàn 7,15 gam kim loại M hóa trị 2 vào lượng dư dung dịch HNO3 loãng, thu được 0,448 lít(đktc) hỗn hợp 2 khí không màu, không hóa nâu trong không khí (số mol hai khí bằng nhau) và dung dịch chứa 21,19 gam muối. Kim loại M là:
A. Fe
B. Ca
C. Mg
D. Zn
2 khí không màu, không hóa nâu trong không khí và là sản phẩm khử của N+5 chỉ có thể là N2 và N2O
-TH1: 21,19 gam muối không có muối NH4NO3
Theo bảo toàn nguyên tố M ta có: nM= nM(NO3)2
→ m M m M ( N O 3 ) 2 = M M M M ( N O 3 ) 2 → 7 , 15 21 , 19 = M M + 62 , 2
→M= 63,148 Loại
Do đó trường hợp này loại
-TH2: 21,19 gam muối có muối NH4NO3
QT cho e:
M → M2++ ne (1)
7,15/M 7,15.2/M
QT nhận e : nkhí= 0,02 mol. Mà số mol hai khí bằng nhau nên n N 2 O = n N 2 =0,01mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,08 0,1 ← 0,01 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (3)
0,1 0,12← 0,01 mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (4)
8x xmol
Đặt số mol muối NH4+ là x mol
Theo ĐL BT e: ne cho= ne nhận nên 7,15.2/M= 0,08 + 0,1+8x (*1)
Mặt khác : mmuối= mM(NO3)2+ mNH4NO3= 7,15/M. (M+124)+80x= 21,19 (*2)
Từ (*1) và (*2) ta có: x= 5.10-3 và M=65. M là Zn
Đáp án D
Hòa tan 12 gam hỗn hợp gồm Fe và một kim loại M hóa trị II vào dung dịch H2SO4 dư thu được 4,48 lít H2 (đktc). Nếu hòa tan 23,8 gam kim loại M vào dung dịch chứa 0,7 mol HCl thì M không tan hết. Tìm M
\(n_{Fe} = a(mol) ; n_M = b(mol)\\ \Rightarrow 56a + Mb = 12\)
\(Fe + 2HCl \to FeCl_2 + H_2\\ M + 2HCl \to MCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{4,48}{22,4} = 0,2(mol)\\ \Rightarrow a = 0,2 - b ( 0< b < 0,2)\)
Suy ra:
56(0,2 - b) + Mb = 12
\(\Rightarrow M = \dfrac{0,8 + 56b}{b}\)
Vì 0 < b < 0,12
Nên M > 62,67(1)
Mặt khác,
\(n_M > \dfrac{1}{2}n_{HCl} = 0,35\\ \Rightarrow M < \dfrac{23,8}{0,35} = 68(2)\)
Từ (1)(2) suy ra: 62,67 < M < 68
Do đó, M = 65(Zn) thì thỏa mãn
Vậy M là Zn(Kẽm)
Hòa tan hoàn toàn m gam hỗn hợp E gồm Sn và một kim loại R (có hóa trị không đổi) trong lượng dư dung dịch HCl, thu được 5,04 lít khí H2 (đktc) và dung dịch chứa 36,27 gam muối. Mặt khác, để đốt cháy cũng m gam hỗn hợp E cần vừa đủ 3,696 lít O2 (đktc). Kim loại R là
A. Al
B. Zn
C. Ca
C. Ca
Gọi hóa trị của R là n và số mol Sn và R lần lượt là a và b mol
+/ Khi phản ứng với HCl :
Sn + HCl → SnCl2 + H2
R + nHCl → RCln + 0,5nH2
+/ Khi đốt trong oxi :
Sn + O2 → SnO2
2R + 0,5nO2 → R2On
=> Ta có : nH2 = a + 0,5nb = 0,225 mol
Và nO2 = a + 0,25nb = 0,165 mol
=> a = 0,105 mol ; nb = 0,24 mol
Có mmuối = 0,105.190 + 0,24/n . (R + 35,5n) = 36,27
=>R = 32,5n
=>Cặp n =2 ; R =65 (Zn) thỏa mãn
=>B
Cho 16,2 gam kim loại M hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng hòa tan hoàn toàn vào dung dịch H2SO4 đặc nóng dư thu được 3,36 lít khí SO2 (đktc) và 4,8 gam S. Xác định kim loại M
Ta có: \(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Coi hh chất rắn gồm M và O.
⇒ nO = 0,15.2 = 0,3 (mol)
Ta có: \(n_M=\dfrac{16,2}{M_M}\left(mol\right)\)
BT e, có: n.nM = 2nO + 2nSO2 + 6nS
\(\Rightarrow\dfrac{16,2n}{M_M}=1,8\Rightarrow M_M=9n\left(g/mol\right)\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
Vậy: M là Al.
Hòa tan hoàn toàn 7,15 gam kim loại M vào lượng dư dung dịch HNO3 loãng, thu được 0,448 lít (đktc) hỗn hợp 2 khí không màu, không hóa nâu trong không khí và dung dịch chứa 21,19 gam muối. Kim loại M là
A. Fe
B. Al
C. Ag
D. Zn
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
Cho 41,68 gam hỗn hợp F gồm Fe3O4 và kim loại M vào dung dịch HNO3 50,4% đun nóng khuấy đều hỗn hợp để phản ứng xảy ra hoàn toàn thu được 4,032 lít NO2 (đktc), dung dịch G và 17,28 gam kim loại M. Cho dung dịch NaOH dư vào dung dịch G thu được kết tủa K. Nung K trong không khí đến khối lượng không đổi thu được 24,72 gam chất rắn R. Biết M có hóa trị không đổi trong các phản ứng trên, khí NO2 là sản phẩm khử duy nhất của N+5. Khối lượng dung dịch HNO3 50,4% tối thiểu để hòa tan hoàn toàn 41,68 gam hỗn hợp F là
A. 85,0 gam
B. 112,5 gam
C. 125,0 gam
D. 95,0 gam
Cho 41,68 gam hỗn hợp F gồm Fe3O4 và kim loại M vào dung dịch HNO3 50,4% đun nóng khuấy đều hỗn hợp để phản ứng xảy ra hoàn toàn thu được 4,032 lít NO2 (đktc), dung dịch G và 17,28 gam kim loại M. Cho dung dịch NaOH dư vào dung dịch G thu được kết tủa K. Nung K trong không khí đến khối lượng không đổi thu được 24,72 gam chất rắn R. Biết M có hóa trị không đổi trong các phản ứng trên, khí NO2là sản phẩm khử duy nhất của N+5. Khối lượng dung dịch HNO350,4% tối thiểu để hòa tan hoàn toàn 41,68 gam hỗn hợp F là
A. 112,5 gam
B. 95,0 gam
C. 85,0 gam
D. 125,0 gam
Đáp án D
TH1 : Nếu M là Cu → Oxit R 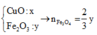
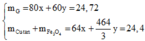
→ vô nghiệm
TH2 : Nếu M là Ag
