hợp chất khí đối với hidro có một nguyên tử r có dạng rh2 õit cao nhất của nguyên tố r chứa 40% khối lượng của R. vậy công thức oxit cao nhất là

Những câu hỏi liên quan
Hợp chất của một nguyên tố có công thức RH2 . Oxit cao nhất của R chứa 40% khối lượng R . Vậy R là ?
CTHH: RH2 => R có hoá trị cao nhất là VI
=> CTHH R hoá trị cao nhất với O: RO3
\(V\text{ì}:\%m_{\dfrac{R}{RO_3}}=40\%\\ \Leftrightarrow\dfrac{M_R}{M_R+48}=40\%\\ \Leftrightarrow M_R-0,4M_R=19,2\\ \Leftrightarrow M_R=\dfrac{19,2}{0,6}=32\left(\dfrac{g}{mol}\right)\\ \Rightarrow R:L\text{ưu}.hu\text{ỳ}nh\left(S=32\right)\)
Đúng 0
Bình luận (0)
Oxit cao nhất của một nguyên tố có dạng R2O5 . Hợp chất khí với hidro của nguyên tố R có công thức phân tử là: * 4 điểm RH2 RH3 RH4 RH
1. Hợp chất khí với hidro của nguyên tố có công thức RH2. Oxit cao nhất của R có chứa 60% oxi về khối lượnga) Tìm nguyên tố Rb) Cho 16g oxit cao nhất của R vào 144g H2O được ddX. tính C% của ddXc) Nếu cho 12g oxit cao nhất của R vào 88g dd H2SO4 10% được ddY. Tính C% ddYd) Để trung hòa ddX phải dùng bao nhiêu ml dd( KOH 1M ; Ba(OH)2 0.5M ).
Đọc tiếp
1. Hợp chất khí với hidro của nguyên tố có công thức RH2. Oxit cao nhất của R có chứa 60% oxi về khối lượng
a) Tìm nguyên tố R
b) Cho 16g oxit cao nhất của R vào 144g H2O được ddX. tính C% của ddX
c) Nếu cho 12g oxit cao nhất của R vào 88g dd H2SO4 10% được ddY. Tính C% ddY
d) Để trung hòa ddX phải dùng bao nhiêu ml dd( KOH 1M ; Ba(OH)2 0.5M ).
1. Hợp chất khí với hidro của nguyên tố có công thức RH2. Oxit cao nhất của R có chứa 60% oxi về khối lượnga) Tìm nguyên tố Rb) Cho 16g oxit cao nhất của R vào 144g H2O được ddX. tính C% của ddXc) Nếu cho 12g oxit cao nhất của R vào 88g dd H2SO4 10% được ddY. Tính C% ddYd) Để trung hòa ddX phải dùng bao nhiêu ml dd( KOH 1M ; Ba(OH)2 0.5M ).
Đọc tiếp
1. Hợp chất khí với hidro của nguyên tố có công thức RH2. Oxit cao nhất của R có chứa 60% oxi về khối lượng
a) Tìm nguyên tố R
b) Cho 16g oxit cao nhất của R vào 144g H2O được ddX. tính C% của ddX
c) Nếu cho 12g oxit cao nhất của R vào 88g dd H2SO4 10% được ddY. Tính C% ddY
d) Để trung hòa ddX phải dùng bao nhiêu ml dd( KOH 1M ; Ba(OH)2 0.5M ).
5. Hợp chất khí với hiđro của R có dạng RH2, oxit cao nhất của nguyên tố này có 50% oxi về khối lượng.
a. Tìm tên nguyên tố R?
b. Viết công thức oxit cao nhất và hợp chất khí với hiđro của R?
Hợp chất của một nguyên tố có công thức R H 2 . Oxit cao nhất của R chiếm 40% khối lượng R. R là:
A. N (M = 14)
B. Se (M = 79).
C. S (M = 32)
D. Ca (M = 40)
Chọn C
Oxit cao nhất của R có dạng R O 3 . Theo bài ra có:
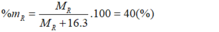
→ R = 32. Vậy R là lưu huỳnh (S).
Đúng 0
Bình luận (0)
Nguyên tố R có công thức hợp chất khí với Hidro là RH3. Trong công thức oxit cao nhất của nó có chứa 56,34% Oxi về khối lượng. Xác định nguyên tố R; công thức hợp chất khí với Hidro; hợp chất với oxi.
Gọi CTHH của R với oxi là: R2O3
Theo đề, ta có: \(\%_{O_{\left(R_2O_3\right)}}=\dfrac{16.3}{NTK_R.2+16.3}.100\%=56,34\%\)
=> \(NTK_R\approx19\left(đvC\right)\)
=> R là flo (F)
=> CTHH của R và H là: FH3
CTHH của R và O là: F2O3
Đúng 0
Bình luận (0)
a. Hợp chất khí với Hidro của nguyên tố R có công thức là RH 3 . Trong hợp chất oxit cao nhấtcủa R có chứa 43,66% R về khối lượng. Hãy xác định nguyên tố R? (cho: Si 28 ; N14;S32; P 31)b. Hợp chất oxit cao nhất của nguyên tố R có công thức là R 2 O 5 . Trong hợp chất khí với Hidrocó chứa 8,82% H về khối lượng. Hãy xác định nguyên tố R? Viết công thức oxit cao nhất vàcông thức hidroxit (cho: Si 28 ; N14; S32; P 31)c. Hợp chất khí với hiđro của nguyên tố R là RH 4 . Trong oxit cao nhất của R c...
Đọc tiếp
a. Hợp chất khí với Hidro của nguyên tố R có công thức là RH 3 . Trong hợp chất oxit cao nhất
của R có chứa 43,66% R về khối lượng. Hãy xác định nguyên tố R? (cho: Si = 28 ; N=14;
S=32; P = 31)
b. Hợp chất oxit cao nhất của nguyên tố R có công thức là R 2 O 5 . Trong hợp chất khí với Hidro
có chứa 8,82% H về khối lượng. Hãy xác định nguyên tố R? Viết công thức oxit cao nhất và
công thức hidroxit (cho: Si = 28 ; N=14; S=32; P = 31)
c. Hợp chất khí với hiđro của nguyên tố R là RH 4 . Trong oxit cao nhất của R có 53,3 % oxi về
khối lượng. Tìm R. (Cho: C=12; Si = 28 ; N=14; S=32)
Hợp chất khí với hidro của một nguyên tố là RH3. Oxit cao nhất của nó chứa 43,66% R về khối lượng. Công thức oxit cao nhất của R A. N2O5 B. P2O5 C. N2O3 D. CO2
Đọc tiếp
Hợp chất khí với hidro của một nguyên tố là RH3. Oxit cao nhất của nó chứa 43,66% R về khối lượng. Công thức oxit cao nhất của R
A. N2O5
B. P2O5
C. N2O3
D. CO2
Đáp án B
Vì công thức khí với hidro của R là RH3
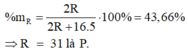
Vậy công thức oxit cao nhất của R là P2O5.
Đúng 0
Bình luận (0)

















