Quan sát hình 4.4, cho biết ở điều kiện chuẩn (áp suất 1 bar và nhiệt độ 25 oC), thể tích 1 mol khí là bao nhiêu.

Quan sát hình 4.4, cho biết ở điều kiện chuẩn (áp suất 1 bar và nhiệt độ 25 oC), thể tích 1 mol khí là bao nhiêu.

Ở điều kiện chuẩn (áp suất 1 bar và nhiệt độ 25oC), thể tích 1 mol khí là 24,79 lít.
1 mol khí ở đkc (1bar, 25oC) có thể tích 24,79 lít
Một bình chứa một lượng khí ở nhiệt độ 30o C và áp suất 2 bar. (1 bar = 105 Pa). Hỏi phải tăng nhiệt độ lên tới bao nhiêu độ để áp suất tăng gấp đôi?
Trạng thái 1: T1 = t1 + 273 = 303 K; P1 = 2 bar
Trạng thái 2: P2 = 4 bar ; T2 = ?
Áp dụng định luật Sác-lơ cho quá trình biến đổi đẳng tích, ta có:
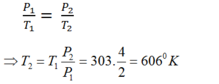
Một bình chứa một lượng khí ở nhiệt độ 30 ° C và áp suất 2 bar. ( 1 b a r = 10 5 P a ). Hỏi phải tăng nhiệt độ lên tới bao nhiêu độ để áp suất tăng gấp đôi ? Xem thể tích bình chứa luôn không đổi.
A. 333 ° C
B. 606 ° C
C. 60 ° C
D. 303 ° C
+ Ta có:
![]()
+ Vì bình chứa có thể tích không đổi nên theo định luật Sác-lơ (quá trình đẳng tích) ta có:
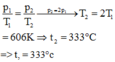
=> Chọn A.
Một bình chứa một lượng khí ở nhiệt độ 30 độ C và áp suất 2 bar ( 1 bar = 105 Pa ) . Hỏi phải tăng nhiệt độ lên tới bao nhiêu độ để áp suất tăng gấp đôi.
Ta có : T1 = toC + 273 = 30 + 273 = 303oK
p1 = 2 bar = 2 . 105 Pa
p2 = 4 bar = 4 . 105
Vì quá trình là đẳng tích , áp dụng định luật Charles ta có
\(\frac{p_1}{p_2}=\frac{T_1}{T_2}\)→ T2 = \(\frac{p_2.T_1}{p_1}=\frac{4.10^5.303}{2.10^5}\)= 606oK
Vậy để áp suất tăng lên gấp đôi , ta phải tăng nhiệt độ lên 606oK
* Trạng thái 1: T1 = 273 + 30 = 303 K
p1 = 2 bar
* Trạng thái 2: T2 = ? p2 = 2p1
* Vì thể tích bình không đổi nên:
\(\frac{P1}{T1}=\frac{P2}{T2}\Rightarrow T2=\frac{P2.T1}{P1}=\frac{2P1.T1}{P1}\) = 2T1 = 606 K
một lượng chứa một lượng khí ở nhiệt độ 30oC và áp suất 2 bar . (1 bar = 105 Pa) . Hỏi phải tăng nhiệt độ lên tới bao nhiêu độ để áp suất tăng gấp đôi ?
t = 30*C => T = 303K
Quá trình đẳng tích thì áp suất tỉ lệ thuận với nhiệt độ.
Áp suất tăng gấp đôi thì nhiệt độ tăng gấp đôi => T' = 2T = 606K
=> t' = 606 - 273 = 333*C
Một bình chứa một lượng khí ở nhiệt độ 30oC và áp suất 2 bar. (1 bar = 105 Pa). Hỏi phải tăng nhiệt độ lên tới bao nhiêu độ để áp suất tăng gấp đôi?
Bài giải:
* Trạng thái 1: T1 = 273 + 30 = 303 K
p1 = 2 bar
* Trạng thái 2: T2 = ? p2 = 2p1
* Vì thể tích bình không đổi nên:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow T_2=\dfrac{p_2.T_1}{p_1}=\dfrac{2p_1.T_1}{p_1}=2T_1=606k\)
Một chiếc lốp ô tô chứa không khí có áp suất 5 bar ( 1 b a r = 10 5 P a ) và nhiệt độ 25 ° C . Khi xe chạy nhanh lốp xe nóng lên làm cho nhiệt độ không khí trong lốp tăng lên tới 50 ° C . Áp suất của không khí trong lốp xe lúc này gần nhất với giá trị nào sau đây?
A. 10 bar
B. 5,42 bar
C. 4,61 bar
D. 2,5 bar
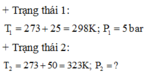
+ Áp dụng định luật Sác – lơ cho quá trình biến đổi đẳng tích:
![]()
=> Chọn B.
Hãy tính số mol có trong:
a) 28 gam Fe
b) 13,5 gam Al
c) 11 gam CO2
d) 4,958 lít khí oxi ở điều kiện tiêu chuẩn (250C và áp suất 1 bar)
e) 12,359 lít khí Me tan ở điều kiện tiêu chuẩn( 250C và áp suất 1 bar)
a) \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
b) \(n_{Al}=\dfrac{13,5}{27}=0,5\left(mol\right)\)
c) \(n_{CO_2}=\dfrac{11}{44}=0,25\left(mol\right)\)
d) \(m_{O_2}=\dfrac{4,958.0,99}{0,082.\left(273+25\right)}=0,2\left(mol\right)\)
e) \(m_{CH_4}=\dfrac{12,359.0,99}{0,082\left(273+25\right)}=0,5\left(mol\right)\)
a: \(n=\dfrac{28}{56}=0.5\left(mol\right)\)
b: \(n=\dfrac{13.5}{27}=0.5\left(mol\right)\)
1 bình oxi có thể tích 0,15met khối áp suất tuyệt đối là 20 bar nhiệt độ tuyệt đối 27độ c.người ta bơm khí vào bình đến áp suất tuyệt đối la 6 bar nhiệt độ không đổi tính lương khí oxi bơm vào bình
1. Trong phòng thí nghiệm, người ta điều chế được 20 dm' khi ở áp suất 750 mmlg và nhiệt độ 37°C . Thể tích của lượng khi trên ở điều kiện chuẩn là bao nhiêu cm" Biết ở điều kiện tiêu chuẩn áp suất 740 mmHg và nhiệt độ 0 C.
Ta có: \(\dfrac{p_1\cdot V_1}{T_1}=\dfrac{p_2\cdot V_2}{T_2}\)
\(\Rightarrow\dfrac{20\cdot750}{37+273}=\dfrac{V_2\cdot740}{0+273}\)
\(\Rightarrow V_2=17,85dm^3=17,85l\)
Đổi 20dm3=20000cm3
Áp dụng pt trạng thái:
(P1.V1):T1 = (P2.V2):T2
⇒( 750.20000):310 = (740.V2): 273
⇒V2= 17851 cm3