Khi nhiệt độ trong một bình tăng cao, áp suất của khối khí trong bình cũng tăng lên đó là vì
A. Số lượng phân tử tăng
B. Phân tử khí chuyển động nhanh hơn
C. Phân tử va chạm với nhau nhiều hơn
D. Khoảng cách giữa các phân tử tăng
Khi nhiệt độ trong một bình tăng cao, áp suất của khối khí trong bình cũng tăng lên đó là vì
A. số lượng phân tử tăng.
B. phân tử khí chuyển động nhanh hơn.
C. phân tử va chạm với nhau nhiều hơn.
D. khoảng cách giữa các phân tử tăng.
Đáp án: B
Khi chuyển động, mỗi phân tử khí va chạm với thành bình, bị phản xạ và truyền động lượng cho thành bình, rất nhiều phân tử va chạm với thành bình tạo nên một lực đẩy vào thành bình. Lực này tạo ra áp suất của khí lên thành bình. Do vậy khi nhiệt độ trong một bình tăng cao → chuyển động này càng nhanh → động lượng tăng nhanh → áp lực lên thành bình tăng → áp suất của khối khí trong bình cũng tăng lên.
Khi tăng nhiệt độ của khí đựng trong một bình kín làm bằng inva (một chất hầu như không nở vì nhiệt) thì
A. khoảng cách giữa các phân tử khí tăng
B. khoảng cách giữa các phân tử khí giảm
C. vận tốc của các phân tử khí tăng
D. vận tốc của các phân tử khí giảm.
Chọn C
Vì theo tính chất của chất khí khi tăng nhiệt độ thì vận tốc của các phân tử khí sẽ tăng.
Hai bình khí lí tưởng cùng nhiệt độ. Bình B có dung tích gấp đôi bình A, có số phân tử bằng nửa số phân tử trong bình A, Mỗi phân tử khí trong bình B có khối lượng gấp đôi khối lượng mỗi phân tử khí trong bình A. Áp suất khí trong bình B so với áp suất khí trong bình A là:...?
ta có
\(\text{P1.V1=m/M.R.T (1) }\)
\(\text{P2.2V1=1/2.2m/M.R.T (2) }\)
lấy (1) chia (2) vế theo vế ta đc
\(\text{P1.V1/P2.2V1=1 }\)
\(\Rightarrow\text{P1.V1=P2.2V1 }\)
\(\Rightarrow\text{P1=2P2 }\)
Đối với không khí trong một lớp học thì khi nhiệt độ tăng
A. kích thước các phân tử không khí tăng
B. vận tốc các phân tử không khí tăng
C. khối lượng không khí trong phòng tăng
D. thể tích không khí trong phòng tăng.
Chọn B
Vì theo tính chất của chất khí khi nhiệt độ tăng thì vận tốc chuyển động động của các phân tử không khí tăng.
Đốt nóng một lượng khí chứa trong một bình kín gần như không nở vì nhiệt sao cho nhiệt độ tuyệt đối của khí tăng lên 1,5 lần. Khi đó áp suất của khí trong bình
A. tăng lên 3 lần. B. giảm đi 3 lần.
C. tăng lên 1,5 lần. D. giảm đi 1,5 lần.
Một bình kín dung tích 5,6 lít có chứa hỗn hợp hơi của hai ancol đơn chức và 3,2 g O 2 . Nhiệt độ trong bình là 109 , 2 ° C , áp suất trong bình là 0,728 atm.
Bật tia lửa điện để đốt cháy hoàn toàn hai ancol, sau phản ứng nhiệt độ trong bình là 136 , 5 ° C và áp suất là p atm.
Dẫn các chất trong bình sau phản ứng qua bình (1) đựng H 2 S O 4 đặc (dư), sau đó qua bình (2) đựng dung dịch NaOH (dư), thấy khối lượng bình (1) tăng 1,26 g, khối lượng bình (2) tăng 2,2 g.
1. Tính p, biết rằng thể tích bình không đổi.
2. Xác định công thức phân tử, công thức cấu tạo, phần trăm khối lượng và gọi tên từng chất trong hỗn hợp ancol biết rằng số mol của ancol có phân tử khối nhỏ hn gấp 2 lần số mol của ancol có phân tử khối lớn hơn.
1. Đổi thể tích hỗn hợp khí trong bình trước phản ứng về đktc:
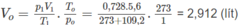
Số mol các chất trong bình trước phản ứng là:
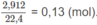
Số mol O2 = 0,1 (mol) ⇒ Số mol 2 ancol = 0,13 - 0,1 = 0,03 (mol).
Khi 2 ancol cháy :
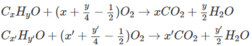
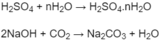
Số mol
H
2
O
là: 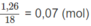
Số mol
C
O
2
là: 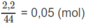
Theo định luật bảo toàn khối lượng :

= 3,2 + 0,03.16 - 0,07.16 - 0,05.32 = 0,96 (g).
Số mol
O
2
còn dư: 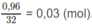
Tổng số mol các chất trong bình sau phản ứng :
0,07 + 0,05 + 0,03 = 0,15 (mol).
Thể tích của 0,15 mol khí ở đktc là: V O = 0,15.22,4 = 3,36 (lít).
Thực tế, sau phản ứng V = 5,6 lít.
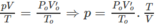
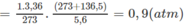
2. Giả sử C x H y O có PTK nhỏ hơn C x ' H y ' O ; như vậy số mol C x H y O sẽ là O 2 và số mol C x ' H y ' O là 0,01.
Số mol C O 2 sẽ là 0,02x + 0,01x' = 0,05 (mol) hay 2x + x' = 5.
x và x' là số nguyên: x = 1 ; x' = 3
hoặc x = 2; x' = 1
Cặp x = 2; x' = 1 loại vì trái với điều kiện: C x H y O có PTK nhỏ hơn C x ' H y ' O
Vậy, một ancol là C H 4 O và chất còn lại C 3 H y ' O .
Số mol H 2 O là 0,02.2 + 0,01.(y′/2) = 0,07 (mol).
⇒ y' = 6 ⇒ Ancol còn lại là C 3 H 6 O .
% về khối lượng của C H 4 O hay C H 3 - O H (ancol metylic) :

% về khối lượng của C 3 H 6 O hay C H 2 = C H - C H 2 - O H (a- Oncol anlylic): 100,00% - 52,46% = 47,54%.
Một phân tử khí có khối lượng m = 6,54 × 10-26 kg chuyển động với vận tốc v = 244 m / s tới va chạm đàn hồi vào thành bình với góc nghiêng 45 so với pháp tuyến của thành bình . Tính xung lượng của lực va chạm của phân tử khí lên thành bình .
Ta có: \(\overrightarrow{F}\cdot\Delta t=\Delta\overrightarrow{p}=\overrightarrow{p_{sau}}-\overrightarrow{p_{trc}}\)
\(\Rightarrow F\cdot\Delta t=6,54\cdot10^{-26}\cdot\left(-244-244\right)=-3,19152\cdot10^{-23}N\cdot s\)
Một bình kín chứa N = 3 , 01 . 10 23 phân tử khí heli.
a/ Tính khối lượng khí Heli chứa trong bình.
b/ Biết nhiệt độ khí là 0 ∘ C và áp suất khí trong bình là 1atm ( 1 , 013 . 10 5 Pa). Hỏi thể tích của bình là bao nhiêu?
a)
Cứ N A phân tử (nguyên tử) He có khối lượng 4g.
Chú ý: N = 3 , 01.10 23 = N A 2
⇒ khối lượng He trong bình: m = 4 2 = 2 g
b)
Trong điều kiện nhiệt độ và áp suất như trên (ĐKTC),
thể tích của 1 mol He là V 0 = 22,1 lít. Vì lượng khí He
trong bình chỉ là 0,5 mol nên thể tích của bình là:
V = V 0 2 = 11 , 2 lít.
Chọn phương án đúng. Khi nhiệt độ tăng điện trở chất điện phân giảm là do
(1) chuyển động nhiệt của các phân tử tăng nên khả năng phân li thành các ion tăng do tác dụng của các va chạm. Kết quả là làm tăng nồng độ hạt tải điện;
(2) độ nhớt của dung làm cho ác ion chuyển động được dễ dàng hơn.
A. (1) đúng; (2) sai
B. (1) sai; (2) đúng.
C. (1) đúng; (2) đúng.
D. (1) sai; (2) sai