Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
A. C 17 37 l
B. K 19 39
C. K 19 40
D. C 17 35 l
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
A. C 17 37 l
B. K 19 40
C. C 17 35 l
D. K 19 39
Có số p = số e=
2
,
7234
.
10
-
18
1
,
6
.
10
-
19
= 17
Số hạt mang đinẹ nhiều hơn số hạt không mang điện là 16 → n = 17.2 - 16 = 18
Vậy số khối của X là A= n + p = 18 + 17 = 35
Số hiệu nguyên tử của X là Z= p = 17
Vậy kí hiệu của X là
C
17
35
l
.
Đáp án C.
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là:
A. C 17 37 l
B. K 19 39
C. K 19 40
D. C 17 35 l
Đáp án A
Điện tích hạt nhân = số p . (+1,602.10-19) = +2,7234.10-18C.
=> Số p = 17, số n = 17 + 16 = 33
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
![]()
![]()
![]()
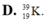
Nguyên tử X có điện tích hạt nhân là +2,7234.10-18 C. Trong ngtử X số hạt mag điện nhiều hơn số hạt không mang điện là 16. Kí hiệu ngtử của X là
Số p trong hạt nhân là : \(\frac{2,7234.10^{-18}}{1,6.10^{-19}}=17\)
Suy ra số e = số p = 17
Số n = 2.17-16 = 18
Kí hiệu nguyên tử X là 3517X
Một nguyên tử X có tổng số hạt là 155, số hạt mang điện nhiều hơn số hạt không mang điện là 33. Xác định điện tích hạt nhân, nguyên tử khối và viết kí hiệu của nguyên tử X
Ta có: \(\left\{{}\begin{matrix}2Z+N=155\\2Z-N=33\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}Z=47\\N=61\end{matrix}\right.\)
Điện tích hạt nhân: 47+
Nguyên tử khối: 108
Kí hiệu: Ag
\(X(2p, n) \begin{cases} 2p+n=155\\ 2p-n=33 \end{cases}\Leftrightarrow \begin{cases} p=e=47\\ n=61 \end{cases} \to: Ag\)
Một nguyên tử X có tổng số hạt nhân là 24. Trong đó số hạt điện mang điện nhiều hơn số hạt không mang điện là 8 a) Tìm P, n, e, A của nguyên tử X b) Viết kí hiệu của nguyên tử X
Tổng số hạt là :24
2p+n=24(1)
Số hạt mang điện nhiều hơn số hạt không mang điện là :8
2p−n=8(2)
(1),(2):p=e=8,n=8
=>A=8+8=16
=> đây là chất O oxi
a) Tổng số hạt mang điện trong nguyên tử X là 18, nguyên tử X có tổng số hạt mang điện gấp đôi số hạt không mang điện. Hãy viết kí hiệu nguyên tử X b) Tổng số hạt P,E,N trong nguyên tử X là 156, số hạt mang điện nhiều hơn số hạt không mang điện là 32. Tìm số hạt P,E,N, số khối của X.
a) Ta có : \(\left\{{}\begin{matrix}2Z=18\\2Z=2N\end{matrix}\right.\)
=> Z=N=9
Vậy X là Flo (F)
b) Ta có : \(\left\{{}\begin{matrix}2Z+N=156\\2Z-N=32\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}Z=47=P=E\\N=62\end{matrix}\right.\)
A=Z+N=47+62=109
1. Nguyên tử của nguyên tố X có tổng số hạt là 28. Trong HẠT NHÂN, số hạt không mang điện nhiều hơn số hạt mang điện là 1. Tìm X? Viết kí hiệu nguyên tử của X?
Gọi số hạt proton = số hạt electron = p
Gọi số hạt notron = n
Ta có :
$2p + n = 28$ và $n - p = 1$
Suy ra p = 9 ; n = 10
Vậy X là nguyên tố Flo, KHHH : F
Bài 2.2.3. Tổng số hạt mang điện của nguyên tử X là 30. Biết rằng tổng số hạt trong hạt nhân nguyên tử X nhiều hơn số hạt mang điện trong nguyên tử X là 1. Viết kí hiệu nguyên tử X.
Ta lập HPT: \(\left\{{}\begin{matrix}2Z+N=30\\Z+N-2Z=1\end{matrix}\right.\) \(\Rightarrow\) Nghiệm lẻ
*Bạn xem lại đề !!