Trộn 100ml dung dịch có pH=1 gồm HCl và HNO3 với 100ml dung dịch NaOH nồng độ a (mol/l) thu được 200ml dung dịch có pH=12 . Giá trị của a là ?

Những câu hỏi liên quan
Trộn 100ml dung dịch có pH =1 gồm HCl và HNO3 với 100ml dung dịch NaOH nồng độ a mol/l thu được 200ml dung dịch có pH=12 giá trị của a là
Dung dịch axit ban đầu có [H+] = 0,1 M
⇒ nH+= 0,1.0,1 = 0,01 mol
Dung dịch sau phản ứng có pH = 12
⇒ dư bazơ và có pOH =14 – 12 = 2
⇒ [OH-] = 0,01M
⇒ nOH− dư = 0,002 mol
Phản ứng trung hòa:
nH+phản ứng = nOH−phản ứng = 0,01 mol
⇒ nNaOH ban đầu = nOH−phản ứng + nOH− dư
= 0,01 + 0,002 = 0,012 mol
⇒ a = 0,12M
Đúng 2
Bình luận (0)
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a mol/l thu được 200 ml dung dịch có pH = 12. Giá trị của a là
A. 0,03
B. 0,30
C. 0,15
D. 0,12
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a mol/l thu được 200 ml dung dịch có pH = 12. Giá trị của a là
A. 0,03
B. 0,30
C. 0,15
D. 0,12
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a mol/l thu được 200 ml dung dịch có pH = 12. Giá trị của a là
A. 0,03.
B. 0,30.
C. 0,15.
D. 0,12.
Đáp án D
Dd axit ban đầu có [H+] =0,1 M → nH+=0,1.0,1 =0,01 mol
Dd sau phản ứng có pH = 12 → dư bazo và có pOH =14-12=2 → [OH-] =0,01M→ nOH = 0,002 mol
PTHH: H+ + OH- → H2O
Ta có nNaOH = nH+ + nOH dư = 0,01 + 0,002 = 0,012 mol → a = 0,12M
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch có pH 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a (mol/l) thu được 200 ml dung dcó pH 12. Giá trị của a là : A. 0,15 B. 0,30 C. 0,03. D. 0,12.
Đọc tiếp
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a (mol/l) thu được 200 ml dung dcó pH = 12. Giá trị của a là :
A. 0,15
B. 0,30
C. 0,03.
D. 0,12.
Đáp án D
nH+ = 0,1.0,1= 0,01
Trong dụng dịch sau phản ứng có nOH- = 0,01 .0,2=0,002
⇒ nOH- ban đầu = n H+ + n OH-dư = 0,01+0,002=0,012
⇒ a = 0,012 ÷ 0,1 =0,12
Đáp án D.
Đúng 0
Bình luận (0)
Trộn 100ml dd có pH=1 gồm HCl và HNO3 với 100ml dd NaOH nồng độ a (mol/l) thu được 200ml dd có pH=12. Giá trị của a là (biết trong mọi dd [H+][OH-]=10-14 )
A.0,15
B. 0,30
C. 0,03
D. 0,12
Đáp án D
pH =1 => [H+] = 0,1 => n H + = 01.01 = 0,01 mol.
n O H - = 0,1a
pH =12 => [H+] = 10-12 => [OH-] =10-2 => n O H - dư = 0,01.(0,1+0,1) = 0,002 mol
=> 0,1a - 0,01 = 0,002 => a = 0,12.
Đúng 0
Bình luận (0)
Trộn 300ml dung dịch có pH 2 gồm HCl và HNO3với 300ml dung dịch NaOH nồng độ a (mol/l) thu được 600 ml dung dịch có pH 11. Giá trị của a là: A. 0,012 B. 0,021 C. 0,018 D. 0,024
Đọc tiếp
Trộn 300ml dung dịch có pH = 2 gồm HCl và HNO3với 300ml dung dịch NaOH nồng độ a (mol/l) thu được 600 ml dung dịch có pH = 11. Giá trị của a là:
A. 0,012
B. 0,021
C. 0,018
D. 0,024
Đáp án A
pH = 11 => OH- dư sau phản ứng => pOH =3
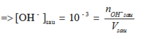
=> nOH- sau = Vsau . [OH-] = 10-3. 0,6= 0,0006 = 6.10-4 (mol)
pH = 2 => [H+]= 10-2 = 0,01M => nH+= 0,3 . 0,01= 0,003
nOH- = 0,3.a
H+ + OH- → H2O
Ban đầu: 0,003 0,3.a
Phản ứng: 0,003 0,003
Sau: 0 0,3.a-0,003
nOH- sau= 6.10-4 = 0,3a -0,003 => a=0,012M
Đúng 0
Bình luận (0)
Trộn 100ml dung dịch KOH 0,3M với 100ml dung dịch HNO3 có pH=1 thu được 200ml dung dịch A. pH của dung dịch A bằng:
A. 0,7
B. 1,0
C. 13,0
D. 13,3
Đáp án C
nOH- = 0,03 mol; nH+ = 0,1.10-1 = 0,01 mol
H+ + OH- → H2O
0,01 0,03 mol
nOH- dư = 0,02 mol; [OH-]dư= 0,02/0,2 = 0,1M, [H+] = 10-13 M, pH = 13
Đúng 0
Bình luận (0)
Trộn 100ml đ có pH=1 gồm HCL và HNO3 với 100ml dd NAOH nồng độ a (mol/l) thu 200ml dd pH=12. Giá trị a?
A.0.15 B.0.30 C.0.03 D.0.12
Dung dịch HCl và HNO3 có pH=1:
=>[H+] = 10^-1 (mol/l)
=>Σ nH{+} = 10^-1*0.1 = 0.01(mol)
+nNaOH = 0.1a (mol)
NaOH => Na{+} + OH{-}
0.1a.........0.1a.......0.1a(mol)
=>nOH{-} = 0.1a (mol)
_Sau phản ứng thu được dung dịch có pH = 12:
+pH = 12:môi trường có tính bazơ => bazơ dư , axit hết.
+pH = 12 => pOH = 14 - 12 = 2 => [OH-] = 10^-2 (mol/l)
=>nOH{-} dư = 10^-2*0.2 = 2*10^-3 (mol)
H{+} + OH{-} => H2O
0.01....0.1a
0.01....0.01........0.01(mol)
..0....0.1a - 0.01.0.01(mol)
=>nOH{-} dư = 0.1a - 0.01 = 2*10^-3 (mol)
<=>0.1a = 0.012
<=>a = 0.12
Vậy a = 0.12 (M)
=> D đúng
Đúng 0
Bình luận (0)








