Cho 7,2 gam một loại oxit sắt tác dụng hoàn toàn với khí hiđro cho 5,6 gam sắt. Xác định CTHH của Oxit Sắt.
//Mn giúp mik vs ạ 🙋//
Cho 7,2 gam một loại oxit sắt tác dụng hoàn toàn với khí hiđro cho 5,6 gam sắt. Công thức oxit sắt là
A. F e O
B. F e 2 O 3
C. F e 3 O 4
D. F e O 2
Đáp án: A
Đặt oxit sắt là FexOy
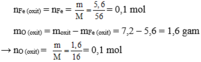
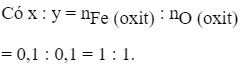
Vậy oxit là FeO.
Cho 7,2 gam một loại oxit sắt tác dụng hoàn toàn với khí hiđro cho 5,6 gam sắt . Tìm công thức oxit sắt
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Gọi: CTHH của oxit là FexOy
Ta có: mO = 7,2 - mFe = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
⇒ x:y = 0,1:0,1 = 1:1
→ CTHH cần tìm là FeO.
Bài 5. a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol. b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
a) Gọi CTHH của oxit sắt là $Fe_2O_n$
$Fe_2O_n + nCO \xrightarrow{t^o} 2Fe +nCO_2$
$n_{Fe} = \dfrac{22,4}{56} = 0,2(mol)$
$\Rightarrow n_{Fe_2O_n} = \dfrac{1}{2}n_{Fe} = 0,2(mol)$
$M_{oxit} = 56.2 + 16n = \dfrac{32}{0,2}=160$
Suy ra : n = 3
Vậy oxit cần tìm là $Fe_2O_3$
b) $n_{CO_2} = \dfrac{3}{2}n_{Fe} = 0,6(mol)$
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,6(mol)$
$m_{CaCO_3} = 0,6.100 = 60(gam)$
Câu 6: Cho 7,2 gam một loại oxit sắt tác dụng hoàn toàn với axit HCl thu được 12,7 gam muối. Tìm công thức oxit sắt..
giải chi tiết
Gọi CTHH oxit sắt cần tìm là \(Fe_xO_y\)
\(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\)
\(n_{FeCl_{\dfrac{2y}{x}}}=x.n_{Fe_xO_y}\\ \Leftrightarrow\dfrac{12,7}{56+35,5\cdot\dfrac{2x}{y}}=\dfrac{7,2x}{56x+16y}\\ \Leftrightarrow308x=308y\\ \Rightarrow\dfrac{x}{y}=\dfrac{308}{308}=\dfrac{1}{1}\)
CTHH oxit sắt cần tìm là \(FeO\)
Khử hoàn toàn 4,06 gam một oxit sắt bằng khí CO dư ở nhiệt độ cao thành kim loại . Dẫn toàn bộ khí sinh ra vào bình đựng dd ca(oh)2 dư . Thấy tạo thành 7(g) kết rủa a) xác định công thức oxit sắt B) cho 4,06 g oxit sắt trên tác dụng hoàn toàn với dd H2SO4 đặc nóng
`a)`
Oxit: `Fe_xO_y`
`Fe_xO_y+yCO` $\xrightarrow{t^o}$ `xFe+yCO_2`
`CO_2+Ca(OH)_2->CaCO_3+H_2O`
Theo PT: `n_{CO_2}=n_{CaCO_3}=7/{100}=0,07(mol)`
`->n_{Fe_xO_y}={n_{CO_2}}/y={0,07}/y(mol)`
`->M_{Fe_xO_y}={4,06}/{{0,07}/y}=58y`
`->56x+16y=58y`
`->x/y={42}/{56}=3/4`
`->` Oxit: `Fe_3O_4`
`b)`
`n_{Fe_3O_4}={4,06}/{232}=0,0175(mol)`
`2Fe_3O_4+10H_2SO_4->3Fe_2(SO_4)_3+SO_2+10H_2O`
Đề thiếu.
Cho 5,6 gam kim loại sắt tác dụng với một lượng axit HCl vừa đủ, dẫn toàn bộ lượng khí sinh ra đi cho qua 16 gam sắt (III) oxit đun nóng
cho 16 gam một loại oxit sắt hợp chất của sắt và oxi tác dụng hết với khí hiđro thu được 11,2g fe tìm CTHHcua oxit sắt
\(n_{Fe}=0,2mol\)
\(Fe_xO_y+yH_2\rightarrow xFe+yH_2O\)
\(\dfrac{0,2}{x}\)..........................0,2
\(M_{Fe_xO_y}=\dfrac{16}{\dfrac{0,2}{x}}=80x\Leftrightarrow56x+16y=80x\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(\Rightarrow x=2;y=3\)
Oxit sắt là: \(Fe_2O_3\)
Đặt CTHH: FexOy
\(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{Fe_xO_y}=\dfrac{0,2}{x}\left(mol\right)\)
\(M_{Fe_xO_y}=\dfrac{16}{\dfrac{0,2}{x}}=80x\)
\(56x+16y=80x\)
\(\Leftrightarrow16y=24x\)
\(\Leftrightarrow\)\(\dfrac{x}{y}=\dfrac{16}{24}=\dfrac{2}{3}\)
\(\Rightarrow x=2;y=3\)
CTHH của oxit sắt: Fe2O3
Dùng khí hiđro dư để khử x gam sắt(III) oxit, sau phản ứng người ta thu được y gam sắt kim loại. Nếu dùng lượng sắt này cho phản ứng hoàn toàn với axit clohiđric có dư thì thu được 5,6 lít khí hiđro đo ở điều kiện tiêu chuẩn.
a) Viết các phương trình phản ứng hóa học.
b) Hãy xác định giá trị x, y và lượng muối sắt(II) clorua tạo thành sau phản ứng.
Khử hoàn toàn 11,6g một oxit sắt (FexOy) bằng khí H2 ở to cao thu được 8,4g sắt kim loại. Xác định CTHH của oxit sắt và tính VH2 (đktc) đã dùng
chỉ mik với các bn
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\ n_O=\dfrac{11,6-0,15}{16}=0,2\left(mol\right)\)
CTHH: FexOy
\(\rightarrow x:y=n_{Fe}:n_O=0,15:0,2=3:4\)
CTHH: Fe3O4
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
0,2 0,15
=> VH2 = 0,2.22,4 = 4,48 (l)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
\(n_{Fe_xO_y}=\dfrac{11,6}{56x+16y}\) mol
\(Fe_xO_y+yH_2\rightarrow\left(t^p\right)xFe+yH_2O\)
\(\dfrac{11,6}{56x+16y}\) \(\dfrac{11,6x}{56x+16y}\) ( mol )
\(\Rightarrow\dfrac{11,6x}{56x+16y}=0,15\)
\(\Leftrightarrow11,6x=8,4x+2,4y\)
\(\Leftrightarrow3,2x=2,4y\)
\(\Leftrightarrow4x=3y\)
\(\Leftrightarrow x=3;y=4\)
\(\Rightarrow CTHH:Fe_3O_4\)
\(\Rightarrow n_{H_2}=0,15.4:3=0,2mol\)
\(V_{H_2}=0,2.22,4=4,48l\)