Ngâm 17,6 gam hỗn hợp sắt và đồng vào trong dung dịch đồng (II) sunfat dư. Phản ứng xong thu được 19,2gam chất rắn không tan
viết pthh
tính thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp ban đầu
Ngâm 15 gam hỗn hợp Fe và Cu trong dung dịch CuSO4 dư. Phản ứng xong thu được 16 gam chất rắn. Thành phần phần trăm khối lượng của mỗi kim loại trong hỗn hợp ban đầu tương ứng là:
A. 53,34% và 46,66%
B. 46,67% và 53,33%
C. 40% và 60%
D. 60% và 40%
Đáp án B
Phương trình phản ứng:
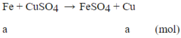
m tăng = (64-56).a = 1 ⇒a=0,125 mol
nFe = 0,125 ⇒nCu = (15-56.0,125)/64 = 0,125 mol
Thành phần phần trăm theo khối lượng:
⇒ % mCu = 53,33
Câu 9: Ngâm 21,6 g hỗn hợp 3 kim loại Zn, Fe và Cu trong dung dịch H2SO4 loãng, dư. Phản ứng xong, thu được 3g chất rắn không tan và 6,72l khí (ở đktc).
a) Viết PTHH xảy ra
b) Xác định thành phần phần trăm của mỗi kim loại trong hỗn hợp
a)Zn +H2SO4 -> ZnSO4 +H2
Fe +H2SO4 -> FeSO4 +H2
Cu +H2SO4 -> CUSO4+H2
đặt số mol 3 KL Zn, Fe, Cu lần lượt là a, b, c (mol), ta có pt theo đề bài:
65a+56b+64c=21.6 (1)
c=3/64 (2)
a+b=6.72/22.4 (3)
Từ (1)(2)(3)==> a=0.2(mol), b=0.1(mol), c=3/64(mol)
==>%Zn=0.2 x 65 x100/21.6 = 60.185%
%Fe=0.1 x 56 x 100/21.6 = 25.925%
%Cu=100%-( 60.185% + 25.925% )= 13.89%
Cho 13g hỗn hợp A gồm Cu, Al, Mg vào dung dịch HCl dư, phản ứng xong thu được 4 gam chất rắn không tan và 10,08 lít khí H 2 (đktc). Tính thành phần phần trăm theo khối lượng của từng kim loại trong hỗn hợp.
A. 30,77%; 27,69%; 41,54%
B. 27,69%; 41,54%; 30,77%
C. 30,77%; 41,54%; 27,69%
D. 27,69%; 30,77%;41,54%
2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
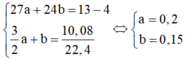
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.

Bảo toàn nguyên tố M: nMSO4 = 0,25mol
Bảo toàn nguyên tố Cu: nCuSO4 dư = 0,1 mol
=> M = 24 (Mg)
b.

3. Hòa tan 24,8 gam hỗn hợp bột sắt và đồng trong dung dịch HNO3 loãng thu được 6,72 lít khí NO ( ở đktc).
a. Viết các phương trình phản ứng hóa học
b. Tính thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn h
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(Fe+4HNO_{3l}\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_{3l}\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(n_{NO}=\dfrac{6,72}{22,4}=0,3mol\)
\(\Rightarrow\left\{{}\begin{matrix}56a+64b=24,8\\BTe:3a+2b=3\cdot0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,3\end{matrix}\right.\)
\(\%m_{Fe}=\dfrac{0,1\cdot56}{24,8}\cdot100\%=22,58\%\)
\(\%m_{Cu}=100\%-22,58\%=77,42\%\)
Cho 10 gam hỗn hợp bột các kim loại sắt và đồng vào dung dịch CuSO 4 dư. Sau khi phản ứng xảy ra hoàn toàn thu được chất rắn có khối lượng 11 gam. Thành phần phần trăm theo khối lượng của sắt và đồng trong hỗn hợp đầu là
A. 35% và 65% ; B. 40% và 60% ;
C. 70% và 30% ; D. 50% và 50%.
Đáp án C.
Fe + CuSO 4 → FeSO 4 + Cu
n Fe = x mol
Khối lượng Fe phản ứng (cũng là khối lượng sắt trong hỗn hợp đầu) là 56x. Khối lượng Cu sinh ra 64x.
CuSO 4 dư nên chất rắn sau phản ứng là đồng :
10 - 56x + 64x = 11 → x = 1/8 mol
m Fe trong hỗn hợp đầu là: 56 x 1/8 = 7g
% m Fe = 7/10 x 100% = 70%
% m C u = 100% - 70% = 30%
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.2.....................................0.2\)
\(m_{Fe}=0.2\cdot56=11.2\left(g\right)\)
\(m_{Fe}=m_{hh}=11.2\left(g\right)\)
=> Đề sai
Cho 13 g hỗn hợp bột các kim loại magie, nhôm và đồng tác dụng với dung dịch HCl 2M dư. Phản ứng xong thu được 10,08 lít khí bay ra ở (đktc) và 4 g chất rắn không tan. a/ Tính thành phần % khối lượng mỗi kim loại có trong hỗn hợp. b/ Để trung hòa lượng axit HCl 2M dư người ta dùng dung dịch NaOH vừa đủ. Hãy tính thể tích dung dịch HCl 2M đã dùng.
Chất rắn ko tan là Cu
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=13-4=9(1)\)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,45(2)\\ (1)(2)\Rightarrow x=0,15(mol);y=0,2(mol)\\ a,\%_{Cu}=\dfrac{4}{13}.100\%=30,77\%\\ \%_{Mg}=\dfrac{0,15.24}{13}.100\%=27,69\%\\ \%_{Al}=100\%-30,77\%-27,69\%=41,54\%\\ b,\Sigma n_{HCl}=2x+3y=0,9(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,9}{2}=0,45(l)\)
m(Zn,Mg)=25-6,5= 18,5(g)
nHCl(p.ứ)= 0,8.2 : 125%= 1,28(mol)
PTHH: Zn + 2 HCl -> ZnCl2 + H2
x__________2x_____x____x(mol)
Mg + 2 HCl -> MgCl2 + H2
y______2y____y_____y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}65x+24y=18,5\\2x+2y=1,28\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=\dfrac{157}{2050}\\y=\dfrac{231}{410}\end{matrix}\right.\)
=>
\(\%mAg=\dfrac{6,5}{25}.100=26\%\\ \%mZn=\dfrac{\dfrac{157}{2050}.65}{25}.100\approx19,912\%\\ \rightarrow\%mMg\approx54,088\%\)