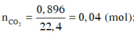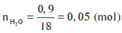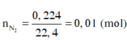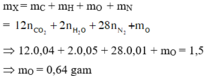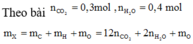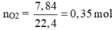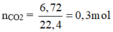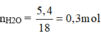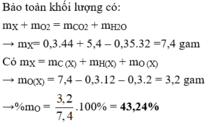Oxi hóa hoàn toàn 4,56g một hợp chất hữu cơ A thu được 13,20g CO2 và 3,16g H2O. Ở ống nghiệm khác nung 5,58g A với cho thu được 0,67 lít khi nitơ( đktc). Tính % khối lượng của C, N, H và oxi ở hợp chất A.

Những câu hỏi liên quan
Nung 4,65 gam một chất hữu cơ A trong dòng khí oxi thì thu được 13,20 gam CO2 và 3,15 gam H2O. Ở thí nghiệm khác, nung 5,58 gam chất hữu cơ với CuO thì thu được 0,67 lít khí N2 (đktc). Trong A có chứa nguyên tố: A. C và H. B. C, H và N. C. C, H, N và O. D. C, N và O.
Đọc tiếp
Nung 4,65 gam một chất hữu cơ A trong dòng khí oxi thì thu được 13,20 gam CO2 và 3,15 gam H2O. Ở thí nghiệm khác, nung 5,58 gam chất hữu cơ với CuO thì thu được 0,67 lít khí N2 (đktc). Trong A có chứa nguyên tố:
A. C và H.
B. C, H và N.
C. C, H, N và O.
D. C, N và O.
Đáp án B
Đốt cháy A tạo CO2 và H2O => chắc chắn trong A có C và H.
=> nC = nCO2 = 0,3 mol ; nH = 2nH2O = 0,35 mol
Xét 5,58g A phản ứng với CuO tạo nN2 = 0,03 mol
=> Trong 5,58g A có 0,06 mol N
=> Trong 4,65g A thì nN = 0,05 mol
Ta có : mC + mH + mN = 4,65g
=> A chỉ có 3 nguyên tố là C, H , N.
Đúng 0
Bình luận (0)
Oxi hóa hoàn toàn 1,5 gam hợp chất hữu cơ X, thu được 0,224 lít
N
2
và 0,896 lít
CO
2
(các khí đều đo ở đktc) và 0,9 gam
H
2
O
. Khối lượng nguyên tố oxi trong 1,5 gam X là A. 0,32 gam B. 0,16 gam C. 0,64 gam D. 0,78 gam
Đọc tiếp
Oxi hóa hoàn toàn 1,5 gam hợp chất hữu cơ X, thu được 0,224 lít N 2 và 0,896 lít CO 2 (các khí đều đo ở đktc) và 0,9 gam H 2 O . Khối lượng nguyên tố oxi trong 1,5 gam X là
A. 0,32 gam
B. 0,16 gam
C. 0,64 gam
D. 0,78 gam
Oxi hóa hoàn toàn 6 gam hợp chất hữu cơ X, thu được 6,72 lít CO2 (đktc) và 7,2 gam H2O . Khối lượng nguyên tố oxi có trong 6 gam X là
A. 3,2 gam
B. 2,4 gam
C. 2,0 gam
D. 1,6 gam
Oxi hóa hoàn toàn 6 gam hợp chất hữu cơ X, thu được 6,72 lít CO2 (đktc) và 7,2 gam H2O . Khối lượng nguyên tố oxi có trong 6 gam X là A. 3,2 gam B. 2,4 gam C. 2,0 gam D. 1,6 gam
Đọc tiếp
Oxi hóa hoàn toàn 6 gam hợp chất hữu cơ X, thu được 6,72 lít CO2 (đktc) và 7,2 gam H2O . Khối lượng nguyên tố oxi có trong 6 gam X là
A. 3,2 gam
B. 2,4 gam
C. 2,0 gam
D. 1,6 gam
Khi oxi hoá hoàn toàn 5,00 gam một hợp chất hữu cơ, người ta thu được 8,40 lít C O 2 (đktc) và 4,50 g H 2 O .
Xác định phần trăm khối lượng của từng nguyên tố trong hợp chất hữu cơ đó.
Nguyên tố C chiếm 90% và nguyên tố H chiếm 10% về khối lượng.
Đúng 0
Bình luận (0)
6. Oxi hoá hoàn toàn 14,75g một hợp chất hữu cơ X bằng CuO dư , đun nóng , thu được 16,80 lít CO2 ; 2,80 lít N2 ( các thể tích đo ở đktc) và 20,25g H2O. Thành phần % về khối lượng các nguyên tố C,H,N có trong X lần lượt là?
Xem chi tiết
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam
C
O
2
và 5,4 gam
H
2
O
. Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A? A.
C
2
H
6
B.
C
2
H
4
C.
C...
Đọc tiếp
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
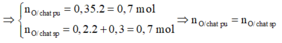
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
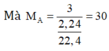
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
Đúng 0
Bình luận (0)
Oxi hoá hoàn toàn 0,6 gam hợp chất hữu cơ A thu được 0,672 lít CO2 (đktc) và 0,72 gam H2O. Tính thành phần phần trăm khối lượng của các nguyên tố trong phân tử chất A.
Gọi CTPT của hợp chất hữu cơ là CxHyOz (x, y, z nguyên dương; z ≥ 0)
Ta có:
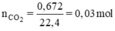
BT nguyên tố ⇒ nC = nCO2 = 0,03 mol ⇒ mC = 12. 0,03 = 0,36g
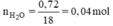
BT nguyên tố ⇒ nH = 2.nH2O = 2. 0,04 = 0,08 mol ⇒ mH = 0,08. 1 = 0,08 g
mO = 0,6 - 0,36 - 0,08 = 0,16(g)
⇒ Hợp chất A có chứa C, H, O
Phần trăm khối lượng các nguyên tố trong phân tử A là:

Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn m gam hợp chất hữu cơ X ( C, H, O ). Cần vừa đủ 7,84 lít
O
2
(đktc), thu được 6,72 lít
CO
2
(đktc) và 5,4 gam
H
2
O
. Thành phần phần trăm khối lượng oxi trong X là A. 16,62% B. 45,95% C. 28,85 % D. 43,24%.
Đọc tiếp
Đốt cháy hoàn toàn m gam hợp chất hữu cơ X ( C, H, O ). Cần vừa đủ 7,84 lít O 2 (đktc), thu được 6,72 lít CO 2 (đktc) và 5,4 gam H 2 O . Thành phần phần trăm khối lượng oxi trong X là
A. 16,62%
B. 45,95%
C. 28,85 %
D. 43,24%.