Khi hòa tan 30 gam hỗn hợp đồng và đồng 2 oxit trong dung dịch HNO3 1 M lấy dư ,thấy thoát ra 6,72 lít khí NO (đktc).a) có tính khối lượng các chất trong hỗn hợp ban đầu. b) Tính phần trăm các chất trong hỗn hợp ban đầu.
Khi hoà tan 30,0 g hỗn hợp đồng và đồng(II) oxit. trong dung dịch N H O 3 1,00 M lấy dư, thấy thoát ra 6,72 lít khí NO (đktc). Khối lượng của đồng (II) oxit trong hỗn hợp ban đầu là
A. 1,2 g. B. 4,25 g.
C. 1,88 g . D. 2,52 g.
Đáp án: A.
Hướng dẫn:
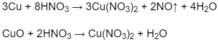
Số mol khí NO:
![]()
Theo phản ứng (1) số mol Cu:
![]()
Khối lượng Cu trong hỗn hợp ban đầu : m C u = 0,45.64 = 28,8 (g).
Khối lượng CuO trong hỗn hợp ban đầu : m C u O = 30 - 28,8 = 1,2 (g).
Hòa tan 32 g hỗn hợp Cu và CuO trong dung dịch HNO 3 1M (dư), thoát ra 6,72 lít khí NO (đktc). Khối lượng CuO trong hỗn hợp ban đầu là
A. 1,2g.
B. 1,88g.
C. 2,52g.
D. 3,2g.
Khi hoà tan 24,4 gam hỗn hợp đồng và sắt trong dung dịch HNO3 loãng dư thì thu được 6,72 lít khí nitơmonooxit (đktc). Xác định thành phần phần trăm về khối lượng từng kim loại trong hỗn hợp ban đầu
\(\left\{{}\begin{matrix}n_{Cu}\\n_{Fe}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}64x+56y=24,4\\2x+3y=\dfrac{6,72}{22,4}.3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,285\\y=0,11\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cu}=74,75\%\\\%m_{Fe}=25,25\%\end{matrix}\right.\)
Chia 38,6 gam hỗn hợp gồm Fe và kim loại M có hóa trị duy nhất thành 2 phần bằng nhau:
Phần 1: Tan vừa đủ trong 2 lít dung dịch HCl thấy thoát ra 14,56 lít H2 (đktc).
Phần 2: Tan hoàn toàn trong dung dịch HNO3 loãng nóng thấy thoát ra 11,2 lít khí NO duy nhất (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là:
A. 30,05%
B. 50,05%
C. 50,03%
D. Đ/a khác
Bài 7: Dẫn từ từ 6,72 lít hỗn hợp gồm CH4 và C2H2(đktc) lội qua dung dịch Brom dư thấy thoát ra 4,48 lít khí.
a) Viết PTHH xảy ra và tính phần trăm về khối lượng từng chất trong hỗn hợp ban đầu.
b) Tính khối lượng brom tham gia phản ứng
a)
PTHH: C2H2 + 2Br2 --> C2H2Br4
Khí thoát ra là CH4
\(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{C_2H_2}=\dfrac{6,72}{22,4}-0,2=0,1\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,2.16}{0,2.16+0,1.26}.100\%=55,17\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,2.16+0,1.26}.100\%=44,83\%\end{matrix}\right.\)
b)
PTHH: C2H2 + 2Br2 --> C2H2Br4
0,1--->0,2
=> mBr2 = 0,2.160 = 32 (g)
3. Hòa tan 24,8 gam hỗn hợp bột sắt và đồng trong dung dịch HNO3 loãng thu được 6,72 lít khí NO ( ở đktc).
a. Viết các phương trình phản ứng hóa học
b. Tính thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn h
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(Fe+4HNO_{3l}\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_{3l}\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(n_{NO}=\dfrac{6,72}{22,4}=0,3mol\)
\(\Rightarrow\left\{{}\begin{matrix}56a+64b=24,8\\BTe:3a+2b=3\cdot0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,3\end{matrix}\right.\)
\(\%m_{Fe}=\dfrac{0,1\cdot56}{24,8}\cdot100\%=22,58\%\)
\(\%m_{Cu}=100\%-22,58\%=77,42\%\)
Khi hòa tan 30g hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư), thoát ra 6,72 lit khí NO (đktc). Khối lượng của CuO trong hỗn hợp ban đầu là
A. 1,2g.
B. 1,88g.
C. 2,52g.
D. 4,25g.
Đáp án A
Bảo toàn ne=> 2nCu = 3nNO => nCu = 0,45 => mCuO = 30 – mCu = 1,2g => Chọn A.
Khi hòa tan 30g hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư), thoát ra 6,72 lit khí NO (đktc). Khối lượng của CuO trong hỗn hợp ban đầu là
A. 1,2g
B. 1,88g
C. 2,52g
D. 4,25g
Đáp án A
Bảo toàn ne => 2nCu = 3nNO => nCu = 0,45 => mCuO = 30 – mCu = 1,2g
Khi hòa tan 30g hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư), thoát ra 6,72 lit khí NO (đktc). Khối lượng của CuO trong hỗn hợp ban đầu là
A. 1,2g.
B. 1,88g.
C. 2,52g.
D. 4,25g.
Đáp án A
Bảo toàn ne =>2nCu = 3nNO => nCu = 0,45 => mCuO = 30 – mCu = 1,2g => Chọn A.