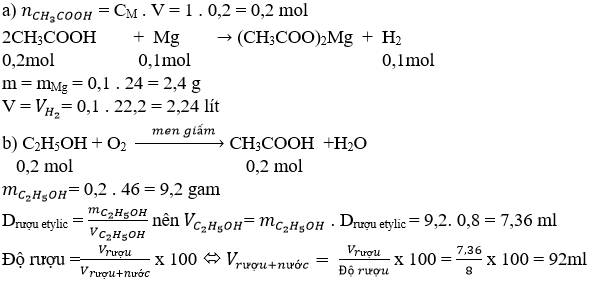Cho 20 gam dung dịch NaOH 10% phản ứng với H2SO4 2M. Tính V axit tham gia phản ứng. Cho lượng NaOH ở trên tác dụng vừa đủ với dung dịch MgCl2 thì thu được bao nhiêu gam kết tủa ?

Những câu hỏi liên quan
Câu 6.
a) Cho 200 ml dung dịch CH3COOH 2M tác dụng vừa đủ với dung dịch NaOH. Tính khối lượng NaOH tham gia phản ứng.
b) Cho 60 gam CH3COOH tác dụng với 100 gam C2H5OH thu được 55 gam CH3COOC2H5 . Tính hiệu suất của phản ứng trên.
a) nCH3COOH= 0,4(mol)
PTHH: CH3COOH + NaOH -> CH3COONa + H2O
0,4____________0,4(mol)
=> mNaOH=0,4. 40=16(g)
b) nCH3COOH= 1(mol)
nC2H5OH= 100/46= 50/23(mol)
Vì : 1/1< 50/23 :1
=> C2H5OH dư, CH3COOH hết, tính theo nCH3COOH.
PTHH: CH3COOH + C2H5OH \(⇌\) CH3COOC2H5 + H2O (đk: H+ , nhiệt độ)
Ta có: nCH3COOC2H5(thực tế)= 0,625(mol)
Mà theo LT: nCH3COOC2H5(LT)= nCH3COOH=1(mol)
=>H= (0,625/1).100=62,5%
Đúng 1
Bình luận (0)
Cho m gam magie tác dụng vừa đủ với 200 ml dung dịch HCI 2M, sau phản ứng thu được dung dịch A và V lít khí ở điều kiện tiêu chuẩn. a. Tính m và V. b. Thêm 100 gam dung dịch NaOH 20% vào dung dịch A. Tính khối lượng kết tủa thu được khi phản ứng kết thúc.
Ta có: \(n_{HCl}=\dfrac{200}{1000}.2=0,4\left(mol\right)\)
\(PTHH:Mg+2HCl--->MgCl_2+H_2\uparrow\left(1\right)\)
a. Theo PT(1): \(n_{Mg}=n_{H_2}=n_{MgCl_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,2.24=4,8\left(g\right)\\V_{H_2}=0,2.22,4=4,48\left(lít\right)\end{matrix}\right.\)
b. \(PTHH:2NaOH+MgCl_2--->Mg\left(OH\right)_2\downarrow+2NaCl\left(2\right)\)
Ta có: \(n_{NaOH}=\dfrac{\dfrac{20\%.100}{100\%}}{40}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,5}{2}>\dfrac{0,2}{1}\)
Vậy NaOH dư.
Theo PT(2): \(n_{Mg\left(OH\right)_2}=n_{MgCl_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Mg\left(OH\right)_2}=0,2.58=11,6\left(g\right)\)
Đúng 1
Bình luận (0)
a: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
200ml=0,2 lít
\(n_{HCl}=0.2\cdot22.4=4.48\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{H_2}=n_{H_2}\cdot M=2.24\cdot1=2.24\left(g\right)\)
\(n_{MgCl_2}=2.24\left(mol\right)\)
\(\Leftrightarrow n_{Mg}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{Mg}=2.24\cdot24=53.76\left(g\right)\)
Đúng 0
Bình luận (1)
cho 60g dung dịch NaOH 11,2% tác dụng vừa đủ với 190 g dung dịch MgCl2 đến khi phản ứng xong
a. Viết pt phản ứng
b. tính khối lượng chất kết tủa thu đc
c. tính nồng độ % (C%) dung dịch MgCl2 tham gia phản ứng
a) \(n_{NaOH}=\dfrac{60.11,2\%}{40}=0,168\left(mol\right)\)
PTHH: \(2NaOH+MgCl_2\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
0,168---->0,084----->0,084
b) \(m_{kt}=m_{Mg\left(OH\right)_2}=0,084.58=4,872\left(g\right)\)
c) \(C\%_{MgCl_2}=\dfrac{0,084.95}{190}.100\%=4,2\%\)
Đúng 2
Bình luận (1)
: Cho 11 gam hỗn hợp hai kim loại Al và Fe tác dụng vừa đủ với V ml dd H2SO4 0,2M, sau phản ứng thu được dung dịch X và khí Y. Cho dung dịch X tác dụng vừa đủ với dung dịch NaOH 10%, thì khối lượng kết tủa lớn nhất thu được là 24,6 gam.a/ Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu?b/ Tính V?c/ Tính khối lượng dung dịch NaOH cần dùng ở trên?d/ Đem kết tủa nung ngoài không khí đến khối lượng không đổi thì thu được bao nhiêu gam chất rắn?
Đọc tiếp
: Cho 11 gam hỗn hợp hai kim loại Al và Fe tác dụng vừa đủ với V ml dd H2SO4 0,2M, sau phản ứng thu được dung dịch X và khí Y. Cho dung dịch X tác dụng vừa đủ với dung dịch NaOH 10%, thì khối lượng kết tủa lớn nhất thu được là 24,6 gam.
a/ Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu?
b/ Tính V?
c/ Tính khối lượng dung dịch NaOH cần dùng ở trên?
d/ Đem kết tủa nung ngoài không khí đến khối lượng không đổi thì thu được bao nhiêu gam chất rắn?
\(a,\) Đặt \(n_{Al}=x(mol);n_{Fe}=y(mol)\)
\(\Rightarrow 27x+56y=11(1)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\ Al_2(SO_4)_3+6NaOH\to 2Al(OH)_3\downarrow+3Na_2SO_4\\ FeSO_4+2NaOH\to Fe(OH)_2\downarrow+Na_2SO_4\\ \Rightarrow n_{Al(OH)_3}=x;n_{Fe(OH)_2}=y\\ \Rightarrow 78x+90y=24,6(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,2(mol)\\ y=0,1(mol) \end{cases} \Rightarrow \begin{cases} m_{Al}=0,2.27=5,4(g)\\ m_{Fe}=11-5,4=5,6(g) \end{cases}\)
\(b,\Sigma n_{H_2SO_4}=1,5x+y=0,4(mol)\\ \Rightarrow V_{dd_{H_2SO_4}}=\dfrac{0,4}{0,2}=2(l)\\ c,\Sigma n_{NaOH}=3x+2y=0,8(mol)\\ \Rightarrow m_{dd_{NaOH}}=\dfrac{0,8.40}{10\%}=320(g)\\ d,2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ Fe(OH)_2\xrightarrow{t^o}FeO+H_2O\\ \Rightarrow n_{Al_2O_3}=0,1(mol);n_{FeO}=0,1(mol)\\ \Rightarrow m_{\text{chất rắn}}=0,1.102+0,1.72=17,4(g)\)
Đúng 1
Bình luận (0)
Câu 10: Cho 200ml dung dịch AlCl3 1M tác dụng với dung dịch NaOH 0,5M. Sau phản ứng thu được một kết tủa keo, lấy kết tủa đem nung đến khối lượng không đổi thu được 5,1 gam chất rắn. Tính thể tích dung dịch NaOH đã tham gia phản ứng.
\(n_{AlCl_3}=0.2\cdot1=0.2\left(mol\right)\)
\(n_{NaOH}=0.5V\left(mol\right)\)
\(n_{Al_2O_3}=\dfrac{5.1}{102}=0.05\left(mol\right)\)
\(2Al\left(OH\right)_3\underrightarrow{^{^{t^0}}}Al_2O_3+3H_2O\)
\(0.1...............0.05\)
TH1 : Al(OH)3 không bị hòa tan.
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3+3NaCl\)
\(0.1...........0.3................0.1\)
\(\Leftrightarrow V=\dfrac{0.3}{0.5}=0.6\left(l\right)\)
TH2 : Al(OH)3 bị hòa tan một phần
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3+3NaCl\)
\(0.2...........0.6................0.2\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
\(0.5V-0.6...0.5V-0.6\)
\(n_{Al\left(OH\right)_3}=0.2+0.5V-0.6=0.1\left(mol\right)\)
\(\Rightarrow V=1\left(l\right)\)
Đúng 4
Bình luận (1)
Cho dung dịch NaOH 10% tác dụng vừa đủ với 48,75 gam FeCl3 . a, Tính khối lượng kết tủa thu được. b, Tính khối lượng dd NaOH đã dùng. c, Tính nồng độ % các chất có trong dd sau phản ứng. d, xác định thể tích dung dịch H2SO4 20% có khối lượng riêng 1,14g/ml cần dùng để hòa tan hết lượng kết tủa thu được ở trên.
\(n_{FeCl_3}=\dfrac{48,75}{162,5}=0,3(mol)\\ 3NaOH+FeCl_3\to Fe(OH)_3\downarrow+3NaCl\\ \Rightarrow n_{Fe(OH)_3}=0,3(mol);n_{NaOH}=n_{NaCl}=0,9(mol)\\ a,m_{Fe(OH)_3}=0,3.107=32,1(g)\\ b,m_{dd_{NaOH}}=\dfrac{0,9.40}{10\%}=360(g)\\ c,C\%_{NaCl}=\dfrac{0,9.58,5}{360+48,75-32,1}.100\%=13,98\%\\ \)
\(d,2Fe(OH)_3+3H_2SO_4\to Fe_2(SO_4)_3+6H_2O\\ \Rightarrow n_{H_2SO_4}=0,45(mol)\\ \Rightarrow m_{dd_{H_2SO_4}}=\dfrac{0,45.98}{20\%}=220,5(g)\\ \Rightarrow V_{dd_{H_2SO_4}}=\dfrac{220,5}{1,14}=193,42(ml)\)
Đúng 2
Bình luận (0)
Cho m gam Mg tác dụng vừa đủ với 200ml dung dịch CH_3COOH 1m.Sau phản ứng thu được dung dịch A và V lít khí ở đktca.Tính m và Vb.Cần lên men bao nhiêu ml dung dịch rượu etylic 8 độ để thu được lượng axit axetic đủ tham gia phản ứng với lượng Mg ở trên?Biết hiệu suất phản ứng là 100%, D_{rượu}_{etylic}0,8g/ml (Cho Mg24;C12;H1;O16)
Đọc tiếp
Cho m gam Mg tác dụng vừa đủ với 200ml dung dịch \(CH_3COOH\) 1m.Sau phản ứng thu được dung dịch A và V lít khí ở đktc
a.Tính m và V
b.Cần lên men bao nhiêu ml dung dịch rượu etylic 8 độ để thu được lượng axit axetic đủ tham gia phản ứng với lượng Mg ở trên?Biết hiệu suất phản ứng là 100%, \(D_{rượu}\)\(_{etylic}\)=0,8g/ml
(Cho Mg=24;C=12;H=1;O=16)
a) PTHH: \(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\uparrow\)
Ta có: \(n_{CH_3COOH}=0,2\cdot1=0,2\left(mol\right)\)
\(\Rightarrow n_{Mg}=n_{H_2}=0,1\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,1\cdot24=2,4\left(g\right)\\V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\end{matrix}\right.\)
b) PTHH: \(C_2H_5OH+O_2\xrightarrow[]{men}CH_3COOH+H_2O\)
Theo PTHH: \(n_{C_2H_5OH}=n_{CH_3COOH}=0,2\left(mol\right)\)
\(\Rightarrow m_{ddC_2H_5OH}=\dfrac{0,2\cdot46}{8\%}=115\left(g\right)\) \(\Rightarrow V_{C_2H_5OH}=\dfrac{115}{0,8}=143,75\left(ml\right)\)
Đúng 3
Bình luận (2)
Cho 250 gam dung dịch MgCl2 19% phản ứng vừa đủ với dung dịch NaOH 8%
a. Tính khối lượng dung dịch NaOH cần dùng.
b. Lọc toàn bộ kết tủa, nhiệt phân hoàn toàn thu được x gam chất rắn. Tính x.
MgCl2+2NaOH->Mg(OH)2+2NaCl
0,5-------1-------------0,5
Mg(OH)2-to>MgO+H2O
0,5----------------0,5
m Mgcl2=47,5g
=>n Mgcl2=0,5 mol
=>m NaOH=1.40=40g
=>m ddNaOH=500g
=>m MgO=0,5.40=20g
Đúng 2
Bình luận (0)
MgCl2 (0,5 mol) + 2NaOH (1 mol) \(\rightarrow\) Mg(OH)2\(\downarrow\) (0,5 mol) + 2NaCl.
a) Khối lượng dung dịch NaOH cần dùng:
m=1.40.100:8=500 (g).
b) Mg(OH)2 (0,5 mol) \(\underrightarrow{t^o}\) MgO (0,5 mol) + H2O.
Khối lượng chất rắn MgO thu được là:
x=0,5.40=20 (g).
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 50 gam hỗn hợp X gồm FeO, CuO, Fe3O4 trong dung dịch axit HCl vừa đủ cho đến khi phản ứng xảy ra hoàn toàn thì thu được dung dịch Y chứa 105 gam muối clorua kim loại. Tính khối lượng kết tủa thu được khi cho Y tác dụng với dung dịch NaOH dư? A. 32 gam B. 68 gam C. 40 gam D. 60 gam
Đọc tiếp
Hòa tan hoàn toàn 50 gam hỗn hợp X gồm FeO, CuO, Fe3O4 trong dung dịch axit HCl vừa đủ cho đến khi phản ứng xảy ra hoàn toàn thì thu được dung dịch Y chứa 105 gam muối clorua kim loại. Tính khối lượng kết tủa thu được khi cho Y tác dụng với dung dịch NaOH dư?
A. 32 gam
B. 68 gam
C. 40 gam
D. 60 gam
M2On→ MCln →M(OH)n
nO/X =(105-50) /55 = 1 (mol)
Tiếp tục tăng giảm khối lượng 1Cl → 1OH
Mỗi mol Cl hoán đổi như vậy thì khối lượng giảm 18,5 gam
→ m↓ =105 – 18,5.2 = 68 gam
Chọn đáp án B
Đúng 0
Bình luận (0)