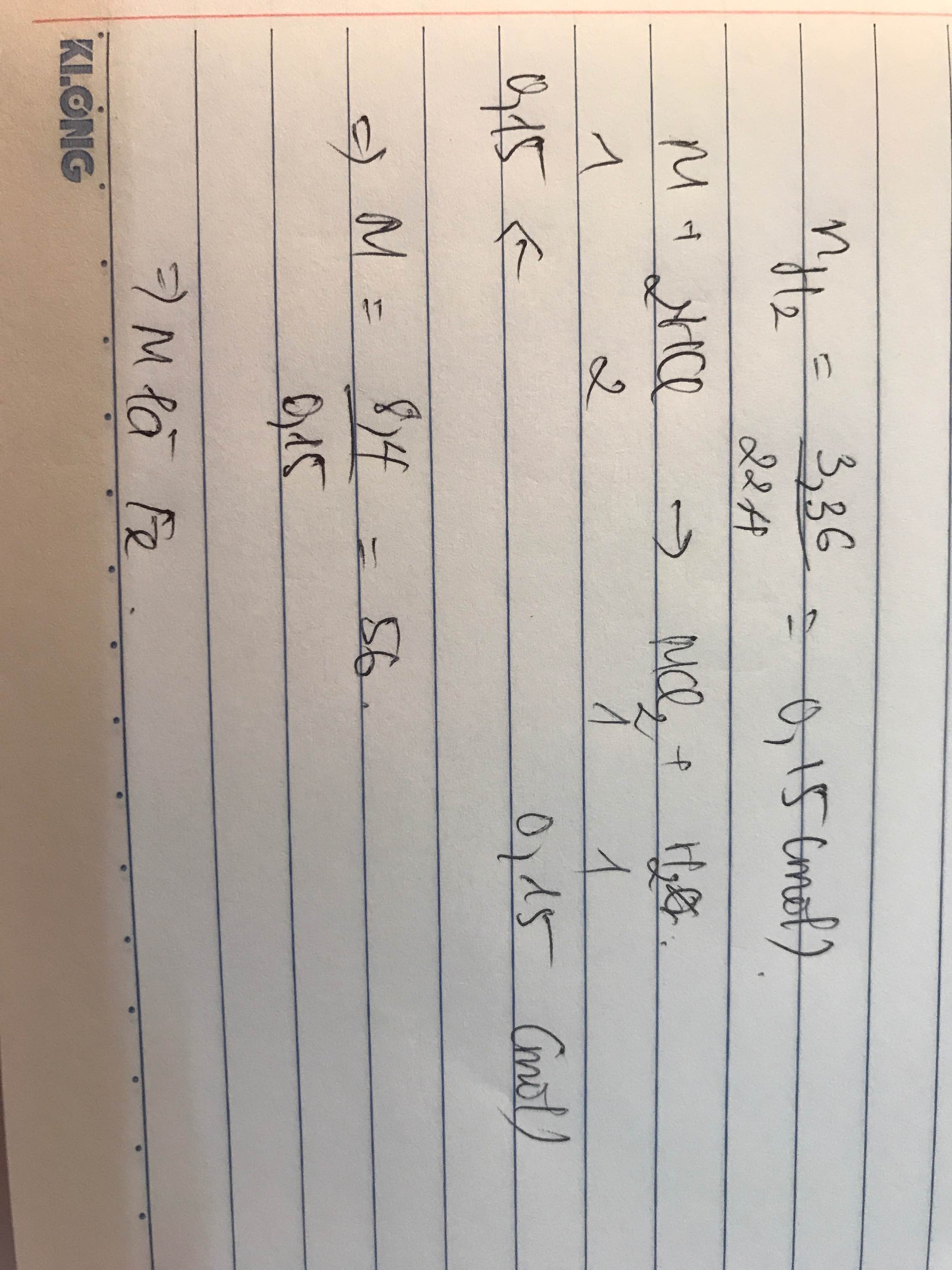Hoà tan hoàn toàn 0,1022 gam một muối kim loại hóa trị hai MCO3 trong 20,0ml dung dịch HCl 0,080M. Để trung hòa lượng HCl dư cần 5,64ml dung dịch NaOH 0,10M. Xác định kim loại M

Những câu hỏi liên quan
Cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,7185 lít khí đo ở đkc và dung dịch A.
a. Xác định kim loại M
b. Để phản ứng hết dung dịch A cần 500 ml dung dịch NaOH 1M. Tính C% các chất trong dung dịch A
\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
0,15<-0,3<---0,15<----0,15
a. \(M=\dfrac{8,4}{0,15}=56\left(g/mol\right)\)
Vậy M là kim loại Fe.
b. \(n_{NaOH}=0,5.1=0,5\left(mol\right)\)
\(HCl+NaOH\rightarrow NaCl+H_2O\)
0,2<-----0,2
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,15----->0,3
\(m_{dd.HCl}=\dfrac{\left(0,3+0,2\right).36,5.100\%}{10\%}=182,5\left(g\right)\)
\(m_{dd.A}=8,4+182,5-0,15.2=190,6\left(g\right)\)
\(C\%_{FeCl_2}=\dfrac{127.0,2.100\%}{190,6}=13,33\%\)
\(C\%_{HCl.dư}=\dfrac{0,3.36,5.100\%}{190,6}=5,75\%\)
Đúng 2
Bình luận (0)
hòa tan hoàn toàn 19,5 gam một kim loại M ( M có hóa trị 2 trong hợp chất ) dung dịch HCl 1M dư thu được dung dịch A và 6,72 lít khí H2 (ở đktc )
a) xác định kim loại M.
b) đẻ trung hòa axits dư trong A cần 200ml dung dịch NaOH 1M. tính thể tích dung dịch HCl 1M đã dùng và nồng độ mol của dung dịch A ( coi thể tích dung dịch A bằng thể tích dung dịch HCl ban đầu )
nH2=\(\frac{6,72}{22,4}=0,3\)mol
PTHH
M+2HCl--> MCl2+H2
0,3mol<---------------0,3mol
=>MM=\(\frac{19,5}{0,3}=64\)
=> km loại là kẽm (Zn)
b) nNaOH=0,2.1=0,2 mol
PTHH
NaOH+HCl-->NaCl + H2O
0,2 mol--> 0,2 mol
---> thể tích HCl 1M đã dùng là V=\(\frac{0,2+0,3}{1}=0,5\)lít
=> CM(ZnCl2)=\(\frac{0,3}{0,5}=0,6M\)
Đúng 0
Bình luận (0)
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn 8,4 gam kim loại R (hóa trị không đổi) vào 200 ml dung dịch HCl 2,5M. Để trung hòa lượng axit dư sau phản ứng phải dùng 80gam dung dịch NaOH 10%
a) Xác định kim loại R
b) Trộn 2,1 gam MgCO3 và 8,4 gam R trên rồi cho tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít hỗn hợp 2 khí (ở đktc) có tỉ khối so với H2 bằng 31. Xác định V
1) Xác định tên kim loại A và M khi:a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
Đọc tiếp
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
Đúng 1
Bình luận (0)
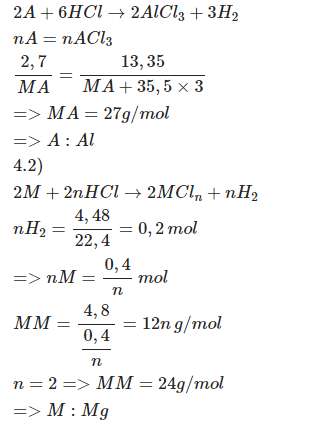
\(\Rightarrow\) \(M:mg\)
Bài 1 :Hòa tan hoàn toàn 2,4 gam kim loại M hóa trị II vào dung dịch có chứa 8,76 gam HCL ( lấy dư 20% lượng cần thiết để hòa tan hết kim loại.Phản ứng theo sơ đồ : M + HCL - MCL2 +H2.Tìm kim loại M.Bài 2: Hòa tan hết 1,35 gam kim loại M trong dung dịch có chứa 9,8 gam H2SO4 . Sau phản ứng người ta phát hiện được 2,48 gam H2SO4 còn dư và thu được sản phẩm gồm muối sunfat của kim loại M và khí H2.Tìm kim loại M
Đọc tiếp
Bài 1 :Hòa tan hoàn toàn 2,4 gam kim loại M hóa trị II vào dung dịch có chứa 8,76 gam HCL ( lấy dư 20% lượng cần thiết để hòa tan hết kim loại.Phản ứng theo sơ đồ : M + HCL -> MCL2 +H2.
Tìm kim loại M.
Bài 2: Hòa tan hết 1,35 gam kim loại M trong dung dịch có chứa 9,8 gam H2SO4 . Sau phản ứng người ta phát hiện được 2,48 gam H2SO4 còn dư và thu được sản phẩm gồm muối sunfat của kim loại M và khí H2.Tìm kim loại M
Bài 1 : Hòa tan hoàn toàn 9.6 gam kim loại R trong dung dịch H2SO4 đặc nóng, sau phản ứng thu được 3.36 lít SO2. Tìm R.Bài 2 : Hòa tan 6.75 gam một kim loại M chưa rõ hóa trị vào dung dịch axit thì cần 50 ml dung dịch axit HCl 1.5M. XÁc định kim loại M.Bài 3 : Hòa tan hoàn toàn 2 hỗn hợp một kim loại hóa trị II và một kim loại hóa trị III cần 31.025 gam dung dịch HCl 20%. a) Tính V H2 thoát ra. b) Tính khối lượng muối khan tạo thành.
Đọc tiếp
Bài 1 : Hòa tan hoàn toàn 9.6 gam kim loại R trong dung dịch H2SO4 đặc nóng, sau phản ứng thu được 3.36 lít SO2. Tìm R.
Bài 2 : Hòa tan 6.75 gam một kim loại M chưa rõ hóa trị vào dung dịch axit thì cần 50 ml dung dịch axit HCl 1.5M. XÁc định kim loại M.
Bài 3 : Hòa tan hoàn toàn 2 hỗn hợp một kim loại hóa trị II và một kim loại hóa trị III cần 31.025 gam dung dịch HCl 20%.
a) Tính V H2 thoát ra.
b) Tính khối lượng muối khan tạo thành.
Gọi KL là R (KL có hoá trị n)
2R + 2nH2SO4-> R2(SO4)n + SO2 + 2nH2O
nSO2=3,36/22,4=0, 15(mol) lắp vào pt suy ra nR=0,3/n (mol).
MR=9,6.n/0,3
vì chưa biết hoá trị n nên ta lập bảng tìm hoá trị. R là KL nên có hoá trị 1, 2 hoặc 3. Cho n lần lượt bằng 1, 2,3 để tìm ra MR thoả mãn. Với n=2 thì MR=64(tm). KL là Cu
Đúng 0
Bình luận (0)
Bài 1 :Gọi KL là R (KL có hoá trị n)
2R + 2nH2SO4-> R2(SO4)n + SO2 + 2nH2O
nSO2=3,36/22,4=0, 15(mol) lắp vào pt suy ra nR=0,3/n (mol).
MR=9,6.n/0,3
vì chưa biết hoá trị n nên ta lập bảng tìm hoá trị. R là KL nên có hoá trị 1, 2 hoặc 3. Cho n lần lượt bằng 1, 2,3 để tìm ra MR thoả mãn. Với n=2 thì MR=64(tm). KL là Cu
Đúng 0
Bình luận (0)
Bài 2 : Hòa tan 6.75 gam một kim loại M chưa rõ hóa trị vào dung dịch axit thì cần 50 ml dung dịch axit HCl 1.5M. XÁc định kim loại M.
Bài 3 : Hòa tan hoàn toàn 2 hỗn hợp một kim loại hóa trị II và một kim loại hóa trị III cần 31.025 gam dung dịch HCl 20%.
a) Tính V H2 thoát ra.
b) Tính khối lượng muối khan tạo thành.
m(HCl)=31.025x20/100=6.205
a/vì số mol H2 luôn bằng 1/2 số mol HCl (theo định luật bảo toàn nguyên tố)
Mà nHCl=0.17(mol)
=>nH2=0.17/2=0.085(mol)
=>VH2=0.085x22.4=1.904(l)
Theo định luật bảo toàn khối lượng có:
m(muối) = m(kim loại) + m(axit) - m(H2)
=2 + 6.205 - 0.085x2
=8.035(g)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 24 gam một kim loại hóa trị 2 trong 750 ml H2SO4 1M. Để trung hòa axit dư trong dung dịch thu được phải dùng hết 150 ml dung dịch NaOH 2M. xác định kim loại
\(n_{NaOH} = 0,15.2 = 0,3(mol)\\ 2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O\\ n_{H_2SO_4\ dư} = \dfrac{1}{2}n_{NaOH} = 0,15(mol)\\ n_{H_2SO_4\ pư} = 0,75 - 0,15 = 0,6(mol)\\ \)
Gọi kim loại cần tìm là R
\(R + H_2SO_4 \to RSO_4 + H_2\\ n_R = n_{H_2SO_4} = 0,6(mol)\\ \Rightarrow M_R = \dfrac{24}{0,6} =40(Ca)\)
Vậy kim loại cần tìm là Canxi
Đúng 2
Bình luận (0)