Xác định khối lượng từng nguyên tố trong hợp chất B, biết khi đốt cháy hoàn toàn B cần dùng 2,24l khí oxi ( ĐKTC), sau phản ứng thu được 2,241l CO2 ( ĐKTC), 0,9g nước và 5,3g Na2CO3

Những câu hỏi liên quan
đốt cháy hoàn toàn khí Y cần dùng hết 13,44 km3 khí oxi,sau khi phản ứng kết thúc thu được 6,72dm3 khí CO2 và 10,08 hơi nước(đktc)
a)hợp chất Y do những nguyên tố hóa học nào tạo nên,tính khối lượng chất Y đem đốt cháy.
b)biết tỉ khối hơi của chất Y với khí oxi là 2,5,xác định CT phân tử của Y.
Đốt cháy hoàn toàn 2,3 gam một hợp chất bằng khí oxi, sau phản ứng thu được 2,24 lít CO2 (dktc) và 2,7 gam H2O.
a: Xác định thành phần định tính các nguyên tố trong hợp chất.
b: Tính khối lượng từng nguyên tố trong 2,3 gam hợp chất
Đốt cháy hoàn toàn 2,24l hidrocacbon A thể khí thu được 6,72l khí CO2 và 5,4g hơi nước.
1) Xác định công thức phân tử của hidrocacbon, biết rằng thể tích khí đo ở đktc.
2) Tính khối lượng khí Oxi cần dùng cho phản ứng trên.
1) \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> nC = 0,3 (mol)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
\(n_A=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Số nguyên tử C = \(\dfrac{0,3}{0,1}=3\) (nguyên tử)
Số nguyên tử H = \(\dfrac{0,6}{0,1}=6\) (nguyên tử)
CTHH: C3H6
2)
PTHH: 2C3H6 + 9O2 --to--> 6CO2 + 6H2O
0,1--->0,45
=> mO2 = 0,45.32 = 14,4 (g)
Đúng 2
Bình luận (0)
Câu 1: Đốt cháy hoàn toàn 15,6 gam hỗn hợp A gồm C và S trong 22,4 lít khí oxi (đktc), thu được hỗn hợp khí C gồm CO2 và SO2.a/ Viết các PTHH xảy ra.b/ Biết khí oxi đã dùng dư 25% so với lượng cần để phản ứng.- Tính khối lượng từng chất trong A.- Tính tỉ khối của hỗn hợp C đối với H2.Câu 2: Trộn 10 lít N2 với 40 lít H2 rồi nung nóng một thời gian, sau đó đưa về to và áp suất ban đầu thấy thu được 42 lít hỗn hợp A gồm N2, H2 và NH3.a/ Tính thể tích H2 đã phản ứng. b/ Tính hiệu suất phản ứng.c/...
Đọc tiếp
Câu 1: Đốt cháy hoàn toàn 15,6 gam hỗn hợp A gồm C và S trong 22,4 lít khí oxi (đktc), thu được hỗn hợp khí C gồm CO2 và SO2.
a/ Viết các PTHH xảy ra.
b/ Biết khí oxi đã dùng dư 25% so với lượng cần để phản ứng.
- Tính khối lượng từng chất trong A.
- Tính tỉ khối của hỗn hợp C đối với H2.
Câu 2: Trộn 10 lít N2 với 40 lít H2 rồi nung nóng một thời gian, sau đó đưa về to và áp suất ban đầu thấy thu được 42 lít hỗn hợp A gồm N2, H2 và NH3.
a/ Tính thể tích H2 đã phản ứng.
b/ Tính hiệu suất phản ứng.
c/ Tính thể tích mỗi khí trong hỗn hợp A.
Đốt cháy hoàn toàn 2,3 gam X bằng khí oxi, sau phản ứng thu được 2,24 lít C O 2 đktc và 2,7 gam nước. Hỏi A được cấu tạo từ những nguyên tố hóa học nào. Tính khối lượng từng nguyên tố trong 2,3 gam X.
Vì A cháy sinh ra C O 2 và H 2 O nên A chứa C, H, và có thể có O.
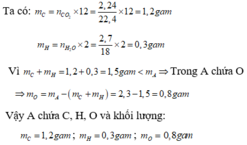
Đúng 0
Bình luận (0)
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Bài 7: Đốt cháy hoàn toàn 3,2 gam hợp chất A cần 8,96 lít khí O2 (đktc) thu được khí CO2 và H2O theo tỉ lệ mol là 1:2.
a. Tính khối lượng của từng nguyên tố trong hợp chất A.
b. Xác định CTPT của hợp chất A biết M = 16.
a)
Do \(\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1}{2}\)
=> \(\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
Giả sử A có CTHH là CxH4xOy
Gọi số mol của A là a (mol)
=> 12ax + 4ax + 16ay = 3,2
=> ax + ay = 0,2 (1)
Bảo toàn C: nCO2 = ax (mol)
Bảo toàn H: nH2O = 2ax (mol)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn O: \(ay+0,4.2=2ax+2ax\)
=> 4ax - ay = 0,8 (2)
(1)(2) => ax = 0,2 (mol); ay = 0 (mol)
=> A chỉ chứa C và H
\(\left\{{}\begin{matrix}n_C=ax\left(mol\right)\\n_H=4ax\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_C=12.ax=2,4\left(g\right)\\m_H=1.4ax=0,8\left(g\right)\end{matrix}\right.\)
b)
Xét \(\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
=> CTPT: (CH4)n
Mà M = 16 g/mol
=> n = 1
=> CTPT: CH4
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 7,4 gam hỗn hợp CH4 và C4H10 trong không khí biết rằng sau phản ứng thu được 22 gam khí CO2.
a. Tính khối lượng các chất có trong hỗn hợp đầu ?
b. Tính VO2 cần dùng ( đktc) để đốt cháy hết hỗn hợp trên?
\(a,Đặt:n_{CH_4}=a\left(mol\right);n_{C_4H_{10}}=b\left(mol\right)\left(a,b>0\right)\\ PTHH:CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ 2C_4H_{10}+13O_2\rightarrow\left(t^o\right)8CO_2+10H_2O\\ \Rightarrow\left\{{}\begin{matrix}16a+58b=7,4\\22,4a+22,4.4b=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}m_{CH_4}=0,1.16=1,6\left(g\right)\\m_{C_4H_{10}}=0,1.58=5,8\left(g\right)\end{matrix}\right.\\ b,n_{O_2}=2a+\dfrac{13}{2}b=2.0,1+6,5.0,1=0,85\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,85.22,4=19,04\left(l\right)\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 7g hợp chất hữu cơ A thu được 11,2 l khí CO2 đo ở đktc và 9 g nước.
a, Xác định CTHH của A biết tỉ khối dA/CH4=1,75
b, Tính thể tích không khí cần dùng để đốt cháy hoàn toàn a biết oxi chiếm 20% không khí



















