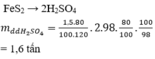Một loại quặng sắt chứa 92 % Fe2O3 được sử dụng để điều chế Sắt. Nếu sử dụng CO để khử hoàn toàn 1,5 tấn quặng thì thu được bao nhiêu Sắt.

Những câu hỏi liên quan
1 một kim loại X chứa 64% Fe2O3, quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z có thể điều chế được 481,25 kg gang chứa 4% cacbon.( Gang là hợp chất của sắt và cacbon).2 Phân hủy hoàn toàn một hợp chất A ở nhiệt độ cao theo phương trình sau: 4A nhiệt phân------ 4B+ C + 2DCác sản phẩm tạo thành đều ở thể khí. Tính tỉ khối của hỗn hợp khí sau phản ứng so với khí hidro là 18. Xác định khối lượng mol của chất A C...
Đọc tiếp
1> một kim loại X chứa 64% Fe2O3, quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z có thể điều chế được 481,25 kg gang chứa 4% cacbon.( Gang là hợp chất của sắt và cacbon).
2> Phân hủy hoàn toàn một hợp chất A ở nhiệt độ cao theo phương trình sau:
4A nhiệt phân------> 4B+ C + 2D
Các sản phẩm tạo thành đều ở thể khí. Tính tỉ khối của hỗn hợp khí sau phản ứng so với khí hidro là 18. Xác định khối lượng mol của chất A
Các bạn giúp tui nha cám ơn mn nhiều:))
2)
Giả sử có 1 mol A
PTHH: 4A --to--> 4B + C + 2D
1------->1-->0,25->0,5
=> nkhí sau pư = 1 + 0,25 + 0,5 = 1,75 (mol)
BTKL: mA = mB + mC + mD
Có \(\overline{M}=\dfrac{m_B+m_C+m_D}{1,75}=18.2=36\)
=> mA = 63 (g)
=> \(M_A=\dfrac{63}{1}=63\left(g/mol\right)\)
Đúng 3
Bình luận (0)
câu 1) đề có nói rõ điều chế 481,25kg gang từ bao nhiêu Z không vậy bn :) ?
Đúng 1
Bình luận (3)
1)
Giả sử a + b = 1 (tấn)
Do cacbon chiếm 4%
=> Fe chiếm 96% khối lượng gang
\(m_{Fe}=\dfrac{481,25.10^3.96}{100}=462.10^3\left(g\right)\)
=> \(n_{Fe}=\dfrac{462.10^3}{56}=8,25.10^3\left(mol\right)\)
\(m_{Fe_2O_3\left(X\right)}=\dfrac{a.10^6.64}{100}=640.10^3.a\left(g\right)\)
=> \(n_{Fe_2O_3}=\dfrac{640.10^3.a}{160}=4.10^3.a\left(mol\right)\)
\(m_{Fe_3O_4\left(Y\right)}=\dfrac{b.10^6.69,6}{100}=696.10^3.b\left(g\right)\)
=> \(n_{Fe_3O_4}=\dfrac{696.10^3.b}{232}=3.10^3.b\left(mol\right)\)
Bảo toàn Fe:
2.4.103.a + 3.3.103.b = 8,25.103
=> 8a + 9b = 8,25
Mà a + b = 1
=> a = 0,75; b = 0,25
=> \(\dfrac{a}{b}=\dfrac{0,75}{0,25}=\dfrac{3}{1}\)
Đúng 1
Bình luận (0)
một nhà máy cần thu 50000l khí sunfurơ mỗi ngày. Hỏi để thu được lượng khí trên thì nhà ,áy cần sử dụng bao nhiêu tấn quặng pirit sắt. Giả sử quặng pirit chứa 98% FeS2, hiệu suất phản ứng là 95%(khi đo ở đktc)
Quặng Pirit (FeS2)---------> SO2
Bảo toàn nguyên tố S: \(n_{FeS_2}.2=n_{SO_2}.1=\dfrac{50000}{22,4}=\dfrac{15625}{7}\Rightarrow n_{FeS_2}=\dfrac{15625}{14}\)(mol)
Vì H=95% => \(n_{FeS_2}=\dfrac{15625}{14}.\dfrac{100}{95}=1174,81\left(mol\right)\)
=> \(m_{FeS_2}=1174,81.120=140977,2\left(kg\right)\)
Vì quặng pirit chứa 98% FeS2
=> \(m_{quặng}=140977,2.\dfrac{100}{98}=143854,3\left(kg\right)\approx143,85\left(tấn\right)\)
Đúng 1
Bình luận (0)
A là một loại quặng sắt chứa 60% Fe2O3; B là loại quặng sắt khác chứa 69,6% Fe3O4. Hỏi trong một tấn quặng A hoặc B có chứa bao nhiêu kg sắt? 2. Trộn quặng A với quặng B theo tỉ lệ khối lượng mA:mB = 2:5 ta được quặng C có bao nhiêu kg sắt
người ta điều chế sắt từ oxit sắt từ Fe3O4 theo sơ đồ CO+Fe3O4 - - - -> Fe+CO2 a, nếu dùng 1 tấn quặng chứa 90% là Fe3O4 thì lượng sắt kim loại thu được là bao nhiêu kg? b, muốn được 1 tấn sắt thì phải dùng bao nhiêu tấn quặng nói trên?
1 tấn=100000kg
\(m_{Fe_3O_4}=1000000.90\%=900000\left(g\right)\)
\(\rightarrow n_{Fe_3O_4}=\dfrac{900000}{232}=\dfrac{112500}{29}\left(mol\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(\dfrac{112500}{29}\) \(\dfrac{337500}{87}\) (mol)
\(\rightarrow m_{Fe}=\dfrac{337500}{87}.56\approx217241,38\left(g\right)\approx217,24\left(kg\right)\)
b.
\(n_{Fe}=\dfrac{1000000}{56}=\dfrac{125000}{7}\left(mol\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(\dfrac{375000}{7}\) \(\dfrac{125000}{7}\) (mol)
\(\rightarrow m_q=\dfrac{375000}{7}.232.100:90=13809523\left(g\right)=13809,5\left(kg\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
Đúng 0
Bình luận (0)
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch
H
2
S
O
4
98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80%
F
e
S
2
(hiệu suất toàn quá trình là 80%) là A. 0,80 tấn B. 1,60 tấn C. 1,25 tấn D. 2,00 tấn
Đọc tiếp
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch H 2 S O 4 98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% F e S 2 (hiệu suất toàn quá trình là 80%) là
A. 0,80 tấn
B. 1,60 tấn
C. 1,25 tấn
D. 2,00 tấn
Câu 1. Dùng 100 tấn quặng pirit sắt chứa 72% FeS2 để điều chế H2SO4. Cho toàn bộ axit thu được tác dụng vs Cu điều chế CuSO4.5H2O sau đó pha thành dd CuSO4 để trừ nấm thực vật. Tính m (tấn) CuSO4.5H2O thu được. biết hiệu suất cả quá trình là 80%.
Khử một lượng quặng hemantit chứa 80% (
Fe
2
O
3
) thu được 1,68 tấn sắt, khối lượng quặng cần lấy là: A. 2,4 tấn B. 2,6 tấn C. 2,8 tấn D. 3,0 tấn
Đọc tiếp
Khử một lượng quặng hemantit chứa 80% ( Fe 2 O 3 ) thu được 1,68 tấn sắt, khối lượng quặng cần lấy là:
A. 2,4 tấn
B. 2,6 tấn
C. 2,8 tấn
D. 3,0 tấn

→ m F e 2 O 3 = ( 1 , 68 . 160 ) : 112 = 2 , 4 t ấ n .
![]()
Đúng 0
Bình luận (0)
Người ta trộn hai loại quặng sắt với nhau, một loại chứa 72% sắt, loại thứ hai chứa 58% sắt được một loại quặng chứa 62% sắt. Nếu tăng khối lượng của mỗi loại quặng thêm 15 tấn thì được một loại quặng chứa 63,25% sắt. Tìm khối lượng quặng của mỗi loại đã trộn.
Gọi khối lượng quặng loại thứ nhất là x ( tấn), loại thứ hai là y (tấn)
Điều kiện: x > 0; y > 0
Lượng sắt nguyên chất có trong mỗi loại quặng bằng lượng sắt có trong hỗn hợp ta có phương trình:
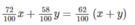
Thêm mỗi loại quặng 15 tấn ta được hỗn hợp chứa 63,25% sắt, ta có phương trình:
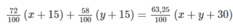
Ta có hệ phương trình:
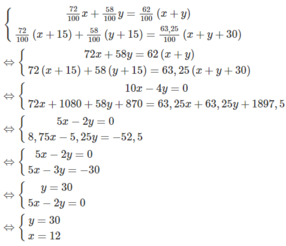
Cả hai giá trị x = 12; y = 30 thỏa mãn điều kiện bài toán.
Vậy loại quặng thứ nhất có 12 tấn, loại quặng thứ hai có 30 tấn.
Đúng 0
Bình luận (0)
Có 50 tấn quặng chứa 55% sắt, người ta trộn thêm 30 tấn quặng sắt. Sau khi trộn xong thì hỗn hợp quặng thu được chứa 35 tấn sắt. Hỏi trong 30 tấn quặng sắt được trộn thêm chứa bao nhiêu phần trăm sắt?
Số tấn sắt có trong 50 tấn quặng sắt :
50 x 55% = 27,5 tấn
=> Trong 30 tấn quặng sắt có : 35 - 27,5 = 7,5 tấn sắt
=> Số phần trăm sắt có trong 30 tấn là : \(\frac{7,5}{30}.100\%=25\%\)
số tấn sắt có trong 50 tấn chúa 55% sắt là:
50 nhân 55%= 27,5 ( tấn )
số tấn sắt có trong 30 tấn quặng sắt là:
35-27,5=7,5 (tấn)
số phần trăm sắt có trong 30 tấn quặng là:
7,5/30 nhân 100%= 25%
đáp số : 25%
Xem thêm câu trả lời