1,Sơ đồ tượng trưng cho phản ứng giữa khí Hiđro và khí Clo tạo ra Axit CloHiđric.
a,Hãy cho biết liên kết giữa nguyên tử trong phân tử nào bị tách rời.
b,Phân tử nào được tạo ra.
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí hidro H 2 và chất đồng (II) oxit CuO tạo ra kim loại đồng và nước:
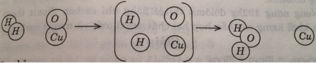
Hãy chỉ ra:
Liên kết giữa những nguyên tử trong phân tử nào bị tách rời, trg phân tử nào được tạo ra?
Liên kết giữa những nguyên tử trong phân tử H 2 và trong phân tử CuO bị tách rời, liên kết giữa những nguyên tử trong phân tử nước tạo ra.
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí hidro H 2 và khí clo C l 2 tạo ra axit clohidric HCl.
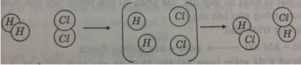
Hãy cho biết:
Liên kết giữa các nguyên tử thay đổi như thế nào? Phân tử nào biến đổi, phân tử nào được tạo ra?
Trước phản ứng: Hai nguyên tử hidro liên kết nhau, hay nguyên tử clo liên kết nhau.
Sau phản ứng: mỗi nguyên tử hidro liên kết với 1 nguyên tử clo, phân tử H 2 và C l 2 biến đổi. Phân tử HCl được tạo ra.
Hình dưới đây là sơ đồ tương trựng cho phản ứng: Giữa khí N2 và khí H2 tạo ra ammoniac NH3.
Hãy cho biết:
a) Tên các chất tham gia và sản phẩm?
b) Liên kết giữa các nguyên tử thay đổi như thế nào? Phân tử nào biến đổi, phân tử nào được tạo ra?
c) Số nguyên tử mỗi nguyên tố trước và sau phản ứng bằng bao nhiêu có giữ nguyên không?
a) Chất tham gia: khí nitơ, khí hiđro.
Chất tạo thành: khí amoniac.
b) Trước phản ứng hai nguyên tử H liên kết với nhau, hai nguyên tử nitơ cũng vậy. Sau phản ứng có 3 nguyên tử H liên kết với 1 nguyên tử N.
Phân tử hiđro và phân tử nitơ biến đổi phân tử ammoniac được tạo thành.
c) Số nguyên tử mỗi nguyên tố giữ nguyên trước và sau phản ứng số nguyên tử H là 6 và số nguyên tử N là 2.
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí hidro H 2 và khí clo C l 2 tạo ra axit clohidric HCl.
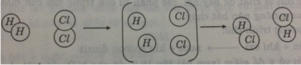
Hãy cho biết:
Trước và sau phản ứng số nguyên tử mỗi nguyên tố có thay đổi không?
Trước và sau phản ứng số nguyên tử mỗi nguyên tố không thay đổi.
Trong phản ứng hoá học giữa khí hiđro và khí oxi tạo ra nước, chỉ có liên kết giữa các nguyên tử H và O thay đổi (I), làm cho phân tử hiđro và phân tử oxi biến đổi thành phân tử nước (II). Nhận định nào sau đây đúng?
A. (I) đúng, (II) sai.
B. (I) sai, (II) đúng.
C. (I) và (II) đúng.
D. (I) và (II) đều sai.
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí hidro H 2 và chất đồng (II) oxit CuO tạo ra kim loại đồng và nước:
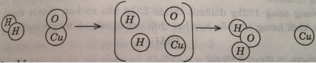
Hãy chỉ ra:
Mỗi phản ứng xảy ra với bao nhiêu phân tử của mỗi chất phản ứng, tạo ra bao nhiêu phân tủ ư nước và nguyên tử đồng?
Mỗi phản ứng xảy ra với 1 phân tử H 2 và 1 phân tử CuO, tạo ra 1 phân tử H 2 O và 1 nguyên tử Cu.
1. Biết rằng kim loại nhôm tác dụng với axit clohiđric HCl tạo ra khí hiđro và muối nhôm clorua AlCl3
a) Lập PTHH của phản ứng.
b) Cho biết tỉ lệ giữa số nguyên tử Al lần lượt với số phân tử của 3 chất trong phản ứng
\(a,2Al+6HCl\to 2AlCl_3+3H_2\)
\(b,\) số nguyên tử Al : số nguyên tử HCl = 1:3
số nguyên tử Al : số nguyên tử AlCl3 = 1:1
số nguyên tử Al : số nguyên tử H2 = 2:3
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí hidro H 2 và khí clo C l 2 tạo ra axit clohidric HCl.
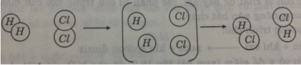
Hãy cho biết:
Tên các chất phản ứng và sản phẩm?
Chất phản ứng: khi hidro, khí clo.
Sản phẩm: axit clohidric.
Tính theo PTHH:
Bài 1: Cho 2,8 gam sắt tác dụng vừa đủ với dung dịch axit clohiđric(HCl) sau phản ứng tạo ra muối sắt (II) clorua (FeCl2) và khí hiđro bay lên.
a) Viết PTHH và cho biết tỉ lệ về số nguyên tử, số phân tử giữa các chất trong phản ứng.
b) Tính thể tích khí hiđro ở đktc?
c) Tính khối lượng axit clohiđric cần dùng cho phản ứng trên?
Bài 2: Cho 5,4 g nhôm vào dd HCl dư tao ra muối nhôm clorua (AlCl3) và khí H2
a. Viết PTHH và cho biết tỉ lệ về số nguyên tử, số phân tử giữa các chất trong phản ứng.
b. Tính thể tích khí Hiđro tạo tành ở đktc
c. Tính khối lượng muối nhôm clorua tạo thành
Fe + 2HCl –> FeCl2 + H2
a) Số mol Fe: 2,8/56=0,05 (mol)
Theo pthh số mol H2= 0,05 mol
Thể tích H2=0,05 x 22,4 = 1.12 (lít)
b) Theo pthh số mol HCl= 0,1 mol
Khối lượng HCl cần dùng: 0,1 x 36,5 = 3,65 (g)
trên là bài 1 đây là bài 2 nha
Số mol Al là:
Bài 1:
a, Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\) ( 1:2:1:1 )
b,
\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\\ \Rightarrow n_{H_2}=0,05.1=0,05mol\\ \Rightarrow V_{H_2}=0,05.22,4=1,12l\)
c, \(n_{HCl}=0,05.2=0,1mol\\ \Rightarrow m_{HCl}=0,1.36,5=3,65g\)
Bài 2:
a, 2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2 ( 2:6:2:3 )
b, \(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(\Rightarrow n_{H_2}=0,2.3=0,6mol\)
\(V_{H_2}=0,6.22,4=13,44l\)
c, \(n_{HCl}=0,2.6=1,2mol\\ \Rightarrow m_{HCl}=1,2.36,5=43,8g\)